Противовирусное для детей 8 лет: Противовирусные препараты для детей купить по низкой цене в интернет-аптеке с доставкой по Москве
Противірусні препарати для дітей: купити за найкращою ціною
Покупцям
Покупцям
Кошик
close
23 елементи(ів)
Сортувати заЦіна за зростаннямЦіна за спаданнямЗа відгукамиРейтингЗа популярністюАкційні
Ціна за зростанням
Ціна за спаданням
За відгуками
Рейтинг
За популярністю
Акційні
За популярністю
Фільтр
Показати
12 24 30 60
на сторінці
23 елементи(ів)
Сортувати заЦіна за зростаннямЦіна за спаданнямЗа відгукамиРейтингЗа популярністюАкційні
Ціна за зростанням
Ціна за спаданням
За відгуками
Рейтинг
За популярністю
Акційні
За популярністю
Фільтр
Показати
12 24 30 60
на сторінці
Оновлено: 07. 09.2022
09.2022
Провірено
Використання противірусних препаратів для дітей доцільно з метою профілактики і лікування захворювань, що мають вірусну етіологію. Специфіка їх застосування полягає в призначенні виключно безпечних засобів, що не роблять негативного впливу на імунітет дитини, в тому числі при тривалому прийомі.
Діти особливо уразливі до вірусних захворювань. Навіть якщо батьки ретельно оберігають дитину від інфекцій, повністю уникнути хвороби не вдається практично нікому. Для швидкого досягнення позитивних результатів необхідно вживати комплексні заходи, які дозволяють ефективно протидіяти вірусам і обмежувати їх життєдіяльність, мобілізувати захисні сили організму, усувати або полегшувати симптоматику захворювання, а також відновлюватися після перенесених хвороб.Противірусні препарати для дітей якраз і спрямовані на вирішення першого завдання – протидія вірусної інвазії. Однак різні засоби і діють по-різному.
Види противірусних засобів, придатних для пацієнтів дитячого віку
Залежно від принципу дії, розглянута категорія препаратів ділиться на дві великі групи – засоби, які мають імуностимулюючу дію і ліки, що зупиняють зростання кількості копій вірусу в організмі. Головна особливість препаратів першої групи полягає в тому, що вони не знищують безпосередньо збудників хвороби, а запускають в організмі ряд певних захисних реакцій. Сюди входять медикаменти, які містять в своєму складі інтерферон (речовина, що робить клітини несприйнятливими до дії вірусу), а також індуктори інтерферону. До останніх відносяться препарати, які не містять цієї речовини, але запускають його вироблення організмом дитини. Індуктори інтерферону можуть ефективно поєднуватися з іншими лікарськими засобами та мають вираженe терапевтичнe дію на початкових етапах захворювання.
Головна особливість препаратів першої групи полягає в тому, що вони не знищують безпосередньо збудників хвороби, а запускають в організмі ряд певних захисних реакцій. Сюди входять медикаменти, які містять в своєму складі інтерферон (речовина, що робить клітини несприйнятливими до дії вірусу), а також індуктори інтерферону. До останніх відносяться препарати, які не містять цієї речовини, але запускають його вироблення організмом дитини. Індуктори інтерферону можуть ефективно поєднуватися з іншими лікарськими засобами та мають вираженe терапевтичнe дію на початкових етапах захворювання.
Що стосується засобів, які припиняють зростання кількості вірусів, то дана група складається з наступних препаратів:
Інгібіторів нейрамінідази. Це високоефективні противірусні засоби, які надають деструктивний вплив на поверхневі антигени вірусів, без яких їх розмноження стає неможливим.
Медикаментів, які блокують M2-канали вірусів. У більшості випадків подібні противірусні ліки мають дуже високу ефективність і дають можливість швидко досягти потрібного ефекту.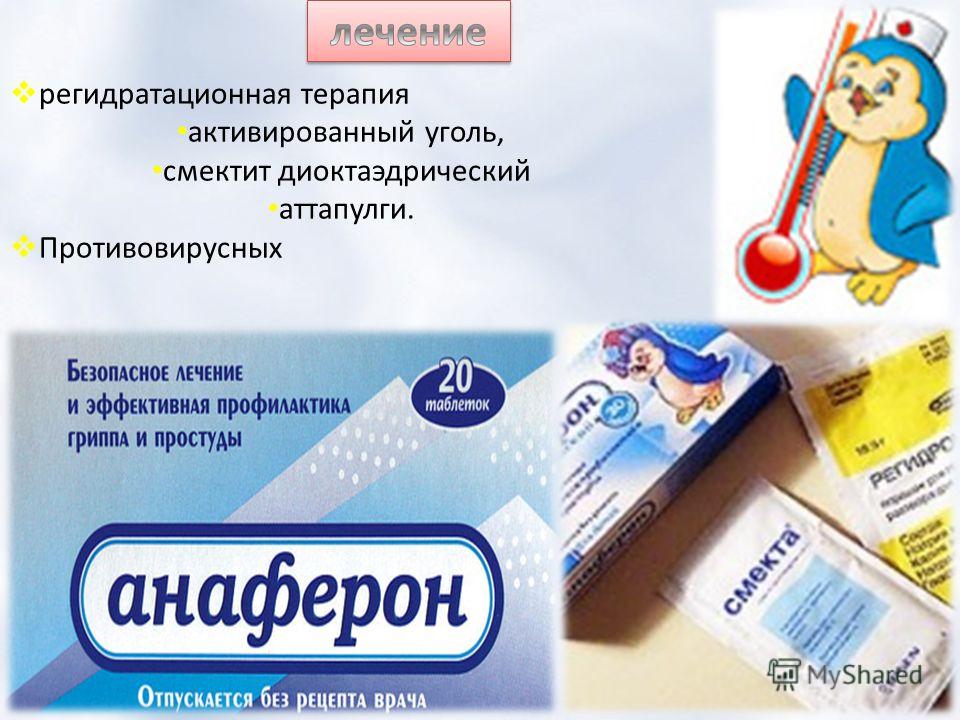 Єдине обмеження – вони протипоказані дітям у віці до 6-7 років.
Єдине обмеження – вони протипоказані дітям у віці до 6-7 років.
Доцільно використовувати комбіновані медикаментозні схеми лікування вірусних захворювань у дітей, проте поєднання має бути максимально обережним і чітким, а призначати його може тільки лікар.
Останні тенденції в терапії вірусних уражень полягають у використанні препаратів, які володіють не тільки противірусною та імуномодулюючою дією, але забезпечують репаративний (відновлюючий) ефект для слизових оболонок. Це дозволить суттєво полегшити симптоматику і помітно скоротити загальні терміни одужання.
Зверніть увагу
Сайт add.ua не несе відповідальності за можливі негативні наслідки, що виникають в результаті використання користувачами інформації, розміщеної на сайті.
Фільтр
Фільтр
Виробник
DHU (Німеччина)
Gedeon Richter (Угорщина)
Schwabe (Німеччина)
TEVA (Ізраїль)
Біолік (Україна, Ладижин)
Біофарма ЗАТ (Україна, Київ)
Інтерфармбіотек ТОВ (Україна)
ІнтерХім СП ВАТ (Україна, Одеса)
Істок-Плюс ТОВ (Україна, Запоріжжя)
Київський вітамінний завод ПАТ (Україна, Київ)
Фармак ВАТ (Україна, Київ)
Не знайдено
Форма товару
Краплі
Порошок
Розчин
Свічки
Сироп
Супозиторії
Таблетки
Не знайдено
Бренд
Амізон
Аміксин
Ізопринозин
Лаферон-Фармбіотек
Протефлазід
Кількість в упаковці
1
3
6
10
20
40
50
Не знайдено
Головний медикамент
Альфарекін
Амізон
Аміксин
Гропринозин
Лаферобіон
Лаферон-Фармбіотек
Назоферон
Новірин
Протефлазід
Умкалор
Не знайдено
Об’єм
5 мл
20 мл
30 мл
50 мл
100 мл
120 мл
150 мл
Не знайдено
Поширені запитання
Які бренди товарів Противірусні препарати для дітей найпопулярніші?
Які найдешевші товари категорії Противірусні препарати для дітей?
Найпопулярніші товари категорії Противірусні препарати для дітей?
Яка ціна на Противірусні препарати для дітей?
Вартість всіх товарів категорії Противірусні препарати для дітей варіюється від 75,00 ₴ до 1 672,00 ₴.
Повідомлення
Facebook messenger TelegramЗворотний дзвінок
Онлайн чат
Як вам зручніше з нами звʹязатися?
Скасувати
Кнопка зв’язку
классификация, механизм действия, эффективность, применение
Если с подавляющим большинством бактериальных инфекций современная медицина научилась бороться, то с вирусными заболеваниями ситуация другая — многие из них приходится лечить симптоматически. Расскажем, какие противовирусные препараты эффективны в лечении ОРВИ, как они действуют, и в каких случаях стоит применять эти лекарства.
Что такое противовирусные препараты
Вирусное заболевание — сложная задача для медикаментозной терапии. Дело в том, что вирус может жить и воспроизводиться только внутри клетки хозяина, изменяя ее обменные процессы. Поэтому долгое время считалось, что невозможно воздействовать на вирусы, не нанося существенного вреда организму.
Со временем эту гипотезу пересмотрели. Со второй половины прошлого века ученые разрабатывают противовирусные препараты, которые действуют на разные этапы жизненного цикла вируса — препятствуют прикреплению вируса к клетке, проникновению внутрь и выходу зрелых вирусных частиц из клетки, нарушают воспроизведение (репликацию).
Действие этих лекарств в терапевтической дозе губительно для вируса и практически безопасно для организма.
Классификация противовирусных препаратов
Все лекарства против вирусов разделяют на следующие группы1:
● Препараты с прямым противовирусным действием. Имеют строго определенную точку приложения и подавляют размножение определенного типа вируса на разных этапах.
● Интерфероны. Это белковые соединения, которые вырабатываются иммунными клетками в ответ на вторжение вируса. Они также подавляют активность вирусов, за счет изменения ряда процессов внутри клетки.
● Индукторы интерферонов. Это препараты, стимулирующие синтез собственных защитных противовирусных веществ.
Это препараты, стимулирующие синтез собственных защитных противовирусных веществ.
● Иммуномодуляторы. Препараты, воздействующие на различные звенья иммунной защиты, их используют только в комплексе с другими противовирусными препаратами.
По способу введения перечисленные препараты делятся на системные и местные. Первые действуют на все органы и системы, вторые — локально, в области нанесения. Местные препараты, как правило, имеют более высокую концентрацию активного вещества, работают более эффективно, но в пределах ограниченного поверхностного очага инфекции.
Остановимся подробнее на противовирусных средствах перечисленных классов, которые применяют при ОРВИ. Многие из них не только лечат, но и предотвращают развитие инфекции.
Препараты с прямым противовирусным действием
Блокаторы М2-каналов
2
К этому классу относится первый препарат, разработанный ещё в прошлом веке для химиотерапии гриппа — амантадин. Исследования, проведённые согласно принципам доказательной медицины, подтвердили его эффективность против гриппозных вирусов типа A. В нашей стране амантадин не применяют в лечении гриппа. Советские учёные создали на его основе новое средство — римантадин. Этот препарат обладает более высокой противовирусной активностью и относительно меньшей токсичностью.
Исследования, проведённые согласно принципам доказательной медицины, подтвердили его эффективность против гриппозных вирусов типа A. В нашей стране амантадин не применяют в лечении гриппа. Советские учёные создали на его основе новое средство — римантадин. Этот препарат обладает более высокой противовирусной активностью и относительно меньшей токсичностью.
Принцип действия. Лекарство принимают внутрь — в виде таблеток, сиропа. Он проникает в кровь, а потом разносится по организму и накапливается в секрете носовой полости. Активное вещество связывает белки M2. Это своеобразный «ключ» в оболочке вируса, который открывает ему «дверь» к клеточному ядру через ионные каналы в ее мембране. Вирус проникает внутрь клетки, но препарат блокирует доступ генетического материала вируса к ДНК клетки. Без этого микроорганизм не может воспроизводиться, поэтому концентрация вирусов в организме не увеличивается. Кроме этого, лекарство обладает антитоксическим действием.
Применение.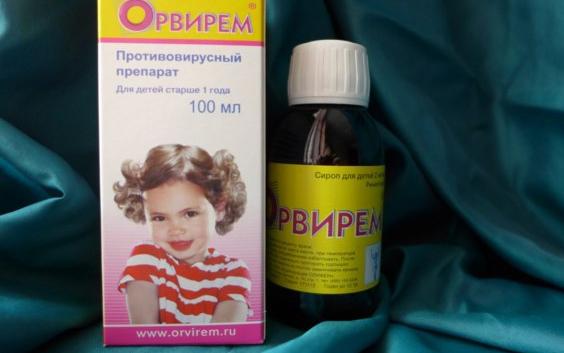 Чтобы лекарство дало хороший лечебный эффект, таблетки начинают пить не позднее двух дней с появления первых симптомов гриппа. Их принимают дважды в сутки в течение пяти дней. Детям в возрасте 1–14 лет дают детский сироп.
Чтобы лекарство дало хороший лечебный эффект, таблетки начинают пить не позднее двух дней с появления первых симптомов гриппа. Их принимают дважды в сутки в течение пяти дней. Детям в возрасте 1–14 лет дают детский сироп.
Противопоказания:
● гиперчувствительность к активным и вспомогательным компонентам лекарства;
● острые печеночные патологии;
● острое повреждение и хроническая болезнь почек;
● гиперфункция щитовидной железы;
● беременность и грудное вскармливание;
● возраст до года.
Побочные эффекты. Амантадин нередко вызывает ряд негативных побочных реакций:
● раздражительность;
● ослабление концентрации внимания;
● нарушение сна;
● снижение аппетита;
● тошноту.
Токсическое воздействие на центральную нервную систему усиливается у пожилых людей, одновременно получающих антигистаминные средства, холиноблокаторы (лекарства, контролирующие бронхиальную астму, болезнь Паркинсона, купирующие рвоту, применяющиеся в лечении хронической обструктивной болезни лёгких).
Ингибиторы нейраминидазы
3К ним относится занамивир (ныне не применяется в России) и осельтамивир. Оба типа противовирусных препаратов имеют сходный механизм действия и показания, эффективны против вирусов гриппа A и B. По сравнению с предыдущей группой не так токсичны, имеют ряд противопоказаний.
Принцип действия. Нейраминидаза — один из основных ферментов, ответственных за репликацию вирусов гриппа обоих типов. Блокируя его, лекарство на время замедляет распространение инфекции по организму. Препарат принимают внутрь. Хорошо взаимодействует с другими лекарственными препаратами, часто используется в составе комплексной терапии.
Применение. Таблетки (суспензию, приготовленную из порошка) рекомендуется пить с первых симптомов инфекции — не позднее 48 часов с начальных проявлений, иначе применение ингибиторов нейраминидазы нецелесообразно. Лекарство принимают в течение 5 суток по 2 раза в день.
Лекарство принимают в течение 5 суток по 2 раза в день.
Противопоказания:
● индивидуальная непереносимость любых компонентов лекарственной формы;
● выраженная почечная и печеночная недостаточность;
● возраст до года.
Побочные эффекты. Чаще всего (в 10–12% случаев) больные жалуются на тошноту и рвоту после первого приема лекарства. Среди других побочных реакций (у 1–2,5% пациентов):
● головные боли;
● головокружение;
● слабость;
● бессонница;
● ощущение заложенности носа;
● кашель;
● боль в горле.
Ингибиторы гемагглютинина
4, 5
В России группу ингибиторов представляет давний отечественный препарат умифеновир, который действуют против вирусов типа A и B, ряда прочих возбудителей ОРВИ. Однако исследование российских и британских ученых показало, что есть возможность мутаций, приводящих к появлению резистентных к умифеновиру штаммов вирусов. Устойчивость обусловливалась неспособностью умифеновира связываться с мутировавшим гемагглютинином.6 Сходный по спектру действием другой препарат — энисамия йодид. По этому препарату заявлена высокая эффективность и хорошая переносимость, отсутствие резистентных штаммов.
Устойчивость обусловливалась неспособностью умифеновира связываться с мутировавшим гемагглютинином.6 Сходный по спектру действием другой препарат — энисамия йодид. По этому препарату заявлена высокая эффективность и хорошая переносимость, отсутствие резистентных штаммов.
Принцип действия. Препараты действуют на гемагглютинин вируса — белок, который обеспечивает слияние его генетического материала с клеточной ДНК. Ингибиторы гемагглютинина блокируют заражение уже на начальной стадии, предотвращая проникновение вирусной частицы в клетку.
Кроме основного, оба лекарства обладают дополнительными эффектами в борьбе с вирусом: стимулируют синтез интерферонов, повышают устойчивость организма к инфекции. Особенно выражены эти свойства у энисамия йодида. Препарат быстро всасывается после приема внутрь и долго (до 14 часов) циркулирует в крови, препятствуя распространению вирусной инфекции по организму.
Применение. Препараты применяются в лечении гриппа и других ОРВИ. Умифеновир принимают внутрь в форме капсул, таблеток, порошка для приготовления суспензии. Дозу и интервал, длительность приёма лекарства индивидуально устанавливает лечащий врач. Энисамия йодид врачи назначают в таблетках, покрытых пленочной оболочкой, которые нужно принимать внутрь по три раза в день в течение 5–7 суток.
Умифеновир принимают внутрь в форме капсул, таблеток, порошка для приготовления суспензии. Дозу и интервал, длительность приёма лекарства индивидуально устанавливает лечащий врач. Энисамия йодид врачи назначают в таблетках, покрытых пленочной оболочкой, которые нужно принимать внутрь по три раза в день в течение 5–7 суток.
В исследовании, проведенном Иллинойским технологическим институтом, США в 2018 г. доказано, что введение энисамия йодида в течение 4 ч. приводит к 100-кратному снижению концентрации вируса в клетках бронхов человека.
Противопоказания:
● повышенная чувствительность к компонентам;
● беременность (умифеновир можно с осторожностью применять со второго триместра) и грудное вскармливание;
● возраст: применение умифеновира разрешено с 6, энисамия йодида — с 12 лет.
Кроме того, энисамия йодид не применяют при склонности к аллергическим реакциям, тяжелых почечных и печеночных патологиях.
Побочные эффекты. Крайне редко (менее одного случая на тысячу) умифеновир может вызвать аллергию — зуд, кожные высыпания, ангионевротический отек, а в тяжелых случаях — анафилактический шок. Другие побочные эффекты не отмечались.
Энисамия йодид, как правило, хорошо переносится. В некоторых случаях его прием могут сопровождать следующие нежелательные явления:
● аллергические — зуд, сыпь на коже, ангионевротический отек;
● неприятный привкус, отек слизистых полости рта, повышенное слюноотделение;
● желудочно-кишечные — изжога, вздутие живота, тошнота и рвота;
● боль в горле, одышка.
Интерфероны
Для лечения гриппа (в том числе «птичьего») и других вирусных респираторных инфекций иногда используются препараты интерферона: лейкоцитарного человеческого (смеси подтипов альфа) и рекомбинантных (полученных с использованием бактерий) — альфа-2b и гамма.
Принцип действия. Интерферон альфа-2b обладает противовирусным и иммуномодулирующим действием. В интактных клетках (не подвергшихся заражению вирусом) он препятствует попаданию вируса внутрь клетки, а в инфицированных клетках интерферон альфа-2b запускает систему запрограммированной смерти клетки – апоптоз, в результате чего вирус гибнет вместе с клеткой. Препарат также повышает активность иммунной системы, усиливает фагоцитоз и цитотоксический эффект лимфоцитов — защиту, направленную на устранение зараженных клеток. Интерферон гамма — мощный иммуномодулятор. Его основное действие — активация клеток, ответственных за формирование специфического иммунитета к первичной вирусной инфекции и подавление вторичной бактериальной.
Применение. Оба типа интерферона применяют при гриппе и ОРВИ в виде капель в нос. Препарат капают по 2–3 капли 5–6 раз в день. Лечение начинают как можно раньше – до истечения трех суток с момента появления симптомов, в противном случае применение будет иметь профилактический эффект. Интерферон-гамма также применяют в период выздоровления — в течение недели.
Интерферон-гамма также применяют в период выздоровления — в течение недели.
Интерферон гамма не применяют при гиперчувствительности к препарату, беременности и в возрасте до семи лет.
Индукторы интерферона
В перечень индукторов интерферона, которые Министерство здравоохранения РФ рекомендует применять в лечении ОРВИ, входят меглюмина акридонацетат, тилорон, риамиловир, имидазолилэтанамид пентандиовой кислоты и др.
Принцип действия. Все препараты обладают схожим эффектом — способствуют выработке собственных интерферонов различных типов, которые действуют универсально, против многих разновидностей вирусов.
Применение. Препараты применяют при ОРВИ с лечебной и профилактической целью. Режим дозирования устанавливает врач индивидуально для каждого пациента. Общие для большинства индукторов интерферона противопоказания:
● беременность;
● кормление грудью;
● индивидуальная непереносимость.
● детский возраст (ограничения варьируются в зависимости от действующего вещества).
Побочные эффекты. Наиболее распространённое нежелательное действие – возникновение аллергической реакции.
Какие противовирусные препараты лучше при лечении ОРВИ
Что касается ОРВИ и гриппа, оценить эффективность противовирусных препаратов в их терапии с точки зрения доказательной медицины поможет таблица. Справа представлены показатели:
● Уровень убедительности рекомендаций (УУР) — от A (наиболее убедительных) до C.
● Уровень достоверности доказательств (УДД), приведенных рекомендаций, где 5 — высший балл.
Таблица 1. Рекомендации Минздрава РФ по применению противовирусных средств разных классов в лечении ОРВИ и гриппа.10, 11
Лекарство |
УУР (УДД) при гриппе |
УУР (УДД) при ОРВИ |
Препараты с прямым противовирусным действием |
||
Ингибиторы нейраминидазы |
A (1) |
Не применяются |
Блокаторы М2-каналов – не рекомендуются при гриппе ввиду роста резистентных штаммов |
A (2) |
|
Умифеновир |
A (1) |
C (2) |
Энисамия йодид |
B (2) |
C (2) |
Интерфероны |
||
Альфа-2b или гамма |
B (3) |
C (5) |
Индукторы интерферонов |
||
Имидазолилэтанамид пентандиовой кислоты |
B (2) |
C (2) |
Эргоферон |
B (2) |
C (2) |
Риамиловир |
B (3) |
C (1) |
Кагоцел |
B (3) |
C (3) |
Тилорон |
B (3) |
C (3) |
Меглюмина акридонацетат |
Не применяется |
B (1) |
Низкие баллы не всегда означают слабую эффективность препарата — возможно, с ним были проведены не все необходимые исследования.
Противовирусные средства для профилактики
Многие препараты, перечисленные выше, эффективны и для предупреждения ОРВИ — экстренной профилактики (после контакта с больным) и сезонной. Профилактический прием препаратов в период вспышки инфекции особенно необходим людям со сниженным иммунитетом — пожилым, страдающим хроническими заболеваниями. Если прием противовирусных препаратов не поможет предотвратить заболевание, он может облегчить его течение. Стоит помнить, что применение противогриппозных средств с целью профилактики по эффективности не заменяет вакцинацию.
Коротко о главном
➢ Противовирусные препараты — лекарства, которые прямо или косвенно воздействуют на вирус.
➢ Наиболее эффективны препараты с прямым противовирусным действием — они влияют непосредственно на вирус, его активность, но существуют далеко не для всех инфекций.
➢ Неспецифические противовирусные средства — интерфероны и их индукторы — помогают иммунной системе победить вирус и могут использоваться в лечении целого ряда различных инфекций.
➢ Прием некоторых противовирусных позволяет предупредить заболевание (или облегчить его течение).
1 Шестакова И.В. Противовирусные препараты // Журнал для непрерывного медицинского образования врачей – https://cyberleninka.ru/article/n/protivovirusnye-preparaty/pdf
2 Хатхоху М.Г. Противовирусные препараты: учебное пособие // Майкопский государственный технологический университет – 2014 – https://mkgtu.ru/sveden/files/Farmakologiya._Uchebno-metodicheskoe_posobie._Protivovirusnye_sredstva.pdf
3 Хатхоху М.Г. Противовирусные препараты: учебное пособие // Майкопский государственный технологический университет – 2014 – https://mkgtu.ru/sveden/files/Farmakologiya._Uchebno-metodicheskoe_posobie._Protivovirusnye_sredstva.pdf
4 Ленева И.А., Пшеничная Н.Ю., Булгакова В.А. Умифеновир и коронавирусные инфекции: обзор результатов исследований и опыта применения в клинической практике // Терапевтический архив – №11, 2020 – https://cyberleninka. ru/article/n/umifenovir-i-koronavirusnye-infektsii-obzor-rezultatov-issledovaniy-i-opyta-primeneniya-v-klinicheskoy-praktike/pdf
ru/article/n/umifenovir-i-koronavirusnye-infektsii-obzor-rezultatov-issledovaniy-i-opyta-primeneniya-v-klinicheskoy-praktike/pdf
5 Возможности этиотропной терапии в снижении рисков развития тяжелого или осложненного течения ОРВИ и гриппа / Паевская Е.А [и другие авторы] // РМЖ – Т.27, №1-2, 2019.
6 Irina A Leneva, Rupert J Russell, Yury S Boriskin, Alan J Hay. Characteristics of arbidol-resistant mutants of influenza virus: implications for the mechanism of anti-influenza action of arbidol. Antiviral Res. 2009 Feb;81(2):132-40. doi: 10.1016/j.antiviral.2008.10.009. Epub 2008 Nov 24.
7 Boltz D, et al. Activity of enisamium, an isonicotinic acid derivative, against influenza viruses in differentiated normal human bronchial epithelial cells. Antivir Chem Chemother. 2018.
8 Инструкция по медицинскому применению (Нобазит® таблетки, покрытые пленочной оболочкой 250 мг; РУ: ЛП-003508 от 16.03.2016)
9 Лиознов Д. А., Карнаухова Е.Ю., Зубкова Т.Г., Шахланская Е.В., Оценка эффективности схемы лечения ОРВИ, включающей этиотропную (энисамия йодид) и симптоматическую терапию // Терапевтический архив №3 – 2020 г.
А., Карнаухова Е.Ю., Зубкова Т.Г., Шахланская Е.В., Оценка эффективности схемы лечения ОРВИ, включающей этиотропную (энисамия йодид) и симптоматическую терапию // Терапевтический архив №3 – 2020 г.
10 Острые респираторные вирусные инфекции (ОРВИ) у взрослых: клинические рекомендации – https://apicr.minzdrav.gov.ru/api.ashx?op=GetClinrecPdf&id=724_1
11 Грипп у взрослых: клинические рекомендации – https://www.rnmot.ru/public/uploads/RNMOT/clinical/2021/%D0%9A%D0%A0%20%D0%B3%D1%80%D0%B8%D0%BF%D0%BF.pdf
О препарате Скачать инструкцию
рейтинг топ-10 средств по версии КП
Многие люди склонны недооценивать всю серьезность вирусов: они продолжают ходить на работу, ездить на общественном транспорте и не заморачиваются с лечением, делая тем самым хуже себе и подвергая риску заражения других. ОРВИ длится обычно 3-4 дня, и лечение нужно начинать с первого дня заболевания, иначе можно заработать осложнения.
Взрослый человек в среднем болеет простудой 2-3 раза в год! Классические признаки ОРВИ: чихание, слезотечение, головная боль, заложенность носа, выделения из носа (насморк), боли в горле и пазухах носа, повышенная температура, озноб, боли в суставах и мышцах1.
Рейтинг топ-10 противовирусных препаратов по версии КП
При ОРВИ в организм вторгаются вирусы, поэтому, чтобы снова встать на ноги, нужно лечиться противовирусными препаратами. Все средства, которые могут помочь при вирусах, делятся на три группы:
- интерфероны,
- синтетические средства,
- препараты растительного происхождения.
Публикуем список недорогих и эффективных средств по версии КП.
1. Арбидол Максимум
Арбидол. Фото: Фармстандарт-ЛексредстваВозглавляет рейтинг препарат «Арбидол Максимум», который зарекомендовал себя на рынке как эффективное средство от ОРВИ и гриппа. В его составе моногидрат умифеновира гидрохлорида – он подавляет вирусы и возбудители ОРВИ2. Помимо противовирусного эффекта «Арбидол Максимум» обладает еще и умеренным иммуномодулирующим действием.
Производитель заявляет, что «Арбидол Максимум» облегчает течение болезни и снижает возможный риск осложнений.
Противопоказан при чувствительности к компонентам препарата, а также детям до 12 лет, женщинам в первом триместре беременности и в период кормления.
2. Кагоцел
Кагоцел. Фото: НиармедикАктивное вещество этого препарата – натриевая соль сополимера. Она образует в организме поздние интерфероны, они же принимают участие в борьбе с вирусами. Большой плюс этого средства в том, что его можно применять и взрослым, и детям от трех лет. Он зарекомендовал себя как препарат, борющийся не только с ОРВИ, но и с гриппом. Также производитель отмечает, что в сочетании с антибиотиками «Кагоцел» усилит их эффективность. Его нельзя принимать во время беременности и в период лактации.
3. Лавомакс
Лавомакс. Фото: НижфармЭтот препарат содержит в составе тилорон, а он способствует синтезу интерферонов. «Лавомакс» обладает также иммуномодулирующим действием и не дает развиваться патогенным клеткам в организме. Препарат активно применяют при ОРВИ, ОРЗ и даже остром гепатите. Используют его и при гриппе – он подавляет репродуктивную функцию вирусов.
Противопоказан при повышенной чувствительности к тилорону и другим компонентам, беременным и кормящим женщинам, а также детям до 18 лет.
4. Эргоферон
Эргоферон. Фото: Материа МедикаУ «Эргоферона» высокая фармакологическая активность: он работает как противовирусный, иммуномодулирующий, антигистаминный и привовоспалительный препарат. «Эргоферон» не только борется с вирусами, но и является профилактическим препаратом при ОРВИ и гриппе – его можно применять в период, когда все вокруг болеют.
Средство противопоказано детям до 6 месяцев, а во время беременности и лактации его можно использовать, если врач полагает, что от препарата будет больше пользы, нежели вреда.
5. Гриппферон
Гриппферон. Фото: Фирн М«Гриппферон» рекомендуется применять для лечения вирусных заболеваний, в том числе и гриппа. Этот препарат относят к интерферонам, а, как многим известно, выработка интерферонов – это отличная защита от вирусов. Интерфероны действуют таким образом, что здоровые клетки нашего организма становятся невосприимчивы к вирусам, создавая некую оборону, поэтому, если в организм и попадет зараза, иммунитет активизируется и не даст ей распространиться. Используется «Гриппферон» также как средство для профилактики простуды и гриппа.
Используется «Гриппферон» также как средство для профилактики простуды и гриппа.
Противопоказан он при индивидуальной непереносимости компонентов, а также при тяжелых формах аллергических заболеваний.
6. Римантадин Актитаб
Римантадин Актитаб. Фото: Оболенское фармацевтическое предприятиеЭто популярный и недорогой препарат на рынке лекарств. «Римантадин Актитаб» лечит вирусы и грипп, а также активно применяется как профилактическое средство, если вдруг вы контактировали с болеющим человеком.
Один важный момент – у этого на первый взгляд безобидного лекарства очень много побочных эффектов — вплоть до астмы и аллергической сыпи. Зато противопоказаний у него немного: гиперчувствительность к лекарствам класса адамантана, включая римантадин и амантадин.
7. Циклоферон
Циклоферон. Фото: Полисан«Циклоферон» известен тем, что подавляет вирусы на ранних сроках. Если начать лечение сразу при заражении, то можно встать на ноги уже в течение двух-пяти дней.
В его составе имеется меглюмина акридонацетат, который представляет собой индуктор синтеза интерферонов. «Циклоферон» эффективен при ОРВИ, ОРЗ и гриппе. Работает как противовоспалительный, иммуномодулирующий и противовирусный препарат.
«Циклоферон» эффективен при ОРВИ, ОРЗ и гриппе. Работает как противовоспалительный, иммуномодулирующий и противовирусный препарат.
Его не рекомендуется применять при циррозе печени, беременности, в период грудного вскармливания. Противопоказан препарат и детям до 4 лет.
8. Ингарон
Ингарон. Фото: ФармаклонПрепарат тоже относится к интерферонам – в его составе интерферон гамма, который способствует активизации внутриклеточного иммунитета. Вирус подавляется в короткие сроки, кроме того, средство помогает избежать осложнений. «Ингарон» не накапливается в организме и полностью выводится из него в течение 24 часов после приема.
У этого средства немного противопоказаний, его нельзя принимать только беременным женщинам и тем, у кого есть непереносимость какого-либо компонента препарата.
9. Тамифлю
Тамифлю. Фото: F.Hoffmann-La RocheАктивное вещество препарата «Тамифлю» — осельтамивира фосфат. Он эффективен против вирусов гриппа типа А и В. Средство не дает патогенам проникать в клетки дыхательных путей, из-за чего вирус не может распространиться по организму.
Противопоказан «Тамифлю» при повышенной чувствительности к препарату или его составляющим, при тяжелой почечной недостаточности, а также детям младше одного года.
10. Триазавирин
Триазаверин. Фото: МедсинтезЭтот препарат разработан на основе синтетического аналога пуриновых нуклеозидов4. Он является эффективным средством против РНК-содержащих вирусов. В лечении он выступает в роли ингибитора РНК, разрушает вирусы в организме, либо не дает им прорваться, если речь идет о профилактике.
Употреблять «Триазавирин» следует с осторожностью и только после прочтения инструкции или консультации с врачом. Дело в том, что существует вероятность передозировки, а отсюда тошнота, рвота, головные боли. Противопоказан он беременным и кормящим женщинам, детям до 18 лет, а также людям с почечной и печеночной недостаточностью.
Как выбрать противовирусные препараты
При выборе препарата нужно ориентироваться на следующие параметры:
- минимум побочных эффектов;
- отсутствие токсичности;
- возможность сочетания препарата с другими (если вы принимаете какие-то средства).

Источники
- Лиясова Д.Б. Лечение острой респираторной инфекции в амбулаторных условиях // West Kazakhstan Medical Journal. 2010. №2 (26). https://cyberleninka.ru/article/n/lechenie-ostroy-respiratornoy-infektsii-v-ambulatornyh-usloviyah
- Инструкция по медицинскому применению препарата Арбидол® от 5.04.2019
- Караулов А.В. и др. Применение иммуномодулятора ИРС®19 при рецидивирующих респираторных заболеваниях // Русский Медицинский Журнал, том 8, №13-14, 2000.
- Инструкция по медицинскому применению препарата Тонзилгон® Н таблетки покрытые оболочкой от 29.12.11
Эргоферон. Эргоферон инструкция по применению, цена.
Препарат Эргоферон выпускается в удобной лекарственной форме — таблетки для рассасывания или раствор для приема внутрь.
Эргоферонобладает несколькими лечебными эффектами. Первое, самое важное — противовирусное действие. Второй не менее важный эффект препарата — иммуномодулирующий. Средство мобилизует защитные силы организма для более слаженной и быстрой борьбы с инфекцией, в том числе за счет активного распознавания возбудителя и адекватного иммунного ответа на его вторжение.
Благодаря противовоспалительному и антигистаминному эффектам Эргоферонспособствует уменьшению выраженности и продолжительности отека слизистых оболочек, бронхоспазма и кашля.
Может применяться для лечения гриппа и ОРВИ у всех членов семьи — взрослых и детей начиная с 6-месячного возраста.
Лекарственная форма, состав, описание
Регистрационный номер
ЛП-N (000031) — (РГ-RU)
Торговое название
Эргоферон
Лекарственная форма
Таблетки для рассасывания.
Cостав (на 1 таблетку)
Действующие вещества:
антитела к гамма интерферону человека аффинно очищенные — 0,006 г*
антитела к гистамину аффинно очищенные — 0,006 г*
антитела к CD4 аффинно очищенные — 0,006 г*
Вспомогательные вещества: лактозы моногидрат 0,267 г, целлюлоза микрокристаллическая 0,03 г, магния стеарат 0,003 г.
* наносятся на лактозы моногидрат в виде смеси трех активных водно-спиртовых разведении субстанции, разведенной соответственно в 10012, 10030, 10050 раз.
Описание
Таблетки плоскоцилиндрической формы с риской и фаской, от белого до почти белого цвета. На плоской стороне с риской нанесена надпись MATERIA MEDICA, на другой плоской стороне нанесена надпись ERGOFERON.
Фармакотерапевтическая группа
Противовирусное и иммуностимулирующее средство.
Коды АТХ
Фармакодинамика
Спектр фармакологической активности Эргоферона включает в себя противовирусную, иммуномодулирующую, антигистаминную, противовоспалительную.
Компоненты, входящие в препарат, обладают единым механизмом действия в виде повышения функциональной активности CD4 рецептора, рецепторов к интерферону гамма (ИФН-γ) и гистамину, соответственно; что сопровождается выраженным иммунотропным действием.
Экспериментально доказано, что антитела к интерферону гамма: повышают экспрессию ИФН-γ, ИФН а/β, а также сопряженных с ними интерлейкинов (ИЛ-2, ИЛ-4, ИЛ-10 и др.), улучшают лиганд-рецепторное взаимодействие ИФН, восстанавливают цитокиновый статус; нормализуют концентрацию и функциональную активность естественных антител к ИФН-γ, являющихся важным фактором естественной противовирусной толерантности организма; стимулируют интерферонозависимые биологические процессы: индукцию экспрессии антигенов главного комплекса гистосовместимости I, II типов и Fc- рецепторов, активацию моноцитов, стимуляцию функциональной активности NK- клеток, регуляцию синтеза иммуноглобулинов, активируя смешанный Тh2 и Тh3 иммунный ответ.
Антитела к СD4, вероятно являясь аллостерическими модуляторами данного рецептора, регулируют функциональную активность CD4 рецептора, что приводит к повышению функциональной активности CD4 лимфоцитов, нормализации иммунорегуляторного индекса CD4/CD8, а также субпопуляционного состава иммунокомпетентных клеток (CD3, CD4, CD8, CD16, CD20).
Антитела к гистамину модифицируют гистамин-зависимую активацию периферических и центральных h2-рецепторов и, таким образом, снижают тонус гладкой мускулатуры бронхов, уменьшают проницаемость капилляров, что приводит к сокращению длительности и выраженности ринореи, отека слизистой оболочки носа, кашля и чихания, а также уменьшению выраженности сопутствующих инфекционному процессу аллергических реакций за счет подавления высвобождения гистамина из тучных клеток и базофилов, продукции лейкотриенов, синтеза молекул адгезии, снижения хемотаксиса эозинофилов и агрегации тромбоцитов в реакциях на контакт с аллергеном.
Совместное применение компонентов комплексного препарата сопровождается усилением противовирусной активности входящих в него компонентов.
Фармакокинетика
Чувствительность современных физико-химических методов анализа (газожидкостная хроматография, высокоэффективная жидкостная хроматография, хромато-масс-спектрометрия) не позволяет оценивать содержание действующих веществ препарата Эргоферон в биологических жидкостях, органах и тканях, что делает технически невозможным изучение фармакокинетики.
Показания к применению
Эргоферон показан к применению у взрослых и детей в возрасте от 6 месяцев.
Лечение гриппа и острых респираторных вирусных инфекций (ОРВИ).
Лечение острых кишечных инфекций вирусной этиологии.
Противопоказания
Повышенная индивидуальная чувствительность к компонентам препарата.
Дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция.
Детский возраст до 6 месяцев.
Применение при беременности и в период грудного вскармливания
Безопасность применения препарата Эргоферон у беременных не изучалась.
При беременности и в период лактации препарат применяют только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода и ребенка. Соотношение «польза-риск» определяется лечащим врачом.
Способ применения и дозы
Риска не предназначена для деления таблетки на части.
Внутрь, не во время приема пищи. Таблетку следует держать во рту, не проглатывая, до полного растворения.
При назначении препарата детям младшего возраста (от 6 месяцев до 3 лет) рекомендуется растворять таблетку в небольшом количестве (1 столовая ложка) кипяченой воды комнатной температуры.
Взрослым и детям с 6 месяцев. В 1-й день лечения принимают 8 таблеток по следующей схеме: по 1 таблетке каждые 30 минут в первые 2 часа (всего 5 таблеток за 2 часа), затем в течение этого же дня принимают еще по 1 таблетке 3 раза через равные промежутки времени. На 2-ой день и далее принимают по 1 таблетке 3 раза в день до полного выздоровления.
При необходимости препарат можно сочетать с другими противовирусными и симптоматическими средствами.
Побочное действие
Возможны реакции повышенной индивидуальной чувствительности к компонентам препарата.
Передозировка
При случайной передозировке возможны диспепсические явления, обусловленные входящими в состав препарата наполнителями.
Взаимодействие с другими лекарственными средствами
Случаев несовместимости с другими лекарственными средствами до настоящего времени не зарегистрировано.
Особые указания
В состав препарата входит лактозы моногидрат, в связи с чем его не рекомендуется назначать пациентам с врожденной галактоземией, синдромом мальабсорбции глюкозы или галактозы, либо при врожденной лактазной недостаточности.
Влияние на способность управлять транспортными средствами, механизмами
Эргоферон не оказывает влияния на способность управлять транспортными средствами и другими потенциально опасными механизмами.
Форма выпуска
Таблетки для рассасывания. По 20 таблеток в контурной ячейковой упаковке из пленки поливинилхлоридной и фольги алюминиевой.
По 1, 2 или 5 контурных ячейковых упаковок вместе с инструкцией по медицинскому применению помещают в пачку из картона.
Условия хранения
В защищенном от света месте, при температуре не выше 25°С.
Хранить в недоступном для детей месте.
Срок хранения
3 года.
Не применять по истечении срока годности.
Условия отпуска из аптек
Без рецепта.
Адрес для обращений
ООО «НПФ «МАТЕРИА МЕДИКА ХОЛДИНГ»;
Россия, 127473, г. Москва, 3-й Самотечный пер., д. 9.
Тел./факс: +7 (495) 684-43-33.
Телефоны «Горячей линии»: +7 (495) 681-09-30, +7 (495) 681-93-00.
E-mail: [email protected]
Адрес производства
Россия, 454139, г. Челябинск, ул. Бугурусланская, д. 54
СКАЧАТЬ
Купити ПРОТИВІРУСНІ препарати в Україні – Ціна від 34.00 грн.
- Товари
- Ціни
Товарів: 115
Сортування: За рейтингомВід дешевихВід дорогих
Вид:
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Огляд
Перейти до кошика
Огляд
Перейти до кошика
Перейти до кошика
Разом дешевше
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Огляд
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Огляд
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Перейти до кошика
Разом дешевше
Перейти до кошика
Перейти до кошика
Перейти до кошика
Редакторська група
Дата створення: 30. 03.2021
Дата оновлення: 16.09.2022
03.2021
Дата оновлення: 16.09.2022
Противірусні засоби: фармакокінетика й показання
Віруси – це патогенні мікроорганізми, які проникають в організм людини, вбудовуються в чутливі клітини і спричиняють захворювання. Зараження можливе через фізичні пошкодження, впорскування й через попадання інфекції на слизову. Клінічна картина залежить від типу патогена. Для лікування пацієнтам призначають противірусні препарати, що стимулюють імунну реакцію і пригнічують життєдіяльність патогенів.
У яких випадках потрібно приймати противірусне
Віруси – найчисленніша форма життя на Землі. Багато з них становлять небезпеку тільки для певних видів організмів. Людство страждає від таких вірусних захворювань:
- ГРВІ;
- герпес;
- кір;
- свинка;
- краснуха;
- вітряна віспа;
- грип;
- мононуклеоз;
- ВІЛ;
- ВПЛ;
- гепатити А, В і С.
Симптоматика в кожного стану індивідуальна. Найчастіше жителі України стикаються з застудами та ГРВІ. Часто до вірусного зараження приєднується вторинна інфекція, і в людини розвивається бронхіт, риніт, пневмонія.
Як працюють противірусні
Віруси проникають у клітину і використовують її ресурс для розмноження й подальшого інфікування. Складність лікування полягає в тому, що точкове знищення патогена можливе тільки з хазяйською клітиною.
Звичайні імуностимулятори бувають безсилі, оскільки віруси мають здатність до латентності. Противірусні препарати ефективні, оскільки спрацьовують у певний життєвий цикл і запускають складні хімічні реакції, що пригнічують патогени на конкретному етапі розвитку.
Різновиди препаратів:
- З опосередкованою дією. Ліки цього типу стимулюють імунну систему на вироблення антитіл. Якщо організм пацієнта виснажений, препарат може не спрацювати.
- З прямою дією. Медикамент впливає на суб’єкт інфікування.
 Одні ліки перешкоджають пересуванню вірусу до місця розмноження, інші блокують процес, треті – результат копій з ураженої клітини.
Одні ліки перешкоджають пересуванню вірусу до місця розмноження, інші блокують процес, треті – результат копій з ураженої клітини.
Обидва типи ліків сприяють зниженню інтоксикації і зменшують ймовірність ускладнень.
Форми випуску
Фармацевтичні компанії пропонують широкий вибір препаратів із різними діючими речовинами і зручною формою випуску. Це можуть бути:
- таблетки;
- капсули;
- порошок для розчину інфузій;
- порошок для оральної суспензії;
- рідина для перорального застосування;
- сироп;
- гелі, креми, мазі;
- спрей;
- свічки;
- краплі.
Противірусні препарати приймають за призначенням лікаря. Профільний фахівець визначає дозування і прийнятну лікарську форму.
Протипоказання до вживання
Найчастішим протипоказанням є індивідуальна непереносимість діючої речовини й допоміжних компонентів. Решта залежать від типу захворювання, тому перед покупкою варто ознайомитися з інструкцією. Також є низка обмежень для жінок у періоди вагітності та лактації й дітей до 3-х років.
Також є низка обмежень для жінок у періоди вагітності та лактації й дітей до 3-х років.
Вживання противірусних препаратів пом’якшує симптоматику і прискорює одужання. Деякі з них мають профілактичні властивості. За допомогою МІС Аптека 9-1-1 можна замовити будь-які ліки з адресною доставкою за доступною ціною.
Список використаної літератури
- Компендіум — лікарські препарати;
- Державний реєстр лікарських засобів;
- GoodRX.
Популярні питання про противірусні препарати
Як працюють противірусні препарати?
Дія спрямована на пригнічення життєдіяльності патогенів у конкретний цикл розвитку: потрапляння в клітину, створення копій генетичного матеріалу, вихід із клітини.
Які противірусні можна вагітним?
Вагітні жінки можуть користуватися препаратами із зовнішнім застосуванням. З другого триместру допускається застосування засобів із групи інтерферонів.
Яке противірусне краще для дітей?
Малюкам з 1-го року рекомендовані засоби на основі інозину, випущені у формі сиропів. Оскільки імунна система дитини тільки формується, будь-які втручання можливі тільки під контролем педіатра.
Оскільки імунна система дитини тільки формується, будь-які втручання можливі тільки під контролем педіатра.
Які противірусні найкращі?
Найкращі ліки – ті, які вам призначив лікар на основі клінічної картини. У безвихідній ситуації вибирайте ті, у яких мінімум протипоказань і побічних ефектів.
Поширені запитання
Які недорогі товари в категорії Противірусні препарати?
Які імпортні товари є в категорії Противірусні препарати?
Які найпопулярніші товари в категорії Противірусні препарати?
Скільки коштують товари в категорії Противірусні препарати?
Ціни на товари в категорії Противірусні препарати починаються від 34.00 грн.
Противірусні препарати ціна в Аптеці 911
| Назва | Ціна |
|---|---|
Новірин табл. 500мг №40 500мг №40 | 223.67 грн. |
| Римантадин табл. 50мг №20 | 79.00 грн. |
| Ацикловір-Дарниця табл. 200мг №20 | 70.96 грн. |
| Герпевір табл. 400мг №10 | 78.12 грн. |
| Герпевір мазь 2.5% туба 5г | 72.92 грн. |
Кипферон
Когда Мама молодец!
Кипферон® — двойная защита малыша от бактериальных осложнений!1,2
Где купить Узнать подробнее
Уникальный состав
1Содержит интерферон — защита от вирусов, и КИП — готовые антитела от вирусов и бактерий
На любой стадии ОРВИ
1Благодаря уникальному КИП, может применяться на любой стадии ОРВИ*1
Для детей с рождения
1Разрешен к применению малышам с первых дней жизни и будущим мамам
Сравнение интерфероновых суппозиториев по критичным характеристикам
Другие интерфероновые свечи
Другие интерфероновые свечи
Защита клеток от вирусов
противовирусная активность
Прямое воздействие
на саму причину ОРВИ
обезвреживание и выведение вирусов и бактерий из организма.
Обладает прямой противовирусной и антибактериальной активностью за счет КИП1
Не обладает прямой противовирусной и антибактериальной активностью4
Предотвращение развития бактериальных осложнений ОРВИ за счет прямого антибактериального эффекта
Благодаря наличию
КИП1
Действие преимущественно направлено на борьбу
с вирусами4
Возможность использовать
на любой стадии ОРВИ
за счет наличия КИП
(готовых антител)1
Эффективный старт терапии — первые 48 часов от начала симптомов5
Достаточное количество интерферона даже для детей с низкой чувствительностью к интерферону
500 тыс. МЕ1
150 тыс. МЕ4
Двойная защита малыша от бактериальных осложнений ОРВИ
1,2-
борется не только
с вирусами, но и с бактериями1 -
способствует снижению выраженности симптомов ОРВИ6
-
может использоваться
на любой стадии ОРВИ*1
- до 1 года
- 1 свеча 1 раз в день
- от 1 года до 12 лет
- 1 свеча 2 раза в день
Инструкция по применению
- Малышам до 1 года
- Детям от 1 до 12 лет
- Будущим мамам
1 свеча
1 раз в сутки
Курс приема: 5-7 дней1
1 свеча
2 раза в сутки
Курс приема: 5-7 дней1
1 свеча
3 раза в сутки
Курс приема: 5-7 дней1
Комментарии
и советы педиатров
- Запустить видео
Формирование иммунитета у детей и понятие «часто болеющие дети»
- Запустить видео
Коронавирус у детей: как защитить и что делать, если в семье кто-то заболел
- Запустить видео
Опасен ли Интерферон и зачем нужны Антитела? Помощь ребенку при ОРВИ
Часто задаваемые вопросы
Вы можете задавать любые интересующие вас вопросы по проблеме и о препарате, мы с радостью на них ответим
Почему стоит выбрать Кипферон® в составе комплексной терапии ОРВИ?Дети довольно часто болеют, ведь у них еще не полностью сформировалась иммунная система, которая бы полноценно их защищала7. Продукция интерферона значительно ниже, чем у взрослого, а тот, что вырабатывается, имеет слабый уровень защиты7.
Продукция интерферона значительно ниже, чем у взрослого, а тот, что вырабатывается, имеет слабый уровень защиты7.
Ребенку нужна помощь в борьбе с вирусами и бактериями — антивирусным действием обладает интерферон — он помогает клеткам противостоять вирусам3. Однако для направленной борьбы против бактерий его будет недостаточно. Поэтому в составе КИПферон®, кроме интерферона, содержится уникальный КИП (готовые антитела)1, который распознает, обезвреживает и выводит из организма причину заболевания — вирусы и бактерии3, снижая выраженность симптомов ОРВИ и недопуская бактериальных осложнений2.
Частые простуды — часть становления иммунной системы малыша, важно, чтобы они проходили быстрее и не перерастали в осложнения.
Какой эффект от лечения?Препарат Кипферон®, за счет комбинированного состава1, активирует сразу 2 механизма защиты человека: неспецифический — интерферон и специфический — антитела3. Препарат напрямую борется и с вирусами, и с бактериями, способствуя снижению выраженности симптомов ОРВИ: лихорадка, ринит, кашель, покраснение горла — а также защищая от бактериальных осложнений9.
Препарат напрямую борется и с вирусами, и с бактериями, способствуя снижению выраженности симптомов ОРВИ: лихорадка, ринит, кашель, покраснение горла — а также защищая от бактериальных осложнений9.
Стоит начать применение в остром периоде, как только проявились симптомы ОРВИ, однако если момент упущен, Кифперон, благодаря наличию КИП, будет помогать малышу быстрее поправиться. Более того, существует исследование, демонстрирующее, что в группе детей, принимавших помимо прочей терапии Кипферон®, эффективность лечения повысилась на 20–25%, а сроки болезни сократились на 25—35%9.
Кто производитель?Препарат Кипферон® производится российским фармацевтическим холдингом полного цикла — ГК Alium, созданной на базе АО «Фармацевтическое предприятие «Оболенское» и АО «Биннофарм». Более подробно о компании можно узнать тут:
https://is.gd/SVo4t4
Как и когда появился Кипферон®?Препарат Кипферон® был разработан в 1991 году на базе Федерального бюджетного учреждения науки «Московский научно-исследовательский институт эпидемиологии и микробиологии им. Г.Н.Габричевского» Роспотребнадзора. Ученые во главе с Владимиром Андриановичем Алёшкиным (доктор биологических наук, профессор, заслуженный деятель науки, член РАЕН и Нью-Йорской академии наук) имели широкий опыт применения интерферона. Они знали, что организм малыша не только продуцирует в разы меньше интерферона в сравнении со взрослыми, но и хуже его воспринимает.
Г.Н.Габричевского» Роспотребнадзора. Ученые во главе с Владимиром Андриановичем Алёшкиным (доктор биологических наук, профессор, заслуженный деятель науки, член РАЕН и Нью-Йорской академии наук) имели широкий опыт применения интерферона. Они знали, что организм малыша не только продуцирует в разы меньше интерферона в сравнении со взрослыми, но и хуже его воспринимает.
Так в составе Кипферон® появилось 500 тыс. МЕ интерферона, чтобы иметь более высокую терапевтическую эффективность по сравнению с другими интерфероновыми суппозиториями. Также разработчики хотели, чтобы их лекарство помогало от часто встречающейся микст-инфекции (сочетание сразу вирусного и бактериального компонента), что особенно важно для детей, у которых на фоне ослабленного иммунитета высока вероятность возникновения бактериальных осложнений. Поэтому они включили в свой лекарственный препарат дополнительный компонент, который бы боролся напрямую с вирусами и бактериями.
Так в составе Кипферон® появился уникальный КИП — комплексный иммуноголубиновый препарат — это готовые антитела, они распознают, обезвреживают и выводят из организма вирусы и бактерии1,3.
Вот уже практически 20 лет Кипферон® помогает малышам, детям и беременным женщинам противостоять вирусным и бактериальным инфекциям, бережно защищая их от вирусов и бактерий.
Задать вопрос
Купить Кипферон
® в интернет-аптеке Купить в аптеке
рядом с домом
Вы можете купить Кипферон®
в аптеках России
без рецепта
Имеются противопоказания. Необходима консультация врача.
Противовирусные препараты для здоровых детей
КЭТРИН Л. МАРГО, M.D., И АЛЛЕН Ф. ШОНЕССИ, PHARM.D.
МАРГО, M.D., И АЛЛЕН Ф. ШОНЕССИ, PHARM.D.
Семейный врач. 1998;57(5):1073-1077
Существует несколько противовирусных препаратов для лечения вирусных заболеваний у здоровых детей. У некоторых детей лечение ацикловиром является альтернативой вакцинации для лечения и профилактики ветряной оспы. Ацикловир также может быть полезен при лечении или профилактике инфекции простого герпеса у новорожденных. Рибавирин, когда-то рекомендовавшийся в качестве рутинной терапии для младенцев из группы высокого риска с респираторно-синцитиальным вирусным заболеванием, в настоящее время зарезервирован для использования у отдельных детей. Амантадин и римантидин эффективны против гриппа типа А и могут использоваться для защиты детей от гриппа, а также для уменьшения продолжительности и тяжести заболевания у уже больных.
Вирусные инфекции у новорожденных, младенцев и детей варьируются от обычной простуды до чрезвычайно редкого, но смертельного менингита, вызванного простым герпесом. Хотя мало что можно сделать для профилактики или лечения простуды, противовирусные средства могут сократить продолжительность некоторых вирусных заболеваний.
Хотя мало что можно сделать для профилактики или лечения простуды, противовирусные средства могут сократить продолжительность некоторых вирусных заболеваний.
В этом обзоре кратко изложено современное состояние противовирусных препаратов для лечения ветряной оспы, инфекций, вызванных вирусами простого герпеса и респираторно-синцитиальных вирусных инфекций, а также для профилактики и лечения гриппозной инфекции. Сложные потребности детей с ослабленным иммунитетом выходят за рамки этой статьи.
Ветряная оспа
Инфекция ветряной оспы (ветряная оспа) встречается примерно у 3-4 миллионов детей в год. Однако эта заболеваемость должна резко снизиться в результате недавнего одобрения вакцины против ветряной оспы (Varivax) и рекомендации по ее широкому использованию Консультативным комитетом по практике иммунизации Центров по контролю и профилактике заболеваний. 1,2
Помимо конституциональных проявлений ветряной оспы наиболее частыми побочными эффектами, связанными с инфекцией, являются пропущенные дни учебы (в среднем 8,7 дня) и рабочие дни родителей (в среднем 0,5 дня) которые должны оставаться дома со своим ребенком. 3 Серьезные осложнения у детей, такие как пневмония и энцефалит, встречаются редко, хотя ежегодно происходит около 50 летальных исходов. Группы повышенного риска осложнений включают младенцев в возрасте до одного года, подростков, беременных женщин и пациентов, принимающих высокие дозы кортикостероидов. Пожилые пациенты с заболеванием имеют более тяжелое клиническое течение.
3 Серьезные осложнения у детей, такие как пневмония и энцефалит, встречаются редко, хотя ежегодно происходит около 50 летальных исходов. Группы повышенного риска осложнений включают младенцев в возрасте до одного года, подростков, беременных женщин и пациентов, принимающих высокие дозы кортикостероидов. Пожилые пациенты с заболеванием имеют более тяжелое клиническое течение.
Ацикловир (зовиракс) одобрен для экстренного лечения ветряной оспы у детей и взрослых. При назначении ацикловира в течение первых 24 часов после появления сыпи у детей уменьшаются конституциональные симптомы и зуд. Также уменьшается количество поражений и время до образования корки. У детей, получавших лечение, снижение температуры происходит в среднем быстрее (1-й день по сравнению со 2-м днем). Однако к третьему дню у всех детей, получавших лечение, и у 75 процентов детей, не получавших лечения, лихорадка отсутствовала. 4 При начале терапии ацикловиром через 24 или более часов после появления сыпи польза не присуждается.
В настоящее время нет данных, указывающих на то, что лечение ветряной оспы ацикловиром ускоряет возвращение детей в школу или родителей на работу; скорость развития осложнений не уменьшилась при активной терапии.
Побочные эффекты, связанные с ацикловиром, встречаются редко. Проблемы с желудочно-кишечным трактом возникают редко. Иммунный ответ после ветряной оспы не зависит от терапии ацикловиром. Не было выявлено влияния на последующее развитие ветряной оспы у детей, получавших ацикловир.
Дозировка перорального ацикловира составляет 20 мг на кг на дозу, четыре раза в день, до 800 мг на дозу. Терапия ацикловиром не показана беременным женщинам и детям младше двух лет. Терапия продолжается в течение пяти дней и стоит от 70 до 80 долларов.
Ацикловир также использовался для предотвращения развития ветряной оспы после воздействия в домашних условиях. В одном неслепом нерандомизированном исследовании 5 детей, подвергшихся воздействию, получали ацикловир, начиная с семи-девятого дня после воздействия и продолжая в течение семи дней. Ветряная оспа развилась у 16 процентов детей, получавших лечение, по сравнению со 100 процентами детей, не получавших лечения. Сероконверсия, маркер субклинической инфекции, произошла у 85% детей, получавших ацикловир.
Ветряная оспа развилась у 16 процентов детей, получавших лечение, по сравнению со 100 процентами детей, не получавших лечения. Сероконверсия, маркер субклинической инфекции, произошла у 85% детей, получавших ацикловир.
Второе исследование 6 также показало, что профилактика ацикловиром, назначаемая на второй неделе после контакта, приводила к сероконверсии без развития симптомов. Эта защита наблюдалась не у всех субъектов исследования, поэтому до сих пор неизвестно, является ли ацикловир подходящей альтернативой иммуноглобулину против ветряной оспы для постконтактной защиты.
Американская академия педиатрии 7 (AAP) не рекомендует рутинное использование ацикловира в случаях неосложненной ветряной оспы у здоровых детей. Он рекомендует лечение ацикловиром для восприимчивых небеременных подростков. Терапию ацикловиром также можно рассматривать у детей старше 12 месяцев, получающих длительную терапию салицилатами (из-за риска развития синдрома Рея), у детей с хроническими заболеваниями легких или кожи, а также у детей, получающих аэрозольные кортикостероиды. Однако преимущества терапии в этих группах не доказаны.
Однако преимущества терапии в этих группах не доказаны.
Дети с ослабленным иммунитетом, в том числе получающие пероральные кортикостероиды в дозах 2 или более мг на кг в день, должны получать ацикловир внутривенно для профилактики или лечения диссеминированной ветряной оспы. Дозировка составляет 500 мг на м 2 каждые восемь часов. Детям до 12 месяцев доза составляет 30 мг/кг в сутки в 3 приема. Терапию продолжают в течение семи-десяти дней. 8(p635)
Два других противовирусных препарата, фамцикловир (Фамвир) и валацикловир (Валтрекс), доступны для лечения опоясывающего герпеса и рецидивирующего генитального герпеса. Ни одно из этих средств не предназначено для лечения ветряной оспы у детей, и ни одно исследование не оценивало использование этих средств у детей с лишаями.
Таким образом, терапия ацикловиром может немного уменьшить тяжесть и продолжительность острой ветряной оспы. Чтобы быть эффективной, терапия должна быть начата в течение 24 часов после появления сыпи, что может быть затруднительно. Его влияние на последующее развитие опоясывающего лишая неизвестно. С появлением на рынке вакцины против ветряной оспы лишь немногие дети нуждаются в лечении острой ветряной оспы.
Его влияние на последующее развитие опоясывающего лишая неизвестно. С появлением на рынке вакцины против ветряной оспы лишь немногие дети нуждаются в лечении острой ветряной оспы.
Вирус простого герпеса
Вирус простого герпеса чаще всего вызывает «лабиальный герпес» у младенцев и детей и генитальный герпес у подростков. Вирус простого герпеса также вызывает глазные инфекции у детей и поражения дистальных отделов пальцев (герпетический панариций) и в других местах.
Наиболее впечатляющие результаты применения противовирусной терапии у здоровых детей отмечены при применении ацикловира при лечении гингивостоматита, вызванного простым герпесом. Недавнее исследование 9 с участием 72 детей, получавших ацикловир в дозе 15 мг/кг пять раз в день в течение семи дней, показало заметное преимущество лечения по сравнению с плацебо. Внутриротовые поражения исчезли значительно быстрее (четыре дня против 10 дней) при использовании ацикловира. Другие признаки и симптомы исчезали при лечении значительно быстрее: лихорадка (один против трех дней), трудности с приемом пищи (четыре дня против семи), трудности с питьем (три дня против шести) и наличие поражений вокруг рта (ноль против пяти и одного дня). -полдня).
-полдня).
Гораздо большую озабоченность вызывает инфекция вируса простого герпеса у новорожденных. Вирус чаще всего передается младенцам от матери во время вагинальных родов или, иногда, восходящим путем.
Вероятность передачи инфекции во время вагинальных родов у матери с первым эпизодом генитального герпеса гораздо выше. В таких случаях скорость передачи может составлять от 33 до 50 процентов. К сожалению, в большинстве случаев инфицированные новорожденные рождаются у женщин, у которых ни анамнез, ни физикальное обследование не указывают на активную инфекцию. 8(p268)
Инфекция простого герпеса у новорожденных может варьировать от местной инфекции кожи, глаз и рта до генерализованной системной инфекции или локализованной инфекции центральной нервной системы. Неонатальный менингит встречается крайне редко: недавно опубликованное исследование 10 всех причин неонатального менингита в Англии и Уэльсе за период с 1975 по 1991 год выявило только 10 случаев, вызванных вирусом простого герпеса, среди 26 090 зарегистрированных случаев. По этой причине ААП 8(p272) не рекомендует эмпирическое лечение младенцев, рожденных от матерей с активными первичными или рецидивирующими инфекциями генитального герпеса, за исключением случаев, когда посев положительный или если не наблюдаются проявления инфекции, вызванной вирусом простого герпеса.
По этой причине ААП 8(p272) не рекомендует эмпирическое лечение младенцев, рожденных от матерей с активными первичными или рецидивирующими инфекциями генитального герпеса, за исключением случаев, когда посев положительный или если не наблюдаются проявления инфекции, вызванной вирусом простого герпеса.
Младенцы с документально подтвержденными инфекциями, вызванными вирусом простого герпеса, независимо от того, являются ли они локализованными, системными или поражающими центральную нервную систему, должны лечиться ацикловиром. Обычная доза составляет 30 мг на кг в сутки, вводимая внутривенно в три приема. Пациенты должны получать лечение в течение как минимум 14 дней и до 21 дня.
Рибавирин против респираторно-синцитиального вируса
Рибавирин (виразол) был одобрен с начала 1980-х годов для лечения респираторно-синцитиального вируса. Его вводят в виде аэрозоля, как правило, через кислородную палатку, головной бокс или маску с использованием специального генератора аэрозолей с малыми частицами. Начальная доза состоит из непрерывной ингаляции от 12 до 20 часов в день в течение четырех-пяти дней. Препарат также можно давать в больших дозах по два часа три раза в день.
Начальная доза состоит из непрерывной ингаляции от 12 до 20 часов в день в течение четырех-пяти дней. Препарат также можно давать в больших дозах по два часа три раза в день.
Недавнее исследование эффективности рибавирина противоречило предыдущим выводам. В результате в AAP 8(p445),11 были изменены рекомендации по применению рибавирина у младенцев с высоким риском серьезного респираторно-синцитиального заболевания. Предыдущая рекомендация о том, что рибавирин «следует использовать», была изменена в последнем отчете на менее четкую «следует рассмотреть».
В двух недавних исследованиях 12,13 не удалось подтвердить эффективность рибавирина. Одно исследование 12 сравнили продолжительность пребывания в больнице, количество дней кислородотерапии и количество пациентов, нуждающихся в искусственной вентиляции легких, в одной больнице, которая использовала рибавирин, и в одной больнице, где его не применяли. Никакой разницы в этих результатах между двумя группами не наблюдалось. Второе рандомизированное исследование 13 , сравнивающее рибавирин с физиологическим раствором плацебо, также не показало преимуществ, измеренных по тем же стандартам. Два метаанализа подтвердили отсутствие положительного влияния рибавирина на смертность, респираторные нарушения или продолжительность госпитализации. 14 В связи с этой новой информацией ААР рекомендует рассмотреть возможность применения рибавирина у младенцев с тяжелыми заболеваниями сердца или легких или с иммуносупрессией, а также у тяжелобольных.
Второе рандомизированное исследование 13 , сравнивающее рибавирин с физиологическим раствором плацебо, также не показало преимуществ, измеренных по тем же стандартам. Два метаанализа подтвердили отсутствие положительного влияния рибавирина на смертность, респираторные нарушения или продолжительность госпитализации. 14 В связи с этой новой информацией ААР рекомендует рассмотреть возможность применения рибавирина у младенцев с тяжелыми заболеваниями сердца или легких или с иммуносупрессией, а также у тяжелобольных.
Использование рибавирина заменяется иммунизацией внутривенным введением иммуноглобулина респираторно-синцитиального вируса (RespiGam) детям, подверженным риску развития респираторно-синцитиальной вирусной инфекции. Было показано, что использование иммуноглобулина снижает частоту госпитализаций и продолжительность госпитализации по поводу респираторно-синцитиальных вирусных инфекций или других респираторных инфекций. 15 Препарат вводят один раз в месяц во время сезона респираторно-синцитиального вируса детям младше двух лет с бронхолегочной дисплазией, которые получали или получают оксигенотерапию. Он также используется у детей, рожденных недоношенными (менее 35 недель беременности). 16
Он также используется у детей, рожденных недоношенными (менее 35 недель беременности). 16
Профилактика и лечение гриппа
Ежегодная вакцинация против гриппа является предпочтительным методом защиты детей от гриппа, особенно детей с высоким риском осложнений. Вакцина недорога, проста в применении и эффективна против вирусов гриппа как типа А, так и типа В (при условии, что они выбраны для включения в вакцину). Пероральные противовирусные препараты — амантадин (симметрел) и римантадин (флумадин) — эффективны только против вирусов гриппа типа А. Тем не менее, они 70 на 90 процентов эффективны в предотвращении заболеваний, вызванных этими вирусами, и их защита наступает быстрее, чем вакцинация, что делает их полезной альтернативой, особенно во время эпидемий гриппа типа А.
Амантадин и римантадин одобрены для профилактики гриппа типа А у детей в возрасте одного года и старше. 17 Эти препараты можно назначать детям, впервые получающим вакцину против гриппа, поскольку для выработки адекватного уровня антител требуется шесть недель. Пероральные агенты не влияют на реакцию антител на вакцину.
Пероральные агенты не влияют на реакцию антител на вакцину.
Амантадин, но не римантадин, также предназначен для лечения гриппа типа А у детей. Своевременное лечение в течение 48 часов после появления симптомов снижает тяжесть и сокращает продолжительность болезни. Влияние лечения на развитие осложнений неизвестно.
Дозы амантадина и римантадина для лечения и профилактики гриппа типа А указаны в таблице 1 . Оба агента доступны в жидкой форме, а также в форме таблеток или капсул. Типичные затраты на одну неделю терапии составляют 10 долларов за сироп амантадина и 12 долларов за сироп римантадина.
| Antiviral agent | 1 to 9 years and <40 kg (88 lb) | 10 to 18 years and ≥ 40 kg (88 lb) | Duration of therapy |
|---|---|---|---|
| Amantadine | |||
| Лечение | 5 мг на кг в день, до 150 мг в два приема | 100 мг два раза в день | До 24-48 часов после исчезновения симптомов (обычно семь дней всего) |
| Prophylaxis | 5 mg per kg per day, up to 150 mg in two doses | 100 mg twice daily | Up to six weeks (four weeks if the patient is concurrently immunized) |
| Rimantadine | |||
| Лечение | Не применимо | ||
| Профилактика | 5 мг на кг в день, до 150 мг в два приема | 100 мг два раза в день ) | |
Частота побочных эффектов выше у пациентов, получавших амантадин, чем у пациентов, получавших римантадин. Оба агента могут вызывать тошноту и анорексию. Побочные эффекты со стороны центральной нервной системы могут варьироваться от нервозности и головокружения до бреда, галлюцинаций и судорог. Эти побочные эффекты являются дозозависимыми.
Оба агента могут вызывать тошноту и анорексию. Побочные эффекты со стороны центральной нервной системы могут варьироваться от нервозности и головокружения до бреда, галлюцинаций и судорог. Эти побочные эффекты являются дозозависимыми.
Безопасность, плюсы и минусы, побочные эффекты
Когда ваш малыш (или большой ребенок) заболевает гриппом, может быть просто душераздирающе смотреть, как он борется с этими неприятными симптомами, даже если вы знаете, что эта борьба в значительной степени обычная. для курса.
Но когда грипп протекает тяжело, ваш инстинкт может предупредить вас о необходимости чего-то большего, чем сочувствие, — лечения.
Тамифлю — противовирусный препарат, который назначают для борьбы с сезонным гриппом. Детям также можно давать Тамифлю для профилактики или лечения гриппа под наблюдением педиатра. Хотя препарат не может полностью устранить симптомы, идея состоит в том, что он может помочь уменьшить тяжесть и продолжительность болезни.
Безопасен ли этот препарат для детей? Вот что вам нужно знать о Тамифлю и его преимуществах, а также о некоторых других способах профилактики гриппа в вашем доме.
Тамифлю имеет общее название Осельтамивир. Он был одобрен в 1999 году для использования у детей в возрасте от 2 недель и старше. Его побочные эффекты, как правило, легкие, поэтому он считается безопасным для использования. Однако врач вашего ребенка может не назначать его в каждом случае гриппа, независимо от его безопасности.
Противовирусные препараты предотвращают размножение вирусов гриппа в организме. Хотя противовирусные препараты отличаются от антибиотиков, которые борются с бактериальными инфекциями, они похожи тем, что их также должен назначать врач, а не покупать без рецепта (OTC).
Связанный: Что родители должны знать о гриппе и COVID-19
Ваш педиатр может назначить Тамифлю, если у вашего ребенка есть симптомы гриппа, такие как: боли в теле
Тем не менее, это не будет работать на любом типе вируса, поэтому это не лучший выбор, если у вашего ребенка нет положительного результата теста на грипп A или B.
Отдых, жидкости, безрецептурные жаропонижающие средства (например, детский тайленол) могут помочь детям с более легкими случаями гриппа выздороветь в течение недели.
Если у вашего ребенка серьезные симптомы, может помочь Тамифлю. Это также может быть особенно полезно, если ваш ребенок подвергается наибольшему риску осложнений от гриппа.
По данным Центров по контролю и профилактике заболеваний (CDC), факторы риска включают возраст младше 5 лет, особенно младше 2 лет, а также наличие хронических заболеваний, таких как астма, диабет или заболевания сердца/легких.
Связанный: Как обращаться со школьными больничными
Доктор знает лучше
Всегда следуйте инструкциям по дозировке, прописанным врачом вашего ребенка.
Тамифлю наиболее эффективен, если его начать принимать в течение первых 2 дней болезни. Некоторые педиатры могут даже предложить, чтобы дети из групп высокого риска начинали принимать его после подтвержденного контакта с человеком, больным гриппом, до появления каких-либо симптомов.
И хотя время важно, эксперты из Центра по контролю и профилактике заболеваний говорят, что некоторым детям — детям с высоким риском осложнений или госпитализированным — может помочь прием Тамифлю даже через 2 дня после начала заболевания.
Препарат принимают внутрь в виде таблеток или жидкости. Продолжительность лечения обычно составляет 5 дней. Дозировка зависит от возраста/веса вашего ребенка.
Общие рекомендации по дозировке для лечения следующие, но только врач вашего ребенка может определить, что ему нужно. Их врач также переведет рекомендацию миллиграммов на килограмм (мг/кг) в дозу в миллилитрах (мл), специфичную для вашего ребенка.
| Возраст/вес | Дозировка |
|---|---|
| Ages 1 and under | 3 mg/kg twice daily |
| Over age 1 but 15 kg or less | 30 mg twice daily |
| 16–23 kg | 45 mg twice daily |
| 24–40 кг | 60 мг два раза в день |
| Более 40 кг | 75 мг два раза в день |
Связанные: когда у вашего ребенка до ребенка в госпту дети и взрослые показывают, что противовирусные препараты, такие как Тамифлю, могут предотвратить грипп, приводящий к дыхательной недостаточности и смерти. В частности, эти препараты могут снизить риск пневмонии или других проблем со здоровьем, которые приводят к госпитализации.
В частности, эти препараты могут снизить риск пневмонии или других проблем со здоровьем, которые приводят к госпитализации.
В целом противовирусные препараты могут облегчить симптомы у вашего ребенка и сократить общую продолжительность болезни на 1–1,5 дня. Это означает, что ваш малыш сможет вернуться к своей повседневной жизни — школе, занятиям, играм — раньше, чем если бы он не принимал препарат.
Помните о других
Прежде чем отправить ребенка обратно в школу, подтвердите у педиатра, что он больше не заразен.
При раннем применении Тамифлю может также предотвращать развитие ушных инфекций по мере прогрессирования гриппа. Это может даже снизить потребность в использовании антибиотиков для лечения других бактериальных осложнений, связанных с гриппом, у детей в возрасте от 1 до 12 лет.
Связанный материал: Краткие советы по лечению детей от простуды или гриппа
Без страховки цена противовирусных препаратов может быть высокой, особенно если у вас более одного ребенка, которым могут понадобиться лекарства. Стоимость Тамифлю без страховки может составлять чуть более 100 долларов.
Стоимость Тамифлю без страховки может составлять чуть более 100 долларов.
Со страховкой, конечно, это может быть просто ваша обычная доплата. И вы также можете попробовать использовать такие платформы, как GoodRx, где цена может составлять всего 25 долларов.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) подчеркивает, что Тамифлю наиболее эффективен, если его принять в течение 48 часов после появления симптомов у вашего ребенка. Итак, если вы ошибочно приняли ранний кашель или чихание за простуду, возможно, вы пропустили идеальное окно для лечения.
Еще один недостаток, о котором вы, возможно, слышали, заключается в том, что Тамифлю может быть неэффективен при определенных штаммах гриппа. Однако CDC выявил только один случай, когда вирус был устойчив к Тамифлю. Так было со штаммом h2N1 в 2009 году.
В противном случае CDC ежегодно отслеживает преобладающие штаммы гриппа и соответственно рекомендует использование противовирусных препаратов.
Основные побочные эффекты, связанные с Тамифлю, включают тошноту и рвоту.
FDA отмечает, однако, что у детей в возрасте 16 лет и младше были зарегистрированы необычные побочные эффекты. Они могут включать:
- галлюцинации
- спутанность сознания
- судороги
- другие неврологические или психические проблемы
Важно понимать, что эти побочные эффекты возникают редко.
Наблюдайте за своим ребенком на предмет признаков изменения поведения. Немедленно свяжитесь с врачом, если заметите что-либо, выходящее за рамки их нормального состояния. И если вы заметили признаки затрудненного дыхания, обезвоживания или ухудшение симптомов, немедленно обратитесь за медицинской помощью.
Связанный: Насколько серьезны побочные эффекты Тамифлю?
Тамифлю также называют ингибитором нейраминидазы, так как он блокирует вирусный фермент нейраминидазу, который отвечает за проникновение вируса гриппа в клетки дыхательной системы. В результате педиатр вашего ребенка может назначить Тамифлю до того, как появятся симптомы, чтобы фактически предотвратить грипп.
В результате педиатр вашего ребенка может назначить Тамифлю до того, как появятся симптомы, чтобы фактически предотвратить грипп.
Тем не менее, Тамифлю не назначают широко для профилактики, если только ваш ребенок не относится к группе высокого риска. Вместо этого эксперты сходятся во мнении, что лучший метод профилактики гриппа для детей в возрасте от 6 месяцев и старше — это ежегодная прививка от сезонного гриппа.
Другие способы профилактики гриппа включают:
- избегание тесного контакта с больными гриппом
- поощрение людей прикрываться при кашле/чихании
- соблюдение правил гигиены (мытье рук, поверхностей и т. д.)
Связанные с этим: Как предотвратить грипп: естественные способы, после заражения и многое другое
Есть еще три противовирусных препарата, одобренных FDA для использования у детей. Тип, предлагаемый вашему ребенку, будет зависеть от его возраста и истории болезни.
- Реленза (занамивир): это лекарство предназначено для детей в возрасте от 7 лет и старше.
 Его вводят перорально с помощью ингалятора «Дисхалер». Ваш врач может не рекомендовать использование Релензы, если у вашего ребенка есть основное респираторное заболевание, такое как астма или хроническое заболевание легких.
Его вводят перорально с помощью ингалятора «Дисхалер». Ваш врач может не рекомендовать использование Релензы, если у вашего ребенка есть основное респираторное заболевание, такое как астма или хроническое заболевание легких. - Рапиваб (перамивир): этот препарат предназначен для детей в возрасте от 2 лет и старше. Его вводят внутривенно.
- Xofluza (балоксавир): это лекарство предназначено для детей старше 12 лет и старше. Это разовая доза и вводится внутрь.
В связи с этим: Почему важно обратиться к врачу в течение 48 часов после появления симптомов гриппа
Как можно скорее обратитесь к педиатру, если у вашего ребенка появились симптомы гриппа или он контактировал с кем-то, у кого положительный результат теста на грипп. Чем раньше вы назначите противовирусные препараты, такие как Тамифлю, тем эффективнее они помогут организму бороться с вирусом.
Если у вас есть опасения по поводу этого препарата, спросите своего врача о преимуществах и рисках, характерных для возраста вашего ребенка и истории болезни. В противном случае вы можете помочь предотвратить грипп, делая прививку от гриппа каждый год, часто мойте руки и избегая тесного контакта с больными людьми.
В противном случае вы можете помочь предотвратить грипп, делая прививку от гриппа каждый год, часто мойте руки и избегая тесного контакта с больными людьми.
Предварительно активированный противовирусный врожденный иммунитет в верхних дыхательных путях контролирует раннюю инфекцию SARS-CoV-2 у детей
Abstract
У детей снижена частота инфицирования коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2) и значительно снижен риск на развитие тяжелого течения коронавирусной болезни 2019 года по сравнению со взрослыми. Однако молекулярные механизмы, лежащие в основе защиты в младших возрастных группах, остаются неизвестными. Здесь мы характеризуем транскрипционный ландшафт одиночных клеток в верхних дыхательных путях у SARS-CoV-2-негативных ( n = 18) и соответствующих по возрасту SARS-CoV-2-положительных ( n = 24) детей и соответствующие образцы взрослых ( n = 44), охватывающие возрастной диапазон от 4 недель до 77 лет. У детей наблюдалась более высокая базальная экспрессия соответствующих рецепторов распознавания образов, таких как MDA5 ( IFIh2 ) и RIG-I ( DDX58 ), в эпителиальных клетках верхних дыхательных путей, макрофагах и дендритных клетках, что приводило к более сильным врожденным противовирусным реакциям на SARS-CoV-2. инфекций, чем у взрослых. Далее мы обнаружили различные субпопуляции иммунных клеток, включая KLRC1 (NKG2A) + цитотоксических Т-клеток и популяция CD8 + Т-клеток с фенотипом памяти, встречающимся преимущественно у детей. Наше исследование предоставляет доказательства того, что иммунные клетки дыхательных путей детей настроены на распознавание вирусов, что приводит к более сильному раннему врожденному противовирусному ответу на инфекцию SARS-CoV-2, чем у взрослых.
инфекций, чем у взрослых. Далее мы обнаружили различные субпопуляции иммунных клеток, включая KLRC1 (NKG2A) + цитотоксических Т-клеток и популяция CD8 + Т-клеток с фенотипом памяти, встречающимся преимущественно у детей. Наше исследование предоставляет доказательства того, что иммунные клетки дыхательных путей детей настроены на распознавание вирусов, что приводит к более сильному раннему врожденному противовирусному ответу на инфекцию SARS-CoV-2, чем у взрослых.
Главная
Неоднократно сообщалось, что у лиц более молодого возраста риск заболеть коронавирусной болезнью значительно ниже 2019(COVID-19), несмотря на аналогичный риск заражения, что выражается в резком увеличении смертности с увеличением возраста 1,2,3 . Эти наблюдения позволяют предположить, что дети могут иметь более высокую способность контролировать инфекцию SARS-CoV-2. Было показано, что ранний клеточный внутренний врожденный иммунный ответ, опосредованный рецепторами распознавания образов (PRR) и системой интерферонов типа I и III (IFN), имеет решающее значение для успешного контроля инфекции SARS-CoV-2 4 . В соответствии с этими наблюдениями, недавние исследования сравнивали взрослых и детей с тяжелой формой COVID-19.или те, кто поступил в отделение неотложной помощи и описали нарушение ответа IFN у детей с COVID-19 (ссылки 5,6 ). Однако молекулярные механизмы, защищающие от COVID-19 в более молодых возрастных группах, особенно у тех, у кого симптомы отсутствуют или имеют только легкие/умеренные симптомы, остаются неизвестными.
В соответствии с этими наблюдениями, недавние исследования сравнивали взрослых и детей с тяжелой формой COVID-19.или те, кто поступил в отделение неотложной помощи и описали нарушение ответа IFN у детей с COVID-19 (ссылки 5,6 ). Однако молекулярные механизмы, защищающие от COVID-19 в более молодых возрастных группах, особенно у тех, у кого симптомы отсутствуют или имеют только легкие/умеренные симптомы, остаются неизвестными.
Чтобы понять более высокую способность детей контролировать инфекцию SARS-CoV-2 на ранней стадии, мы систематически охарактеризовали транскрипционный ландшафт верхних дыхательных путей, область дыхательных путей с высокой восприимчивостью к инфекции SARS-CoV-2 7 , у детей и взрослых с отрицательным и положительным результатом на SARS-CoV-2.
Результаты
Различный клеточный состав верхних дыхательных путей у детей и взрослых
В исследование были включены участники трех разных когорт COVID-19: исследование RECAST, посвященное COVID-19 у детей и их семей, исследование Pa-COVID-19 исследование и исследование SC2 8,9 , в том числе SARS-CoV-2-отрицательные и SARS-CoV-2-положительные дети ( n = 42) и взрослые ( n = 44). Всего полученный набор данных содержал 268 745 ячеек (рис. 1а). Образцы из верхних дыхательных путей (носа) были взяты у лиц в возрасте от 4 недель до 77 лет с положительным результатом ПЦР на SARS-CoV-2, а также у контрольных лиц того же возраста, отрицательных на SARS-CoV-2 (дополнительные таблицы 1 и 2). С учетом раннего инфицирования в этом исследовании рассматривались только случаи COVID-19 легкой/средней степени тяжести (рис. 1а). На основе данных секвенирования одноклеточной РНК (scRNA-seq) мы идентифицировали 33 различных типа клеток или состояний в верхних дыхательных путях этих людей, включая 21 иммунный и 12 подтипов эпителиальных клеток (рис. 1b и расширенные данные рис. . 1а, б). Мы наблюдали поразительные различия между детьми и взрослыми участниками исследования в отношении состава иммунных клеток и компартмента эпителиальных клеток в слизистой оболочке носа. В то время как иммунные клетки редко обнаруживались в образцах носа от здоровых взрослых, образцы от SARS-CoV-2-отрицательных детей содержали большое количество почти каждой подгруппы иммунных клеток с общим преобладанием нейтрофилов (рис.
Всего полученный набор данных содержал 268 745 ячеек (рис. 1а). Образцы из верхних дыхательных путей (носа) были взяты у лиц в возрасте от 4 недель до 77 лет с положительным результатом ПЦР на SARS-CoV-2, а также у контрольных лиц того же возраста, отрицательных на SARS-CoV-2 (дополнительные таблицы 1 и 2). С учетом раннего инфицирования в этом исследовании рассматривались только случаи COVID-19 легкой/средней степени тяжести (рис. 1а). На основе данных секвенирования одноклеточной РНК (scRNA-seq) мы идентифицировали 33 различных типа клеток или состояний в верхних дыхательных путях этих людей, включая 21 иммунный и 12 подтипов эпителиальных клеток (рис. 1b и расширенные данные рис. . 1а, б). Мы наблюдали поразительные различия между детьми и взрослыми участниками исследования в отношении состава иммунных клеток и компартмента эпителиальных клеток в слизистой оболочке носа. В то время как иммунные клетки редко обнаруживались в образцах носа от здоровых взрослых, образцы от SARS-CoV-2-отрицательных детей содержали большое количество почти каждой подгруппы иммунных клеток с общим преобладанием нейтрофилов (рис. 1b, c и расширенные данные, рис. 2a). ). У взрослых инфекция SARS-CoV-2 была связана с притоком иммунных клеток, в то время как доля иммунных и эпителиальных клеток у детей оставалась почти стабильной (рис. 1c и расширенные данные, рис. 2a). При инфицировании детские нейтрофилы проявляли более выраженный, чем у инфицированных взрослых, активированный фенотип, характеризующийся повышенной экспрессией, например, CCL3 и CXCR1 / 2 (дополнительная таблица 4).
1b, c и расширенные данные, рис. 2a). ). У взрослых инфекция SARS-CoV-2 была связана с притоком иммунных клеток, в то время как доля иммунных и эпителиальных клеток у детей оставалась почти стабильной (рис. 1c и расширенные данные, рис. 2a). При инфицировании детские нейтрофилы проявляли более выраженный, чем у инфицированных взрослых, активированный фенотип, характеризующийся повышенной экспрессией, например, CCL3 и CXCR1 / 2 (дополнительная таблица 4).
a , Назальные образцы детей ( n = 42) и взрослых ( n = 44) были взяты у лиц с отрицательным и положительным результатом (бессимптомная/легкая/умеренная форма COVID-19) на SARS-CoV-2 и подвергнуты scRNA-seq. b , Единая многообразная аппроксимация и проекция (UMAP), показывающая все идентифицированные индивидуальные типы и состояния иммунных и эпителиальных клеток. МС/базофилы, тучные клетки или базофилы; moMa, макрофаги, происходящие из моноцитов; nrMa, нерезидентные макрофаги; rMa, резидентные макрофаги; mDC, миелоидные дендритные клетки; CD11c_mDC, CD11c-экспрессирующие mDC; pDCs, плазмоцитоидные дендритные клетки; DNT, дважды отрицательные Т-клетки; NK, естественные клетки-киллеры; NKT, натуральные Т-киллеры; p_NKT, пролиферирующие NKT-клетки; ag_T, стареющие Т-клетки; CD8_Tm, память CD8 + Т-клеток; CTL1 и CTL2, цитотоксические Т-клетки 1 и 2 типа; IL-17A_CD8, IL-17A-экспрессирующие CD8 T-клетки; IL-17a_CD4, IL-17A, экспрессирующий CD4 + Т-клеток; p_T, пролиферирующие Т-клетки; Cil-diff, дифференцирующиеся реснитчатые клетки; Epi_low РНК, эпителиальные клетки с низким содержанием РНК; FOXN4, FOXN4 + клеток. c , Масштабированные UMAP, отображающие 45 000 клеток на группу, обнаруживают выраженные различия в составе клеток носа у детей и взрослых, отрицательных и положительных по SARS-CoV-2. d , Таблица, показывающая все типы/состояния клеток, значительно различающиеся у детей и взрослых у неинфицированных людей.
МС/базофилы, тучные клетки или базофилы; moMa, макрофаги, происходящие из моноцитов; nrMa, нерезидентные макрофаги; rMa, резидентные макрофаги; mDC, миелоидные дендритные клетки; CD11c_mDC, CD11c-экспрессирующие mDC; pDCs, плазмоцитоидные дендритные клетки; DNT, дважды отрицательные Т-клетки; NK, естественные клетки-киллеры; NKT, натуральные Т-киллеры; p_NKT, пролиферирующие NKT-клетки; ag_T, стареющие Т-клетки; CD8_Tm, память CD8 + Т-клеток; CTL1 и CTL2, цитотоксические Т-клетки 1 и 2 типа; IL-17A_CD8, IL-17A-экспрессирующие CD8 T-клетки; IL-17a_CD4, IL-17A, экспрессирующий CD4 + Т-клеток; p_T, пролиферирующие Т-клетки; Cil-diff, дифференцирующиеся реснитчатые клетки; Epi_low РНК, эпителиальные клетки с низким содержанием РНК; FOXN4, FOXN4 + клеток. c , Масштабированные UMAP, отображающие 45 000 клеток на группу, обнаруживают выраженные различия в составе клеток носа у детей и взрослых, отрицательных и положительных по SARS-CoV-2. d , Таблица, показывающая все типы/состояния клеток, значительно различающиеся у детей и взрослых у неинфицированных людей. Даны средние различия в процентах; положительные значения указывают на большее количество клеток соответствующей клеточной популяции у детей по сравнению со взрослыми. Сравнения проводили с помощью критерия Краскела-Уоллиса с последующим двусторонним апостериорным сравнением Данна с поправкой Бенджамини-Хохберга (*** P < 0,001; нейтрофилы, 5,54 × 10 –7 ; CD8_T m , 1,97 × 10 -4 ; CTL2, 1,83 × 10 -5 ; Базальная, 6,96 × 10 -5 ; Реснитчатый, 9,18 × 10 -7 ; также см. рис. 2а с расширенными данными). e , Графики рассеяния, представляющие изменения специфических иммунных и эпителиальных клеток с течением времени. Изображены проценты соответствующего типа/состояния клеток по отношению ко всем клеткам для иммунных клеток (слева) или эпителиальных клеток (справа) каждого индивидуума. Лица с отрицательным результатом на SARS-CoV-2 обозначены серым цветом, лица с положительным результатом на SARS-CoV-2 — красным.
Даны средние различия в процентах; положительные значения указывают на большее количество клеток соответствующей клеточной популяции у детей по сравнению со взрослыми. Сравнения проводили с помощью критерия Краскела-Уоллиса с последующим двусторонним апостериорным сравнением Данна с поправкой Бенджамини-Хохберга (*** P < 0,001; нейтрофилы, 5,54 × 10 –7 ; CD8_T m , 1,97 × 10 -4 ; CTL2, 1,83 × 10 -5 ; Базальная, 6,96 × 10 -5 ; Реснитчатый, 9,18 × 10 -7 ; также см. рис. 2а с расширенными данными). e , Графики рассеяния, представляющие изменения специфических иммунных и эпителиальных клеток с течением времени. Изображены проценты соответствующего типа/состояния клеток по отношению ко всем клеткам для иммунных клеток (слева) или эпителиальных клеток (справа) каждого индивидуума. Лица с отрицательным результатом на SARS-CoV-2 обозначены серым цветом, лица с положительным результатом на SARS-CoV-2 — красным. Линии представляют результаты подгонки кривой с помощью локальной полиномиальной регрессии (LOESS). Значения P взяты из линейного регрессионного анализа (с поправкой на двусторонний анализ Бенджамини-Хохберга).
Линии представляют результаты подгонки кривой с помощью локальной полиномиальной регрессии (LOESS). Значения P взяты из линейного регрессионного анализа (с поправкой на двусторонний анализ Бенджамини-Хохберга).
Изображение в натуральную величину
Интересно, что многие популяции эпителиальных клеток продемонстрировали четкую возрастную зависимость, например, количество бокаловидных клеток уменьшилось, а количество реснитчатых клеток увеличилось с возрастом (рис. 1d,e). В недавнем дополнительном исследовании был проанализирован клеточный состав слизистой оболочки носа у здоровых детей и детей, инфицированных SARS-CoV-2, на основе методов секвенирования РНК и деконволюции клеток. Авторы не смогли идентифицировать специфичные для детей бокаловидные клетки, но скорее описали, что в образцах здоровых детей преобладали реснитчатые клетки, подчеркивая ограничения подходов объемной РНК 10 .
Входные рецепторы SARS-CoV-2 не различаются по экспрессии у детей по сравнению со взрослыми
Уровень экспрессии ACE2 , кодирующего входной рецептор SARS-CoV-2, и TMPRSS2 , FURIN , 0 CTSB , CTSL и CTSV , кодирующие протеазы, ассоциированные с проникновением, были одинаковыми у детей и взрослых и не активировались при легкой/средней степени тяжести COVID-19 по сравнению с неинфицированным статусом (расширенные данные, рис. 2b). Следовательно, эти факторы проникновения вируса не могут объяснить различия в патофизиологии SARS-CoV-2 у детей и взрослых.
2b). Следовательно, эти факторы проникновения вируса не могут объяснить различия в патофизиологии SARS-CoV-2 у детей и взрослых.
У детей наблюдается повышенная чувствительность к вирусам в эпителиальных клетках дыхательных путей
SARS-CoV-2 представляет собой РНК-вирус с положительной цепью с очень высокой скоростью репликации 11,12 . Следовательно, контроль инфекции SARS-CoV-2 требует оптимального раннего и скоординированного врожденного противовирусного иммунитета. Этот ответ активируется различными PRR. Недавно было получено все больше доказательств в поддержку MDA5 ( IFIh2 ) в качестве основного PRR для SARS-CoV-2 в эпителиальных клетках с RIG-I ( DDX58 ), возможно, играет дополнительную, но незначительную роль 13,14 (собственные неопубликованные данные). Важным энхансером распознавания вирусной РНК с помощью MDA5 является LGP2 ( DHX58 ) 15 . Важно отметить, что PRR, в частности MDA5 и LGP2, лишь слабо экспрессируются во многих типах эпителиальных клеток, но сильно активируются за счет регуляции с положительной обратной связью при вирусной инфекции клетки или при паракринном воздействии IFN типа I или III. Динамика этой регуляции с обратной связью имеет решающее значение для успешного контроля заражающего вируса (рис. 2а). Важность оси PRR/IFN для успешного разрешения инфекции SARS-CoV-2 недавно была продемонстрирована клиническими исследованиями, обнаружившими сильную связь между врожденными ошибками в различных локусах системы PRR/IFN с повышенным риском тяжелого течения COVID-19.(ссылка 16 ). Точно так же, и затрагивая даже гораздо более широкую группу пациентов, было показано, что аутоантитела, направленные против IFN I типа, встречаются с удивительно высокой частотой у пациентов с тяжелой формой COVID-19 (ссылка 17 ).
Динамика этой регуляции с обратной связью имеет решающее значение для успешного контроля заражающего вируса (рис. 2а). Важность оси PRR/IFN для успешного разрешения инфекции SARS-CoV-2 недавно была продемонстрирована клиническими исследованиями, обнаружившими сильную связь между врожденными ошибками в различных локусах системы PRR/IFN с повышенным риском тяжелого течения COVID-19.(ссылка 16 ). Точно так же, и затрагивая даже гораздо более широкую группу пациентов, было показано, что аутоантитела, направленные против IFN I типа, встречаются с удивительно высокой частотой у пациентов с тяжелой формой COVID-19 (ссылка 17 ).
a , Схематическое представление эпителиального ответа на инфекцию SARS-CoV-2, включая гены, участвующие в восприятии вируса и последующем ответе IFN; создано с помощью BioRender.com. b Точечные диаграммы, изображающие экспрессию генов, чувствительных к вирусам, в эпителиальных клетках детей и взрослых. Каждое значительное увеличение по сравнению с SARS-CoV-2-отрицательными детьми ( n = 18) с SARS-CoV-2-отрицательными взрослыми ( n = 23) и SARS-CoV-2-положительными детьми в течение первых (дней) после появления симптомов (dps) ≤ 4, n = 11) или поздняя фаза инфекции (dps 5–12, n = 11) у SARS-CoV-2-позитивных взрослых среди ранних ( n = 13) или поздно ( n = 8) фаза инфекции, соответственно, отмечена красным кружком (двухсторонний с поправкой на Бенджамини-Хохберга, Wilcoxon P < 0,05). Ave.exp., средняя экспрессия гена; Процент exp., процент клеток, экспрессирующих ген. c , Скрипичные графики, показывающие экспрессию прототипных генов, чувствительных к вирусам, в эпителиальных клетках пациентов с положительным результатом на SARS-CoV-2 ( n = 45) по отношению к дням после появления первых симптомов. d , Тепловая карта, показывающая масштабированную экспрессию 171 репрезентативного ISG во всех эпителиальных клетках на ранней стадии инфекции SARS-CoV-2 (dps ≤ 4).
Каждое значительное увеличение по сравнению с SARS-CoV-2-отрицательными детьми ( n = 18) с SARS-CoV-2-отрицательными взрослыми ( n = 23) и SARS-CoV-2-положительными детьми в течение первых (дней) после появления симптомов (dps) ≤ 4, n = 11) или поздняя фаза инфекции (dps 5–12, n = 11) у SARS-CoV-2-позитивных взрослых среди ранних ( n = 13) или поздно ( n = 8) фаза инфекции, соответственно, отмечена красным кружком (двухсторонний с поправкой на Бенджамини-Хохберга, Wilcoxon P < 0,05). Ave.exp., средняя экспрессия гена; Процент exp., процент клеток, экспрессирующих ген. c , Скрипичные графики, показывающие экспрессию прототипных генов, чувствительных к вирусам, в эпителиальных клетках пациентов с положительным результатом на SARS-CoV-2 ( n = 45) по отношению к дням после появления первых симптомов. d , Тепловая карта, показывающая масштабированную экспрессию 171 репрезентативного ISG во всех эпителиальных клетках на ранней стадии инфекции SARS-CoV-2 (dps ≤ 4). Аннотируются только выбранные гены; полностью аннотированную тепловую карту см. на рис. 3.9 с расширенными данными.0133 e , Дифференциальная экспрессия выбранных ISG в модели in vitro, сравнивающая ответ на инфекцию SARS-CoV-2 в MDA5 (кодируется IFIh2 ) со сверхэкспрессией клеток A549 ACE2 и контрольных пустых векторов. n = 3 биологически независимых повтора; планки погрешностей показывают среднее ± sem; * P <0,05, *** P <0,001 ( IFNB1 , 5,47 × 10 −4 ; MX1, 2,63 × 10 –2 ; BST2 , 8,74 × 10 – 4 ;0018 ; RSAD2 , 4,24 × 10 -2 ; IFIT1 , 1,30 × 10 −2 ) от одностороннего Стьюдента t -тест.
Аннотируются только выбранные гены; полностью аннотированную тепловую карту см. на рис. 3.9 с расширенными данными.0133 e , Дифференциальная экспрессия выбранных ISG в модели in vitro, сравнивающая ответ на инфекцию SARS-CoV-2 в MDA5 (кодируется IFIh2 ) со сверхэкспрессией клеток A549 ACE2 и контрольных пустых векторов. n = 3 биологически независимых повтора; планки погрешностей показывают среднее ± sem; * P <0,05, *** P <0,001 ( IFNB1 , 5,47 × 10 −4 ; MX1, 2,63 × 10 –2 ; BST2 , 8,74 × 10 – 4 ;0018 ; RSAD2 , 4,24 × 10 -2 ; IFIT1 , 1,30 × 10 −2 ) от одностороннего Стьюдента t -тест.
Изображение полного размера
Примечательно, что мы обнаружили значительно более высокий базальный уровень экспрессии генов, кодирующих RIG-I, MDA5 и LGP2, в эпителиальных клетках верхних дыхательных путей здоровых детей по сравнению со взрослыми (рис. 2b). Этот результат предполагает повышенную способность слизистой оболочки дыхательных путей детей реагировать на вирусные инфекции, что также подтверждается значительно повышенным количеством врожденных иммунных клеток в их верхних дыхательных путях (рис. 1 и расширенные данные, рис. 2a). В эпителиальных клетках детей и взрослых, инфицированных SARS-CoV-2, мы наблюдали высокий уровень экспрессии этих генов (рис. 2c), в частности, в начале заболевания COVID-19.симптомы, которые имели тенденцию к снижению до 4-го дня (день 0-4, называемые ранней фазой) и оставались на более низком уровне в более поздней фазе заболевания (5-12 дни после появления симптомов, называемые поздней фазой). Можно предположить, что более высокая базальная экспрессия этих PRR позволит немедленно обнаружить SARS-CoV-2 с помощью MDA5/LGP2 в инфицированных эпителиальных клетках (рис. 2а). Поразительно, но эпителиальные клетки дыхательных путей у детей демонстрировали повышенную экспрессию этих генов PRR по сравнению с уровнем экспрессии этих генов в эпителиальных клетках у взрослых с положительным результатом на SARS-CoV-2 (рис.
2b). Этот результат предполагает повышенную способность слизистой оболочки дыхательных путей детей реагировать на вирусные инфекции, что также подтверждается значительно повышенным количеством врожденных иммунных клеток в их верхних дыхательных путях (рис. 1 и расширенные данные, рис. 2a). В эпителиальных клетках детей и взрослых, инфицированных SARS-CoV-2, мы наблюдали высокий уровень экспрессии этих генов (рис. 2c), в частности, в начале заболевания COVID-19.симптомы, которые имели тенденцию к снижению до 4-го дня (день 0-4, называемые ранней фазой) и оставались на более низком уровне в более поздней фазе заболевания (5-12 дни после появления симптомов, называемые поздней фазой). Можно предположить, что более высокая базальная экспрессия этих PRR позволит немедленно обнаружить SARS-CoV-2 с помощью MDA5/LGP2 в инфицированных эпителиальных клетках (рис. 2а). Поразительно, но эпителиальные клетки дыхательных путей у детей демонстрировали повышенную экспрессию этих генов PRR по сравнению с уровнем экспрессии этих генов в эпителиальных клетках у взрослых с положительным результатом на SARS-CoV-2 (рис. 2b), особенно на ранней стадии заболевания после появления симптомов. Начиная с 5-го дня чувствительность к вирусу у детей и взрослых в значительной степени сопоставима (рис. 2b, нижний график).
2b), особенно на ранней стадии заболевания после появления симптомов. Начиная с 5-го дня чувствительность к вирусу у детей и взрослых в значительной степени сопоставима (рис. 2b, нижний график).
После обнаружения вируса передача сигналов через IRF3/NFκB приводит к экспрессии первичных противовирусных эффекторов, а также противовирусных цитокинов, таких как IFNβ и IFNλ (рис. 2a). IFN действуют на эпителиальные клетки аутокринным и паракринным образом, дополнительно повышая чувствительность тканей к MDA5/LGP2 и индуцируя широкий спектр IFN-стимулируемых генов (ISG). Хотя нам не удалось обнаружить экспрессию самих интерферонов типа I и типа III, ISG продемонстрировали впечатляющий характер активации в эпителиальных клетках детей, инфицированных SARS-CoV-2, включая многие гены, которые, как ранее было показано, проявляют сильную противовирусную активность против SARS-CoV-2. CoV-2, например LY6E (ссылка 18 ), IFITM2 и BST2 (ссылка 19 ). Во всех эпителиальных клетках, и в частности в реснитчатых клетках, величина экспрессии ISG значительно превышала таковую у инфицированных взрослых как на ранней, так и на поздней фазах инфекции (рис. 2d и расширенные данные, рис. 3) с общей тенденцией к снижению на поздней стадии. фаза (расширенные данные, рис. 3).
Во всех эпителиальных клетках, и в частности в реснитчатых клетках, величина экспрессии ISG значительно превышала таковую у инфицированных взрослых как на ранней, так и на поздней фазах инфекции (рис. 2d и расширенные данные, рис. 3) с общей тенденцией к снижению на поздней стадии. фаза (расширенные данные, рис. 3).
Чтобы продемонстрировать прямую связь между уровнями экспрессии MDA5 и активацией ISG при инфицировании SARS-CoV-2, мы создали модель in vitro с использованием линии клеток эпителия легких человека A549., который демонстрирует очень низкие базовые уровни экспрессии MDA5, аналогичные уровням экспрессии, обнаруженным в эпителиальных клетках носа здоровых взрослых. Как и ожидалось, на основании неэффективного распознавания MDA5 в сочетании с быстрой репликацией и экспрессией кодируемых вирусом антагонистов 20 , при инфицировании SARS-CoV-2 в этих клетках индуцировались лишь незначительные количества транскриптов IFNB1 и ISG. Однако в клетках с умеренно повышенной базовой экспрессией MDA5 за счет лентивирусной трансдукции, позволяющей эффективно распознавать вирус до экспрессии антагонистов, мы наблюдали значительную индукцию экспрессии IFNB1 и ключевые ISG, включая MX1 , BST2 (тетерин), RSAD2 (гадюка) и IFIT1 (рис. 2e). Эти результаты подтверждают центральную роль экспрессии MDA5 до заражения для обнаружения SARS-CoV-2 и индукции быстрого и надежного ответа ISG.
2e). Эти результаты подтверждают центральную роль экспрессии MDA5 до заражения для обнаружения SARS-CoV-2 и индукции быстрого и надежного ответа ISG.
Повышенная активация врожденных иммунных клеток у детей
Изучение взаимодействий иммунных и эпителиальных клеток выявило более сильное взаимодействие иммунных и эпителиальных клеток у детей по сравнению со взрослыми, особенно до заражения. Среди иммунных клеток нерезидентные макрофаги (nrMa) и макрофаги, происходящие из моноцитов (moMa), а также CD11c + дендритных клеток (CD11c_mDC) были наиболее интерактивными (рис. 3а). Эти субпопуляции иммунных клеток показали более высокий статус активации у детей, о чем свидетельствует повышенный уровень экспрессии нескольких генов, кодирующих цитокины и хемокины, таких как IL1B , IL8 , TNF , CCL3 и CCL4 (рис. 3b). ). Кроме того, мы наблюдали повышенный уровень экспрессии IFIh2 в moMa, nrMa и CD11c_mDC у детей, инфицированных SARS-CoV-2, и значительное увеличение TLR2 в moMa и nrMa на ранней стадии инфекции, что позволяет предположить, что эти клетки могут играть дополнительную роль в восприятии вируса и продукции IFN. Это дополнительно подчеркивается тем фактом, что moMa, nrMa и CD11c_mDC у детей, отрицательных по отношению к SARS-CoV-2, экспрессировали IFIh2 и TLR2 на более высоких уровнях, чем у взрослых.
Это дополнительно подчеркивается тем фактом, что moMa, nrMa и CD11c_mDC у детей, отрицательных по отношению к SARS-CoV-2, экспрессировали IFIh2 и TLR2 на более высоких уровнях, чем у взрослых.
a , Тепловые карты, изображающие межклеточные связи между всеми идентифицированными типами клеток, полученные на основе подсчета взаимодействия лиганд-рецептор в линейном масштабе у детей (слева, n = 18 SARS-CoV-2 отрицательных, n = 11 SARS-CoV-2 положительных в ранней фазе инфекции (dps ≤ 4), n = 11 SARS-CoV-2 положительных в поздней фазе инфекции (dps 5– 12)) и взрослых (справа, n = 23 отрицательных на SARS-CoV-2, n = 13 положительных на SARS-CoV-2 на ранней стадии инфекции, n = 8 положительных на SARS-CoV-2 на поздней фазе инфекции) . b , Точечные диаграммы, изображающие экспрессию генов, участвующих в противовирусном и цитотоксическом ответе миелоидных дендритных клеток и различных популяций макрофагов. Каждое значительное увеличение по сравнению с SARS-CoV-2-отрицательными детьми ( n = 18) с SARS-CoV-2-негативными взрослыми ( n = 23) и SARS-CoV-2-позитивными детьми в раннем ( n = 11) или позднем ( n 1)= Фаза инфекции SARS-CoV-2-позитивными взрослыми среди ранней ( n = 13) или поздней ( n = 8) фазы инфекции, соответственно, отмечена красным кружком (двухсторонний скорректированный по Бенджамини-Хохбергу Wilcoxon, P < 0,05). Ave.exp., средняя экспрессия гена; Процент exp., процент клеток, экспрессирующих ген. c , UMAP, демонстрирующий различные субпопуляции T/NK-клеток в носу у детей и взрослых. Для сравнения показаны масштабированные графики плотности, показывающие долю различных T/NK-клеток у детей и взрослых, разделенных их статусом инфекции SARS-CoV-2. Желтый представляет высокую плотность; синий представляет низкую плотность. d , Скрипичные графики, показывающие экспрессию репрезентативных иммунных медиаторов субпопуляции CTL2, сравнивающие SARS-CoV-2-отрицательных детей ( n = 18) с SARS-CoV-2-отрицательными взрослыми ( n = 23) и SARS-CoV-2-позитивных детей на ранней ( n = 11) или поздней ( n = 11) фазе инфицирования SARS-CoV-2-позитивными взрослыми на ранней ( n = 13) или поздняя ( n = 8) фаза инфекции соответственно.
Каждое значительное увеличение по сравнению с SARS-CoV-2-отрицательными детьми ( n = 18) с SARS-CoV-2-негативными взрослыми ( n = 23) и SARS-CoV-2-позитивными детьми в раннем ( n = 11) или позднем ( n 1)= Фаза инфекции SARS-CoV-2-позитивными взрослыми среди ранней ( n = 13) или поздней ( n = 8) фазы инфекции, соответственно, отмечена красным кружком (двухсторонний скорректированный по Бенджамини-Хохбергу Wilcoxon, P < 0,05). Ave.exp., средняя экспрессия гена; Процент exp., процент клеток, экспрессирующих ген. c , UMAP, демонстрирующий различные субпопуляции T/NK-клеток в носу у детей и взрослых. Для сравнения показаны масштабированные графики плотности, показывающие долю различных T/NK-клеток у детей и взрослых, разделенных их статусом инфекции SARS-CoV-2. Желтый представляет высокую плотность; синий представляет низкую плотность. d , Скрипичные графики, показывающие экспрессию репрезентативных иммунных медиаторов субпопуляции CTL2, сравнивающие SARS-CoV-2-отрицательных детей ( n = 18) с SARS-CoV-2-отрицательными взрослыми ( n = 23) и SARS-CoV-2-позитивных детей на ранней ( n = 11) или поздней ( n = 11) фазе инфицирования SARS-CoV-2-позитивными взрослыми на ранней ( n = 13) или поздняя ( n = 8) фаза инфекции соответственно. Каждая точка представляет одну ячейку. Графики показывают медиана, *** P <0,001 ( IFNG Отрицательный: 1,50 × 10 -17 , IFNG Ранняя фаза: 1,14 × 10 -47 , IFN Поздняя фаза: 1.69 -47 , IFN × 10 −27 , CCL5 отрицательный: 5,97 × 10 −30 , CCL5 поздняя фаза: 6,32 × 10 −73 ), получено из двустороннего сравнения Wilcon.
Каждая точка представляет одну ячейку. Графики показывают медиана, *** P <0,001 ( IFNG Отрицательный: 1,50 × 10 -17 , IFNG Ранняя фаза: 1,14 × 10 -47 , IFN Поздняя фаза: 1.69 -47 , IFN × 10 −27 , CCL5 отрицательный: 5,97 × 10 −30 , CCL5 поздняя фаза: 6,32 × 10 −73 ), получено из двустороннего сравнения Wilcon.
Изображение полного размера
Различные субпопуляции иммунных клеток у детей
Помимо повышенной клеточной внутренней противовирусной способности эпителиальных клеток дыхательных путей, макрофагов и дендритных клеток, мы обнаружили специфические закономерности субпопуляций иммунных клеток у детей по сравнению со взрослыми. Среди прочих мы выделили субпопуляцию из KLRC1 (NKG2A) + цитотоксических Т-клеток (CTL2), встречающихся преимущественно у детей (рис. 3c). NKG2A представляет собой лектиноподобный ингибирующий рецептор цитотоксических Т-клеток, играющий роль в ограничении чрезмерной активации, предотвращении апоптоза и поддержании вирусспецифического ответа CD8 + Т-клеток 21 . Уже без вирусной инфекции эта подгруппа цитотоксических Т-клеток CD8 характеризовалась высоким уровнем экспрессии цитотоксических медиаторов (рис. 3d, расширенные данные, рис. 4 и дополнительная таблица 5). Кроме того, IFNG был высоко экспрессирован в этих клетках при сравнении детей, не инфицированных SARS-CoV-2, и взрослых. При заражении дети характеризовались достоверно более высоким уровнем экспрессии IFNG по сравнению со взрослыми как в ранней, так и в поздней фазе инфекции. Точно так же мощный хемоаттрактантный ген CCL5 был увеличен у детей по сравнению со взрослыми с инфекцией или без нее (рис. 3d). Цитотоксический потенциал и преобладание этого подмножества цитотоксических Т-клеток, необходимых для эффективного уничтожения инфицированных вирусом клеток, является дополнительным доказательством лучшего противовирусного ответа у детей по сравнению со взрослыми. Кроме того, у детей, инфицированных SARS-CoV-2, были обнаружены отчетливые CD8 9Популяция Т-клеток 0017 + (CD8_T m ) с фенотипом памяти, который почти отсутствовал у взрослых (рис.
Уже без вирусной инфекции эта подгруппа цитотоксических Т-клеток CD8 характеризовалась высоким уровнем экспрессии цитотоксических медиаторов (рис. 3d, расширенные данные, рис. 4 и дополнительная таблица 5). Кроме того, IFNG был высоко экспрессирован в этих клетках при сравнении детей, не инфицированных SARS-CoV-2, и взрослых. При заражении дети характеризовались достоверно более высоким уровнем экспрессии IFNG по сравнению со взрослыми как в ранней, так и в поздней фазе инфекции. Точно так же мощный хемоаттрактантный ген CCL5 был увеличен у детей по сравнению со взрослыми с инфекцией или без нее (рис. 3d). Цитотоксический потенциал и преобладание этого подмножества цитотоксических Т-клеток, необходимых для эффективного уничтожения инфицированных вирусом клеток, является дополнительным доказательством лучшего противовирусного ответа у детей по сравнению со взрослыми. Кроме того, у детей, инфицированных SARS-CoV-2, были обнаружены отчетливые CD8 9Популяция Т-клеток 0017 + (CD8_T m ) с фенотипом памяти, который почти отсутствовал у взрослых (рис. 3c, EDF4). Остается неясным, полезны ли эти клетки для защиты детей от повторного заражения в будущем.
3c, EDF4). Остается неясным, полезны ли эти клетки для защиты детей от повторного заражения в будущем.
Обсуждение
Наши данные четко свидетельствуют о том, что эпителиальные и иммунные клетки верхних дыхательных путей (носа) детей предварительно активированы и подготовлены к восприятию вирусов. Вероятно, это общая черта детского иммунного ответа слизистых оболочек, но она имеет особое значение для SARS-CoV-2. Совсем недавно scRNA-seq фибробластов, инфицированных вирусом Чикунгунья, показало чрезвычайно узкое окно возможностей для клеток экспрессировать IFN до того, как производство вирусного белка отключит противовирусную систему 22 . Это, вероятно, также объясняет различия между SARS-CoV-2 и другими респираторными вирусами, включая респираторно-синцитиальный вирус, вирус гриппа A или SARS-CoV, с точки зрения индуцированного ответа хозяина. SARS-CoV-2 характеризуется обширной внутриклеточной репликацией и поразительным отсутствием продукции и секреции IFN. С другой стороны, SARS-CoV-2 очень чувствителен к лечению интерферонами до или после заражения, как показано в эпителиальных клетках легких, даже более чувствителен, чем SARS-CoV 9.0017 20,23 . Первичное распознавание вируса и предварительно активированный врожденный иммунный ответ у детей приводят к эффективной ранней продукции IFN в инфицированных дыхательных путях, что, вероятно, опосредует существенные противовирусные эффекты, отражающие наблюдаемые in vitro в клетках, обработанных IFN (предварительно). В конечном итоге это может привести к снижению репликации вируса и более быстрой элиминации у детей. На самом деле, несколько исследований уже показали, что дети намного быстрее уничтожают SARS-CoV-2 по сравнению со взрослыми, что согласуется с концепцией, согласно которой они останавливают репликацию вируса раньше 9.0017 24,25,26,27 . Для других респираторных вирусов, таких как респираторно-синцитиальный вирус и вирус гриппа А, которые сами по себе более эффективно индуцируют IFN-ответ, предварительно активированный врожденный иммунный ответ может быть менее актуальным.
С другой стороны, SARS-CoV-2 очень чувствителен к лечению интерферонами до или после заражения, как показано в эпителиальных клетках легких, даже более чувствителен, чем SARS-CoV 9.0017 20,23 . Первичное распознавание вируса и предварительно активированный врожденный иммунный ответ у детей приводят к эффективной ранней продукции IFN в инфицированных дыхательных путях, что, вероятно, опосредует существенные противовирусные эффекты, отражающие наблюдаемые in vitro в клетках, обработанных IFN (предварительно). В конечном итоге это может привести к снижению репликации вируса и более быстрой элиминации у детей. На самом деле, несколько исследований уже показали, что дети намного быстрее уничтожают SARS-CoV-2 по сравнению со взрослыми, что согласуется с концепцией, согласно которой они останавливают репликацию вируса раньше 9.0017 24,25,26,27 . Для других респираторных вирусов, таких как респираторно-синцитиальный вирус и вирус гриппа А, которые сами по себе более эффективно индуцируют IFN-ответ, предварительно активированный врожденный иммунный ответ может быть менее актуальным. Повышенная врожденная противовирусная способность у детей вместе с высокой чувствительностью SARS-CoV-2 к ИФН может объяснить, почему дети лучше контролируют раннюю стадию инфекции по сравнению со взрослыми и, следовательно, имеют более низкий риск развития тяжелой формы COVID-19.
Повышенная врожденная противовирусная способность у детей вместе с высокой чувствительностью SARS-CoV-2 к ИФН может объяснить, почему дети лучше контролируют раннюю стадию инфекции по сравнению со взрослыми и, следовательно, имеют более низкий риск развития тяжелой формы COVID-19.
Методы
Набор пациентов и одобрение этики
В это исследование были включены лица из трех разных когорт. Пациенты проспективного обсервационного когортного исследования Pa-COVID-19 (ссылка 28 ) и его исследовательской группы RECAST (Понимание повышенной устойчивости детей по сравнению со взрослыми к инфекции SARS-CoV-2) были включены в период с августа 2020 г. по июнь 2021 г. в Charité – Universitätsmedizin Berlin. Дальнейшие пациенты были набраны в проспективном исследовании SC2-Study 9.0017 8,9 в Университетской клинике Лейпцига в период с марта 2020 г. по май 2021 г. Перед включением все пациенты и/или их родители дали письменное информированное согласие. Все три исследования были проведены в соответствии с Хельсинкской декларацией и одобрены соответствующими институциональными наблюдательными советами (Pa-COVID-19/RECAST: EA2/066/20, SC2: 123/20-ek).
Когорта пациентов
Из трех когорт пациенты, классифицированные как бессимптомные, легкие или среднетяжелые на основании рекомендаций ВОЗ 29 пациентов с тяжелым течением COVID-19. В общей сложности мы проанализировали мазки из носа 45 подтвержденных SARS-CoV-2-положительных пациентов, в том числе 24 детей в возрасте от 4 недель до 17 лет (средний возраст 9,0 ± 5,6 лет, 10 женщин, 14 мужчин) и 21 взрослого в возрасте от 21 до 18 лет. и 76 лет (медиана возраста 39,0 ± 10,4 года, 12 женщин, 9 мужчин). Никто из детей не был госпитализирован, но все находились на домашнем карантине. Кроме того, мазки из носа 42 здоровых, SARS-CoV-2-негативных контрольных лиц от 18 детей в возрасте от 4 до 16 лет (средний возраст 9 лет).0,0 ± 3,8 года, 8 женщин, 10 мужчин) и от 23 взрослых в возрасте от 24 до 77 лет (средний возраст 46,0 ± 16,3 года, 13 женщин, 10 мужчин; дополнительные таблицы 3 и 4). Все отрицательные контроли были исследованы на возможное воздействие SARS-CoV-2 путем подробного анамнеза. В случаях известного контакта с SARS-CoV-2 дополнительные серологические тесты проводились во время отбора проб и через 14 дней или проводились последующие опросы, чтобы убедиться, что у участников, а также членов их домохозяйств не было признаков инфекции в течение не менее двух недель подряд и что любые обычные тесты дали отрицательные результаты.
В случаях известного контакта с SARS-CoV-2 дополнительные серологические тесты проводились во время отбора проб и через 14 дней или проводились последующие опросы, чтобы убедиться, что у участников, а также членов их домохозяйств не было признаков инфекции в течение не менее двух недель подряд и что любые обычные тесты дали отрицательные результаты.
ПЦР в реальном времени для SARS-CoV-2
РНК экстрагировали с использованием набора MagNA Pure 96 DNA and Viral NA Small Volume Kit (Roche) на системе MagNA Pure 96 в соответствии с рекомендациями производителя. ПЦР в реальном времени с обратной транскрипцией была проведена для гена оболочки (E) и гена нуклеокапсида (N) на системе Roche Light Cycler 480 (Tib-Molbiol).
Получение суспензии одиночных клеток из мазков из носа человека, подготовка к scRNA-seq и последующая предварительная обработка исходных данных
Обработка образцов, подготовка отдельных клеток и библиотек, а также анализ данных выполнялись, как описано ранее 8,9 . Вкратце, свежие мазки из носоглотки переносили в холодную среду DMEM/F12 (Gibco, 11039) и в течение 1 часа подвергали дальнейшей обработке. В соответствии с биобезопасностью S2 к каждому образцу добавляли равный объем 13 мМ дитиотреитола (AppliChem, A2948). Для достижения большего числа клеток раствор медленно пипетировали вверх и вниз, а тампон погружали в среду примерно 20 раз. После инкубации при 37°С и 500 об/мин. в течение 10 мин на термомиксере, образцы центрифугировали при 350 град.0005 г при 4 °C в течение 5 мин и надосадочную жидкость медленно удаляли. Если осадок показывал какие-либо признаки эритроцитов, его ресуспендировали в 1× PBS (Sigma-Aldrich, D8537), обрабатывали буфером для лизиса эритроцитов (Roche, 11814389001) при 25 °C в течение 10 минут и центрифугировали при 350°С . г при 4 °C в течение 5 мин. Если образцы не обрабатывались немедленно, клеточный осадок ресуспендировали в среде DMEM/F12 с добавлением 20% FBS (Gibco, 10500) и 10% диметилсульфоксида (Sigma-Aldrich, D8418) и замораживали при -80 °C.
Вкратце, свежие мазки из носоглотки переносили в холодную среду DMEM/F12 (Gibco, 11039) и в течение 1 часа подвергали дальнейшей обработке. В соответствии с биобезопасностью S2 к каждому образцу добавляли равный объем 13 мМ дитиотреитола (AppliChem, A2948). Для достижения большего числа клеток раствор медленно пипетировали вверх и вниз, а тампон погружали в среду примерно 20 раз. После инкубации при 37°С и 500 об/мин. в течение 10 мин на термомиксере, образцы центрифугировали при 350 град.0005 г при 4 °C в течение 5 мин и надосадочную жидкость медленно удаляли. Если осадок показывал какие-либо признаки эритроцитов, его ресуспендировали в 1× PBS (Sigma-Aldrich, D8537), обрабатывали буфером для лизиса эритроцитов (Roche, 11814389001) при 25 °C в течение 10 минут и центрифугировали при 350°С . г при 4 °C в течение 5 мин. Если образцы не обрабатывались немедленно, клеточный осадок ресуспендировали в среде DMEM/F12 с добавлением 20% FBS (Gibco, 10500) и 10% диметилсульфоксида (Sigma-Aldrich, D8418) и замораживали при -80 °C. Для препаратов библиотек клетки размораживали при 37°С, центрифугировали при 350°С.0005 г при 4 °C в течение 5 мин и далее обрабатывали в соответствии с протоколом. Для получения суспензии одиночных клеток к осадку добавляли Accutase (Thermo Fisher, 00-4555-56) и раствор инкубировали при комнатной температуре в течение 10 мин с осторожным пипетированием клеток через 5 мин. Инкубацию останавливали добавлением DMEM/F12 с добавлением 10% FBS и центрифугированием при 350 g при 4°С в течение 5 мин. Затем супернатант удаляли, а клеточный осадок ресуспендировали в 1× PBS (объем доводили до размера клеточного осадка). Суспензию очищали от любого клеточного детрита с помощью клеточного фильтра 35 мкм (Falcon, 352235), а затем клетки подсчитывали с помощью одноразовой камеры Нойбауэра (NanoEnTek, DHC-N01). Клеточную суспензию разбавляли, чтобы обеспечить загрузку 17 500 клеток на образец. Одноклеточная и уникальная эмульсия штрих-кода была получена путем смешивания разведенных клеток с мастер-миксом и загрузки их на чип вместе с гелевыми шариками и разделяющим маслом с использованием набора 10x Genomics Single Cell 3ʹ GEM, Library and Gel Bead Kit v3.
Для препаратов библиотек клетки размораживали при 37°С, центрифугировали при 350°С.0005 г при 4 °C в течение 5 мин и далее обрабатывали в соответствии с протоколом. Для получения суспензии одиночных клеток к осадку добавляли Accutase (Thermo Fisher, 00-4555-56) и раствор инкубировали при комнатной температуре в течение 10 мин с осторожным пипетированием клеток через 5 мин. Инкубацию останавливали добавлением DMEM/F12 с добавлением 10% FBS и центрифугированием при 350 g при 4°С в течение 5 мин. Затем супернатант удаляли, а клеточный осадок ресуспендировали в 1× PBS (объем доводили до размера клеточного осадка). Суспензию очищали от любого клеточного детрита с помощью клеточного фильтра 35 мкм (Falcon, 352235), а затем клетки подсчитывали с помощью одноразовой камеры Нойбауэра (NanoEnTek, DHC-N01). Клеточную суспензию разбавляли, чтобы обеспечить загрузку 17 500 клеток на образец. Одноклеточная и уникальная эмульсия штрих-кода была получена путем смешивания разведенных клеток с мастер-миксом и загрузки их на чип вместе с гелевыми шариками и разделяющим маслом с использованием набора 10x Genomics Single Cell 3ʹ GEM, Library and Gel Bead Kit v3. 1. (10x Genomics; PN 1000120; PN 1000121; PN 1000213) и загрузить чип в 10x Chromium Controller. Последующую обратную транскрипцию, очистку и амплификацию кДНК, а также подготовку библиотеки проводили в соответствии с руководством производителя. Примечательно, что для того, чтобы убедиться, что вирус инактивирован, мы продлили инкубацию при 85 °C во время обратной транскрипции до 10 мин. Окончательные библиотеки 3’ РНК объединяли для секвенирования в проточной кювете S2 или S4 (S2: до 13 образцов, S4: до 24 образцов) и секвенировали в системе секвенирования NovaSeq 6000 (Illumina, парный конец, одинарная индексация). .
1. (10x Genomics; PN 1000120; PN 1000121; PN 1000213) и загрузить чип в 10x Chromium Controller. Последующую обратную транскрипцию, очистку и амплификацию кДНК, а также подготовку библиотеки проводили в соответствии с руководством производителя. Примечательно, что для того, чтобы убедиться, что вирус инактивирован, мы продлили инкубацию при 85 °C во время обратной транскрипции до 10 мин. Окончательные библиотеки 3’ РНК объединяли для секвенирования в проточной кювете S2 или S4 (S2: до 13 образцов, S4: до 24 образцов) и секвенировали в системе секвенирования NovaSeq 6000 (Illumina, парный конец, одинарная индексация). .
Наборы данных с одной ячейкой были выровнены и предварительно обработаны с помощью Cellranger 3.0.1. Был использован пользовательский эталонный геном hg19 человека (10x Genomics, версия 3.1.0) с геномом SARS-CoV-2 (Refseq-ID: NC_045512), добавленным в качестве дополнительной хромосомы. Для последующего анализа использовали Seurat 3.2.2. Клетки с менее чем 3 генами и клетки с более чем или равным 15% митохондриальных прочтений или менее чем с 200 экспрессированными генами отбрасывали. Чтобы удалить дублеты, пороговое значение количества уникальных молекулярных идентификаторов и генов было определено вручную для каждого образца.
Чтобы удалить дублеты, пороговое значение количества уникальных молекулярных идентификаторов и генов было определено вручную для каждого образца.
Образцы были объединены и экспортированы в виде CSV-файлов, содержащих счетчики и метаданные, и импортированы в scanpy 1.6.0 30 . После нормализации до 10 000 прочтений на клетку значения экспрессии были логарифмически преобразованы и были рассчитаны высоковариабельные гены, которые использовались в качестве основы для следующих этапов предварительной обработки. Данные были масштабированы, PCA преобразованы и выровнены с использованием гармонии 0.0.5 (ссылка 31 ) на основе 100 основных компонентов. Дальнейшее выравнивание было выполнено с использованием bbknn 1.4.0 (ссылка 32 ) на основе 50 предварительно выровненных основных компонентов, 10 деревьев, 3 соседей в пакете и настройки обрезки 85. На основе интегрированных данных было выполнено встраивание UMAP и кластеризация Leiden 33 . Эта кластеризация была использована в качестве основы для субкластеризации популяций иммунных и эпителиальных клеток с использованием того же алгоритма. Кластеры популяций эпителиальных 34,35,36 и иммунных 37,38,39 клеток были отнесены к типам/стадиям клеток в соответствии с уровнем экспрессии различных маркерных генов (расширенные данные, рис. 1 и 4). Кластеры Т-клеток и макрофагов/дендритных клеток были разделены на подкластеры, а затем дополнительно уточнены вручную.
Эта кластеризация была использована в качестве основы для субкластеризации популяций иммунных и эпителиальных клеток с использованием того же алгоритма. Кластеры популяций эпителиальных 34,35,36 и иммунных 37,38,39 клеток были отнесены к типам/стадиям клеток в соответствии с уровнем экспрессии различных маркерных генов (расширенные данные, рис. 1 и 4). Кластеры Т-клеток и макрофагов/дендритных клеток были разделены на подкластеры, а затем дополнительно уточнены вручную.
Объект был сохранен как h5ad, преобразован в h5seurat с помощью SeuratDisk версии 0.0.0.9014 и импортирован обратно в R версии 4.1.0.
Всего в набор данных было включено 268 745 ячеек. Количество клеток между группами было одинаково распределено (отрицательные дети 51 595; отрицательные взрослые 62 701; положительные взрослые 51 500), за исключением группы положительных детей, содержащих большее количество клеток (102 949). Различные образцы содержали разное количество клеток. Проценты вклада каждой выборки в свою изучаемую группу сравнивали с помощью теста Крускала-Уоллиса, который не выявил существенных различий между группами (9). 0005 P = 0,2).
0005 P = 0,2).
Чтобы обеспечить визуальное сравнение между UMAP разных групп, было случайным образом выбрано равное количество клеток (45 000) в каждой группе с использованием функции SubsetData в Seurat.
Предполагаемые межклеточные взаимодействия были количественно оценены с использованием CellPhoneDB версии 2.1.2 с настройками по умолчанию 40 . Чтобы уменьшить влияние отдельных выборок, дающих большее количество ячеек, и ускорить вычисления, мы ограничили количество ячеек в выборке до 2000 случайно выбранных ячеек. Это было сделано с помощью функции SubsetData в Seurat.
Идентификация набора генов ISG
Для анализа ответов PRR/IFN был собран набор генов наиболее известных ISG, экспрессируемых эпителиальными клетками легких. Как описано ранее 9 , мы обработали эпителиальные клетки A549 смесью IFNβ и IFNλ в течение 2, 8 или 24 часов и проанализировали уровни транскриптов с помощью анализа микрочипов с использованием платформы Illumina Human HT-12 v3 Expression Beadchip в области геномики и протеомики. основной объект на ДКФЗ. Мы идентифицировали ISG как проявляющие логарифм 9.0443 2 [кратное изменение] > 0,8 в любой момент времени, что дает 183 гена. Мы также включили ISG, которые, как описано, проявляют сильную активность против SARS-CoV-2 19 (65 генов с наивысшим баллом), если они еще не включены в наш список. В конечном итоге это привело к набору генов из 217 генов, также экспрессированных в нашей scRNA-seq.
основной объект на ДКФЗ. Мы идентифицировали ISG как проявляющие логарифм 9.0443 2 [кратное изменение] > 0,8 в любой момент времени, что дает 183 гена. Мы также включили ISG, которые, как описано, проявляют сильную активность против SARS-CoV-2 19 (65 генов с наивысшим баллом), если они еще не включены в наш список. В конечном итоге это привело к набору генов из 217 генов, также экспрессированных в нашей scRNA-seq.
Инфицирование SARS-CoV-2 клеток A549, экспрессирующих MDA5
Клетки A549, стабильно трансдуцированные лентивирусным вектором, экспрессирующим человеческий IFIh2 , под контролем промотора мышиной ROSA26 (обозначается A549MDA5 high на рис. 2e) были предоставлены Надин Гиллих и Ральфом Бартеншлагером. Мы трансдуцировали клетки A549 (обозначенные как MDA5 low ) и A549 MDA5 high с использованием лентивирусных векторов, кодирующих ACE2 и TMPRSS2 человека, чтобы сделать их пригодными для инфекции SARS-CoV-2; чтобы обеспечить постоянную экспрессию ACE2 / TMPRSS2 в экспериментах, трансдукцию проводили заново за 24 часа до заражения клеток. Инфицирование SARS-CoV-2 (штамм BetaCoV/Германия/BavPat1/2020) проводили в нашем центре BSL3 при множественности заражения 0,1, а клетки собирали через 24 часа после заражения. РНК экстрагировали с использованием набора Monarch Total RNA Miniprep Kit (New England Biolabs) и подвергали обратной транскрипции с помощью набора для обратной транскрипции кДНК High Capacity (Thermo Fisher Scientific). Уровни транскриптов IFNB1 и ISG затем оценивали с помощью ПЦР в реальном времени с использованием iTaq Universal SYBR Green Supermix (BioRad) на системе обнаружения ПЦР в реальном времени BioRad CFX96. Данные представлены как среднее ± sem. из трех биологически независимых повторностей.
Инфицирование SARS-CoV-2 (штамм BetaCoV/Германия/BavPat1/2020) проводили в нашем центре BSL3 при множественности заражения 0,1, а клетки собирали через 24 часа после заражения. РНК экстрагировали с использованием набора Monarch Total RNA Miniprep Kit (New England Biolabs) и подвергали обратной транскрипции с помощью набора для обратной транскрипции кДНК High Capacity (Thermo Fisher Scientific). Уровни транскриптов IFNB1 и ISG затем оценивали с помощью ПЦР в реальном времени с использованием iTaq Universal SYBR Green Supermix (BioRad) на системе обнаружения ПЦР в реальном времени BioRad CFX96. Данные представлены как среднее ± sem. из трех биологически независимых повторностей.
Статистика
Дифференциальная экспрессия генов была рассчитана с использованием rank_genes_groups() в Scanpy версии 1.6.0 и с поправкой на ложные показатели обнаружения с помощью statsmodels версии 0.9.0 (ссылка 41 ). Различия в составе клеток типа/стадии оценивали с использованием критерия суммы рангов Крускала-Уоллиса с последующим двусторонним апостериорным критерием Данна. Зависимости от возраста были рассчитаны в соответствии с моделью линейной регрессии с поправкой на COVID-19.состояние и корректировка значений F -test P с использованием метода Бенджамини-Хохберга 42 .
Зависимости от возраста были рассчитаны в соответствии с моделью линейной регрессии с поправкой на COVID-19.состояние и корректировка значений F -test P с использованием метода Бенджамини-Хохберга 42 .
P значения для точечных диаграмм и диаграмм скрипки были рассчитаны с использованием функции Сёра FindMarkers() на основе критерия Уилкоксона и скорректированы с помощью метода Бенджамини-Хохберга 42 .
Чтобы проверить, значительно ли повышаются уровни MDA5 и RIG-I в клетках A549 под действием IFNB1 и индукции ISG при инфицировании, непарный однохвостый студент 9Был проведен тест 0005 t- из трех биологически независимых повторений (GraphPad Prism v9.1).
Сводка отчетов
Дополнительную информацию о дизайне исследования можно найти в Сводке отчетов об исследованиях природы, связанной с этой статьей.
Доступность данных
Обработанные данные в виде объекта Seurat доступны без ограничений доступа на FigShare (https://doi. org/10.6084/m9.figshare.14938755). Этот набор данных можно использовать для повторения и расширения анализа, представленного в этой статье. Из-за потенциального риска деидентификации псевдонимизированных данных РНК-секвенирования необработанные данные секвенирования могут быть получены через EGA (EGAS00001005461) только для некоммерческих исследовательских целей при условии контролируемого доступа в соответствии с требованиями законов ЕС о защите данных. Для доступа свяжитесь с соответствующим автором, Р.Е. Кроме того, эти данные могут быть дополнительно визуализированы и проанализированы в Magellan COVID-19.обозреватель данных на https://digital.bihealth.org.
org/10.6084/m9.figshare.14938755). Этот набор данных можно использовать для повторения и расширения анализа, представленного в этой статье. Из-за потенциального риска деидентификации псевдонимизированных данных РНК-секвенирования необработанные данные секвенирования могут быть получены через EGA (EGAS00001005461) только для некоммерческих исследовательских целей при условии контролируемого доступа в соответствии с требованиями законов ЕС о защите данных. Для доступа свяжитесь с соответствующим автором, Р.Е. Кроме того, эти данные могут быть дополнительно визуализированы и проанализированы в Magellan COVID-19.обозреватель данных на https://digital.bihealth.org.
Ссылки
Castagnoli, R. et al. Тяжелый острый респираторный синдром коронавирусной инфекции 2 (SARS-CoV-2) у детей и подростков: систематический обзор. JAMA Педиатр. 174 , 882–889 (2020).
Артикул пабмед Google ученый
“>О’Дрисколл, М. и др. Возрастные характеристики смертности и иммунитета при SARS-CoV-2. Природа 590 , 140–145 (2021).
Артикул пабмед Google ученый
Park, A. & Iwasaki, A. Интерфероны типа I и типа III – индукция, сигнализация, уклонение и применение для борьбы с COVID-19. Микроб-хозяин клетки 27 , 870–878 (2020).
КАС Статья пабмед ПабМед Центральный Google ученый
Pierce, C.A. et al. Естественные слизистые барьеры и COVID-19 у детей. JCI Insight 6 , e148694 (2021).

Артикул ПабМед Центральный Google ученый
Йошида, М. и др. Местный и системный ответ на инфекцию SARS-CoV-2 у детей и взрослых. Препринт в medRxiv https://doi.org/10.1101/2021.03.09.21253012 (2021).
Hou, Y.J. et al. Обратная генетика SARS-CoV-2 выявляет переменный градиент инфекции в дыхательных путях. Cell 182 , 429–446 (2020).
КАС Статья пабмед ПабМед Центральный Google ученый
Chua, R.L. et al. Тяжесть COVID-19 коррелирует с взаимодействиями эпителия дыхательных путей с иммунными клетками, выявленными с помощью анализа отдельных клеток. Нац. Биотехнолог. 38 , 970–979 (2020).
КАС пабмед Google ученый
Трамп, С. и др. Гипертония задерживает клиренс вируса и усугубляет гипервоспаление дыхательных путей у пациентов с COVID-19.
 Нац. Биотехнолог. (2020).
Нац. Биотехнолог. (2020).Koch, C.M. et al. Иммунный ответ на SARS-CoV-2 в слизистой оболочке носа у детей и взрослых. Препринт на medRxiv https://doi.org/10.1101/2021.01.26.21250269(2021).
В’Ковски П., Кратцель А., Штайнер С., Штальдер Х. и Тиль В. Биология и репликация коронавируса: значение для SARS-CoV-2. Нац. Преподобный Микробиолог. 19 , 155–170 (2021).
Артикул пабмед Google ученый
Wolfel, R. et al. Вирусологическая оценка госпитализированных пациентов с COVID-2019. Природа 581 , 465–469 (2020).
Артикул пабмед Google ученый
Ребенден, А. и др. SARS-CoV-2 запускает MDA-5-зависимый интерфероновый ответ, который не может контролировать репликацию в эпителиальных клетках легких.
 Дж. Вирол. 95 , e02415–e02420 (2021 г.).
Дж. Вирол. 95 , e02415–e02420 (2021 г.).КАС Статья ПабМед Центральный Google ученый
Инь, X. и др. MDA5 регулирует врожденный иммунный ответ на SARS-CoV-2 в эпителиальных клетках легких. Cell Rep. 34 , 108628 (2021).
КАС Статья пабмед ПабМед Центральный Google ученый
Брунс, А. М., Лезер, Г. П., Лэмб, Р. А. и Хорват, К. М. Сенсор врожденного иммунитета LGP2 активирует противовирусную сигнализацию, регулируя взаимодействие MDA5-РНК и сборку филаментов. мол. Cell 55 , 771–781 (2014).
КАС Статья пабмед ПабМед Центральный Google ученый
Zhang, Q. et al. Врожденные ошибки иммунитета к IFN I типа у пациентов с опасным для жизни COVID-19. Наука 370 , eabd4570 (2020).

КАС Статья пабмед ПабМед Центральный Google ученый
Bastard, P. et al. Аутоантитела к интерферонам I типа могут быть причиной побочных реакций на живую аттенуированную вакцину против желтой лихорадки. Дж. Экспл. Мед. 218 , e20202486 (2021).
КАС Статья пабмед ПабМед Центральный Google ученый
Pfaender, S. et al. LY6E нарушает слияние коронавируса и обеспечивает иммунный контроль над вирусным заболеванием. Нац. микробиол. 5 , 13:30–1339 (2020).
КАС Статья пабмед ПабМед Центральный Google ученый
Martin-Sancho, L. et al. Функциональный ландшафт клеточной рестрикции SARS-CoV-2. мол. Ячейка 81 , 2656–2668.e8 (2021).
КАС Статья пабмед ПабМед Центральный Google ученый
“>Rapaport, A. S. et al. Ингибирующий рецептор NKG2A поддерживает вирусспецифические CD8 + Т-клетки в ответ на летальную поксвирусную инфекцию. Иммунитет 43 , 1112–1124 (2015).
КАС Статья пабмед ПабМед Центральный Google ученый
Pott, F. et al. Одноклеточный транскриптомный анализ противовирусных ответов и вирусного антагонизма в синовиальных фибробластах, инфицированных вирусом Чикунгунья. Препринт в bioRxiv https://doi.org/10.1101/2020.06.07.138610 (2021).
Lokugamage, K.
 G. et al. Чувствительность к интерферону типа I отличает SARS-CoV-2 от SARS-CoV. Дж. Вирол. 94 , e01410-20 (2020).
G. et al. Чувствительность к интерферону типа I отличает SARS-CoV-2 от SARS-CoV. Дж. Вирол. 94 , e01410-20 (2020).Артикул пабмед ПабМед Центральный Google ученый
Dufort, E. M. et al. Мультисистемный воспалительный синдром у детей в штате Нью-Йорк. Н. англ. Дж. Мед. 383 , 347–358 (2020).
КАС Статья пабмед Google ученый
Feldstein, L.R. et al. Мультисистемный воспалительный синдром у детей и подростков в США. Н. англ. Дж. Мед. 383 , 334–346 (2020).
КАС Статья пабмед Google ученый
Weisberg, S.P. et al. Различный ответ антител на SARS-CoV-2 у детей и взрослых во время COVID-19клинический спектр. Нац. Иммунол. 22 , 25–31 (2021).
Артикул пабмед Google ученый
“>Курт, Ф. и др. Изучение патофизиологии коронавирусной болезни 2019: протокол для берлинской когорты предполагаемых пациентов с COVID-19 (Pa-COVID-19). Инфекция 48 , 619–626 (2020).
КАС Статья пабмед ПабМед Центральный Google ученый
Эйлуорд, Б., Лян, В. и Совместная миссия ВОЗ в Китае. Доклад Совместной миссии ВОЗ и Китая по коронавирусной болезни, 2019 г.(COVID-19) (ВОЗ, 2020 г.).
Вольф, Ф. А., Ангерер, П. и Тайс, Ф. Дж. SCANPY: крупномасштабный анализ данных экспрессии генов в одной клетке.
 Геном Биол. 19 , 15 (2018).
Геном Биол. 19 , 15 (2018).Артикул пабмед ПабМед Центральный Google ученый
Корсунский И. и др. Быстрая, чувствительная и точная интеграция данных отдельных ячеек с Harmony. Нац. Методы 16 , 1289–1296 (2019).
КАС пабмед ПабМед Центральный Google ученый
Полански, К. и др. BBKNN: быстрое пакетное выравнивание транскриптомов отдельных клеток. Биоинформатика 36 , 964–965 (2020).
ПабМед Google ученый
Трааг, В. А., Уолтман, Л. и ван Эк, Нью-Джерси. От Лувена до Лейдена: гарантия хорошо связанных сообществ. Науч. Респ. 9 , 5233 (2019).
КАС Статья пабмед ПабМед Центральный Google ученый
“>Plasschaert, L.W. et al. Одноклеточный атлас эпителия дыхательных путей выявляет богатые CFTR легочные ионоциты. Природа 560 , 377–381 (2018).
КАС Статья пабмед ПабМед Центральный Google ученый
Виейра Брага, Ф. А. и др. Клеточная перепись легких человека выявляет новые состояния клеток в норме и при астме. Нац. Мед. 25 , 1153–1163 (2019 г.)).
КАС Статья пабмед Google ученый
Могиленко Д.А. и др. Всестороннее профилирование стареющей иммунной системы выявило клональные GZMK + CD8 + Т-клетки как консервативный признак воспаления.
 Иммунитет 54 , 99–115 (2021).
Иммунитет 54 , 99–115 (2021).КАС Статья пабмед Google ученый
Travaglini, K.J. et al. Атлас молекулярных клеток легкого человека на основе секвенирования одноклеточной РНК. Природа 587 , 619–625 (2020).
КАС Статья пабмед ПабМед Центральный Google ученый
Чжао, С. Т. и Ван, К. З. Регуляторные Т-клетки и астма. J. Zhejiang Univ. науч. B 19 , 663–673 (2018).
КАС Статья пабмед ПабМед Центральный Google ученый
Ефремова, М., Венто-Тормо, М., Тейхманн, С.А. и Венто-Тормо, Р. CellPhoneDB: определение связи между клетками на основе комбинированной экспрессии многосубъединичных комплексов лиганд-рецептор. Нац. протокол 15 , 1484–1506 (2020).

КАС Статья пабмед Google ученый
Сиболд, С. и Перктольд, Дж. Статистические модели: эконометрическое и статистическое моделирование с помощью Python. Проц. 9-я научная конференция Python 57–61 (2010 г.).
Бенджамини Ю. и Хохберг Ю. Контроль уровня ложных открытий: практичный и мощный подход к множественному тестированию. JR Stat. соц. 57 , 289–300 (1995).
Google ученый
Гольдштейн Э., Липсич М. и Чевик М. О влиянии возраста на передачу SARS-CoV-2 в домашнем хозяйстве, школах и обществе. Дж. Заразить. Дис. 223 , 362–369 (2021).
КАС Статья пабмед Google ученый
Хейн, М. и др. Систематический функциональный анализ белков SARS-CoV-2 выявляет вирусные антагонисты врожденного иммунитета и остающиеся уязвимые места. Cell Rep. 35 , 109126 (2021 г.).
КАС Статья пабмед ПабМед Центральный Google ученый
Whittaker, E. et al. Клинические характеристики 58 детей с педиатрическим мультисистемным воспалительным синдромом, временно ассоциированным с SARS-CoV-2. JAMA 324 , 259–269 (2020).
КАС Статья пабмед ПабМед Центральный Google ученый
Lukassen, S. et al. Рецепторы SARS-CoV-2 ACE2 и TMPRSS2 в основном экспрессируются в транзиторных секреторных клетках бронхов. EMBO J. 39 , e105114 (2020).
КАС Статья пабмед ПабМед Центральный Google ученый
Загрузить ссылки
Благодарности
Мы благодарим всех пациентов исследований RECAST, Pa-COVID-19 и SC2 за предоставление носовых образцов и клинических данных. Это исследование было поддержано исследовательской программой BIH COVID-19 и инициативой fightCOVID@DKFZ, Европейской комиссией (ESPACE, 874719, Horizon 2020), Федеральным министерством образования и исследований Германии (BMBF), финансируемой de. NBI Cloud в рамках German Network for Bioinformatics Infrastructure (de.NBI; 031A537B, 031A533A, 031A538A, 031A533B, 031A535A, 031A537C, 031A534A and 031A532B), the BMBF-funded Medical Informatics Initiative (HiGHmed, 01ZZ1802A – 01ZZ1802Z), the BMBF-funded projects 01IK20337 and 82DZL0098B1, Немецкий исследовательский фонд (Deutsche Forschungsgemeinschaft, DFG) профинансировал CRC-TR 84 B08, CRC-1449 Z01 и проект ID 272983813-TRR179, а также проект DFG по целенаправленному финансированию COVID-19 BI1693/2-1. Эта публикация является частью Атласа клеток человека — www.humancellatlas.org/publications.
NBI Cloud в рамках German Network for Bioinformatics Infrastructure (de.NBI; 031A537B, 031A533A, 031A538A, 031A533B, 031A535A, 031A537C, 031A534A and 031A532B), the BMBF-funded Medical Informatics Initiative (HiGHmed, 01ZZ1802A – 01ZZ1802Z), the BMBF-funded projects 01IK20337 and 82DZL0098B1, Немецкий исследовательский фонд (Deutsche Forschungsgemeinschaft, DFG) профинансировал CRC-TR 84 B08, CRC-1449 Z01 и проект ID 272983813-TRR179, а также проект DFG по целенаправленному финансированию COVID-19 BI1693/2-1. Эта публикация является частью Атласа клеток человека — www.humancellatlas.org/publications.
Информация об авторе
Примечания автора
Эти авторы внесли равный вклад: J. Loske, J. Röhmel, S. Lukassen.
Эти авторы совместно руководили этой работой: М. Биндер, С. Трамп, Р. Эйлс, М. А. Молл, И. Леманн.
Авторы и организации
Отделение молекулярной эпидемиологии, Берлинский институт здравоохранения при Charité – Universitätsmedizin Berlin, Берлин, Германия
J.
 Loske, L. Thürmann, M. Messingschlager, Trump, A. Seegebarth & I. Lehmann
Loske, L. Thürmann, M. Messingschlager, Trump, A. Seegebarth & I. LehmannКафедра детской респираторной медицины, иммунологии и реаниматологии, Charité – Universitätsmedizin Berlin, корпоративный член Свободного университета Берлина и Университета Гумбольдта, Берлин, Германия
J. Röhmel, S. Stricker и M. A. Mall
Центр цифрового здравоохранения, Берлинский институт здравоохранения при Charité – Universitätsmedizin Berlin, Берлин, Германия
S. Lukassen, J. Liebig, R.L. Chua, C. Conrad & R. Eils
Исследовательская группа «Динамика ранней вирусной инфекции и врожденный противовирусный ответ», подразделение F170, Немецкий центр исследования рака (DKFZ), Гейдельберг, Германия
V. G. Magalhães и M. Binder
Институт молекулярной генетики им. Макса Планка, Берлин, Германия
Б. Тиммерманн и С. Клагес
Институт биохимии, Charité – Universitätsmedizin Berlin, корпоративный член Свободного университета Берлина и Университета Гумбольдта, Берлин, Берлин Германия
M.
 Ralser
RalserИнститут медицинской иммунологии, Charité – Universitätsmedizin Berlin, корпоративный член Freie Universität Berlin, Humboldt-Universität zu Berlin, Берлин, Германия
B. Sawitzki
Кафедра инфекционных заболеваний и респираторной медицины, Charité – Universitätsmedizin Berlin, корпоративный член Свободного университета Берлина, Humboldt-Universität zu Berlin и Берлинского института здоровья (BIH), Берлин, Германия
L. E. Sander
Немецкий центр исследования легких (DZL), ассоциированный партнер, Берлин, Германия
L. E. Sander, R. Eils, M. A. Mall и I. Lehmann
Институт вирусологии, Charité – Universitätsmedizin Berlin, корпоративный член Свободного университета Берлина, Университета Гумбольдта в Берлине и Берлинского института здравоохранения (БИЗ), Берлин, Германия
В. М. Корман
Немецкий центр исследований инфекций (DZIF), ассоциированный партнер Charité-Universitätsmedizin Berlin, Берлин, Германия
В.
 М. Корман
М. КорманОтделение анестезиологии, Лейцигский университет 0000, Германия
S. Laudi
Charité – Universitätsmedizin Berlin, корпоративный член Freie Universität Berlin, Humboldt-Universität zu Berlin, Берлин, Германия
R. Eils & I. Lehmann
Авторы
- J. Loske
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- J. Röhmel
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- S. Lukassen
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- S. Stricker
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- V.G. Magalhães
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- J.
 Liebig
LiebigПросмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Р. Л. Чуа
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- L. Thürmann
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- M. Messingschlager
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- A. Seegebarth
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- B. Timmermann
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- S. Klages
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- M.
 Ralser
RalserПросмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Б. Савицки
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- L. E. Sander
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- В. М. Корман
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- К. Конрад
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- S. Laudi
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- M. Binder
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- S.
 Trump
TrumpПосмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- R. Eils
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- M. A. Mall
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- I. Lehmann
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
Взносы
С.Т., С. Лукассен, И.Л., М.А.М. и Р.Э. задумал, спроектировал и проконтролировал проект. B.S., M.R., J.R., L.S., V.M.C. и М.А.М. разработал когорту RECAST. Дж.Р., С.С., Л.С. и С. Лауди набрали пациентов и предоставили человеческие образцы, клинические данные и аннотацию пациентов. Дж. Лоске, А.С., Дж. Либих, М.М. и Р.Л.К. проводили эксперименты с скРНК. В.Г.М. и М.Б. провел и проанализировал эксперименты in vitro. Дж. Лоске, Л.Т., С. Лукассен и Р.Л.К. проанализированные данные. Б.С., Л.С., С. Лауди, В.М.К., М.Р., К.С., М.Б. и М.А.М. участвовал в обсуждении результатов. Б.Т. и С.К. оказывали техническую и экспериментальную поддержку. Дж. Лоске, С. Лукассен, С.Т., М.Б., Р.Э. и И.Л. написал рукопись; все авторы прочитали, отредактировали и одобрили рукопись.
Дж. Лоске, Л.Т., С. Лукассен и Р.Л.К. проанализированные данные. Б.С., Л.С., С. Лауди, В.М.К., М.Р., К.С., М.Б. и М.А.М. участвовал в обсуждении результатов. Б.Т. и С.К. оказывали техническую и экспериментальную поддержку. Дж. Лоске, С. Лукассен, С.Т., М.Б., Р.Э. и И.Л. написал рукопись; все авторы прочитали, отредактировали и одобрили рукопись.
Автор, ответственный за переписку
Переписка с Р. Эйлс.
Заявление об этике
Конкурирующие интересы
Авторы не заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Информация о рецензировании Nature Biotechnology благодарит Мелани Ниланд и других анонимных рецензентов за их вклад в рецензирование этой работы.
Примечание издателя Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Расширенные данные
Расширенные данные Рис.
 1. Маркерные гены клеточного типа.
1. Маркерные гены клеточного типа.(a-b) Точечные графики, изображающие среднюю и процентную экспрессию генов, используемых для классификации (a) иммунных и (b) эпителиальных клеток. Процент Exp = процент клеток, экспрессирующих ген, Ave. Exp. = средняя экспрессия гена.
Расширенные данные Рис. 2 Состав клеток у детей и взрослых и экспрессия ACE2.
(a) Распределение всех типов/состояний клеток у детей и взрослых, разделенных статусом инфекции SARS-CoV-2. Приведены проценты от общего числа ячеек. Сравнения по критерию Крускала-Уоллиса с последующим двусторонним апостериорным сравнением Данна (*достоверность сравнения между детьми и взрослыми, P <0,05; нейтрофилы: 5,54E-07, mDC: 1,47E-03, rMa: 3,71E-03, НК: 8.73Э-03, п_НКТ: 4.96E-02, ag_T: 6.09E-04, Treg: 8.50E-03, DNT: 1.62E-04, CD8_Tm: 1.97E-04, IL17A_CD8: 3.05E-04, IL17A_CD4: 2.68E-03, CTL2: 1.83E -05, CTL1: 3.60E-03, Plasma_cell: 1.83E-05, B_cell: 2.45E-03, иммунный_общий: 1. 61E-06, Базальный: 6.96E-05, Cil_diff: 2.35E-03, Cil_acute_phase: 8.92E- 06, Реснитчатые: 9.18E-07, Sec_diff: 5.09E-03). (b) Скрипичные графики показывают распределение экспрессии входного рецептора SARS-CoV-2 ACE2 и экспрессии генов ассоциированных протеаз в эпителиальных клетках детей и взрослых либо с (n=24 детей, n=21 взрослых), либо с без инфекции SARS-CoV-2 (n=18 детей, n=23 взрослых). Графики показывают медиану. Существенных различий не наблюдалось.
61E-06, Базальный: 6.96E-05, Cil_diff: 2.35E-03, Cil_acute_phase: 8.92E- 06, Реснитчатые: 9.18E-07, Sec_diff: 5.09E-03). (b) Скрипичные графики показывают распределение экспрессии входного рецептора SARS-CoV-2 ACE2 и экспрессии генов ассоциированных протеаз в эпителиальных клетках детей и взрослых либо с (n=24 детей, n=21 взрослых), либо с без инфекции SARS-CoV-2 (n=18 детей, n=23 взрослых). Графики показывают медиану. Существенных различий не наблюдалось.
Расширенные данные Рис. 3 Эпителиальный IFN-ответ.
Тепловые карты, отображающие масштабированную экспрессию (нулевое среднее, единичная дисперсия) известных генов ответа на IFN во всех эпителиальных клетках и отдельно в реснитчатых клетках в разных условиях на ранней и поздней фазах инфекции SARS-CoV-2 (ранняя: dps ≤ 4: n =11 детей, n=13 взрослых; поздний dps >4: n=11 детей, n=8 взрослых). Гены были отфильтрованы в соответствии с минимальным кратным изменением 1,5 между группой с самой низкой и самой высокой экспрессией, при этом ген был выбран в соответствии с их дифференциальной экспрессией во всех эпителиальных клетках. Гены, не соответствующие критерию, были выделены серым цветом, чтобы избежать раздувания незначительных различий в результате выполненного масштабирования. Масштабированный опыт. = масштабированное выражение.
Гены, не соответствующие критерию, были выделены серым цветом, чтобы избежать раздувания незначительных различий в результате выполненного масштабирования. Масштабированный опыт. = масштабированное выражение.
Расширенные данные Рис. 4 Характеристики NK и Т-клеток.
Профиль экспрессии цитотоксических генов и генов, связанных со старением, в подтипах NK и Т-клеток, полученных из n = 86 образцов назального обмена, различающих иммунный профиль детей и взрослых. пр. эксп. = средняя экспрессия гена, Pct. Эксп. = процент клеток, экспрессирующих ген.
Дополнительная информация
Сводка отчетов
Дополнительная таблица
Дополнительная таблица 1. Характеристики лиц с положительным результатом теста ( н = 45; a ) и отрицательные ( n = 42; b ), включенные в настоящее исследование.
Дополнительная таблица
Дополнительная таблица 2. Сводка характеристик когорты.
Дополнительные таблицы
Дополнительные таблицы 3–5. (TS 3): Характеристики пробоподготовки всех лиц ( n = 86), включенных в настоящее исследование. (TS 4): Дифференциально экспрессируемые гены в нейтрофилах. (TS 5): по-разному экспрессируемые гены в различных кластерах T/NK-клеток.
(TS 3): Характеристики пробоподготовки всех лиц ( n = 86), включенных в настоящее исследование. (TS 4): Дифференциально экспрессируемые гены в нейтрофилах. (TS 5): по-разному экспрессируемые гены в различных кластерах T/NK-клеток.
Права и разрешения
Перепечатка и разрешения
Об этой статье
Дополнительная литература
Патогенез SARS-CoV-2
- Март М. Ламерс
- Барт Л. Хаагманс
Обзоры природы Микробиология (2022)
Дексаметазон модулирует незрелые нейтрофилы и программирование интерферона при тяжелом течении COVID-19
- Сартак Синха
- Николь Л.
 Розин
Розин - Джефф Бернаски
Природная медицина (2022)
Дети демонстрируют загадочно низкий уровень антител к COVID
- Смрити Маллапати
Природа (2022)
ELF5 является потенциальным геном, специфичным для клеток респираторного эпителия, который может вызывать тяжелое течение COVID-19.

- Майк Питцнер
- Роберт Лоренц Чуа
- Клаудия Лангенберг
Nature Communications (2022)
Идентификация параметров, представляющих иммунную дисфункцию у пациентов с тяжелой и фатальной инфекцией COVID-19: систематический обзор и метаанализ
- Рундун Цинь
- Ли Хэ
- Цзин Ли
Клинические обзоры по аллергии и иммунологии (2022)
Лечение симптомов гриппа у здоровых детей: экономическая эффективность экспресс-тестирования и противовирусной терапии | Гериатрия | ДЖАМА Педиатрия
Абстрактный
Объектив Определить экономическую эффективность экспресс-тестирования и противовирусной терапии у детей разного возраста с симптомами гриппа.
Дизайн Анализ экономической эффективности с точки зрения общества с использованием модели принятия решений на основе опубликованных данных.
Настройка Кабинет врача во время эпидемии гриппа А.
Участники Гипотетические дети в возрасте 2, 7 и 15 лет.
Вмешательства Быстрое тестирование или клинический диагноз с последующим лечением гидрохлоридом амантадина или осельтамивира фосфатом по сравнению с отсутствием противовирусной терапии.
Итоговые показатели Затраты и ожидаемая продолжительность жизни с поправкой на качество.
Результаты Эмпирическая терапия противовирусными препаратами привела к наибольшей ожидаемой продолжительности жизни с поправкой на качество во всех возрастных группах. По сравнению с отсутствием лечения противовирусная терапия увеличила ожидаемую продолжительность жизни с поправкой на качество на 0,003 года жизни с поправкой на качество за счет сокращения продолжительности болезни и предотвращения среднего отита. У маленьких детей это сэкономило до 121 доллара на ребенка, в основном за счет предотвращения потери работы родителями. За исключением потери работы, противовирусная терапия увеличила ожидаемую продолжительность жизни с поправкой на качество при затратах от 800 до 1800 долларов за спасенный год жизни с поправкой на качество. По сравнению с амантадином осельтамивир не был экономически эффективен, когда преобладал грипп А. Приростная рентабельность осельтамивира упала ниже 50 000 долларов США за спасенный год жизни с поправкой на качество, когда доля гриппа B превышала 14 % для 2-летнего ребенка, 27 % для 7-летнего ребенка или 43 % для 15-летний. Экспресс-тестирование было экономически эффективным только тогда, когда вероятность гриппа составляла 60% или менее.
У маленьких детей это сэкономило до 121 доллара на ребенка, в основном за счет предотвращения потери работы родителями. За исключением потери работы, противовирусная терапия увеличила ожидаемую продолжительность жизни с поправкой на качество при затратах от 800 до 1800 долларов за спасенный год жизни с поправкой на качество. По сравнению с амантадином осельтамивир не был экономически эффективен, когда преобладал грипп А. Приростная рентабельность осельтамивира упала ниже 50 000 долларов США за спасенный год жизни с поправкой на качество, когда доля гриппа B превышала 14 % для 2-летнего ребенка, 27 % для 7-летнего ребенка или 43 % для 15-летний. Экспресс-тестирование было экономически эффективным только тогда, когда вероятность гриппа составляла 60% или менее.
Выводы Для детей с симптомами гриппа во время местной вспышки гриппа лечение противовирусной терапией, по-видимому, дает наилучший результат и часто позволяет сэкономить деньги. Выбор противовирусного препарата должен основываться на распространенности гриппа В.
Заражение вирусом гриппа обычно происходит во время зимних эпидемий, ежегодно поражая от 20% до 42% детей дошкольного и школьного возраста. 1 ,2 Хотя заболевание обычно самокупируется у детей старшего возраста, частота осложнений у детей младше 3 лет аналогична таковой у пожилых людей. 3 ,4 По этой причине рекомендуется вакцинация детей в возрасте от 6 до 23 месяцев и их близких контактов. 5 ,6 Кроме того, экономические последствия гриппа для всех возрастных групп огромны, что приводит к ежегодным прямым и косвенным затратам в США от 11 до 18 миллиардов долларов США. 7 Ежегодно от 6% до 28% детей посещают офисы по поводу гриппа, 1 и от трети до половины всех родителей пропускают работу, когда их ребенок болеет гриппом. 8 -10
Поставщики первичной медико-санитарной помощи принимают несколько решений, когда сталкиваются с ребенком, у которого проявляются симптомы гриппоподобного заболевания. Если ребенок поступает в течение 48 часов после появления симптомов, противовирусное лечение может сократить продолжительность болезни и предотвратить осложнения. Однако противовирусные препараты могут быть дорогими и вызывать побочные эффекты. Кроме того, клинический диагноз у детей может быть затруднен, поскольку другие вирусные заболевания могут имитировать грипп. Для повышения точности диагностики можно использовать экспресс-тестирование, но оно стоит дорого и может давать ложноположительные и ложноотрицательные результаты.
Если ребенок поступает в течение 48 часов после появления симптомов, противовирусное лечение может сократить продолжительность болезни и предотвратить осложнения. Однако противовирусные препараты могут быть дорогими и вызывать побочные эффекты. Кроме того, клинический диагноз у детей может быть затруднен, поскольку другие вирусные заболевания могут имитировать грипп. Для повышения точности диагностики можно использовать экспресс-тестирование, но оно стоит дорого и может давать ложноположительные и ложноотрицательные результаты.
Варианты лечения включают гидрохлорид амантадина и фосфат осельтамивира, единственные препараты, лицензированные в настоящее время для лечения гриппа у детей младше 7 лет. Занамивир, ингаляционный противовирусный препарат, одобрен для детей от 7 лет и старше, но он связан с реактивным заболеванием дыхательных путей и больше не рекламируется его производителем. Римантадина гидрохлорид не лицензирован для лечения детей. Несмотря на сходную эффективность против гриппа А, препараты различаются по стоимости, побочным эффектам, активности против гриппа типа В и индукции резистентности вируса. Решение еще более усложняется у детей, потому что стоимость лекарств, вероятность осложнений и объем потери работы родителями зависят от возраста ребенка.
Решение еще более усложняется у детей, потому что стоимость лекарств, вероятность осложнений и объем потери работы родителями зависят от возраста ребенка.
Оправдывают ли преимущества противогриппозной терапии у здоровых детей затраты и побочные эффекты? Если да, то должно ли лечение основываться на клиническом диагнозе или на основе экспресс-тестирования? Должна ли стандартная терапия включать осельтамивир или амантадин? Как рентабельность зависит от возраста ребенка? Чтобы ответить на эти вопросы, мы построили аналитическую модель принятия решений, чтобы определить экономическую эффективность эмпирической противовирусной терапии по сравнению с противовирусной терапией под контролем тестирования по сравнению с отсутствием противовирусной терапии для детей с симптомами гриппа.
Методы
Аналитическая модель принятия решений
Мы построили простое дерево решений (рис. 1) с помощью стандартной компьютерной программы (Decision Maker 7.07; Pratt Medical Group, Бостон, Массачусетс) для сравнения следующих стратегий: (1) нет противовирусная терапия, (2) эмпирическое лечение амантадином или осельтамивиром и (3) экспресс-тестирование в клинике с последующим лечением амантадином или осельтамивиром. Критериями исхода были сохраненные годы жизни с поправкой на стоимость и качество (QALY).
Критериями исхода были сохраненные годы жизни с поправкой на стоимость и качество (QALY).
Рисунок 1.
Просмотреть в большом форматеЗагрузить
Модель принятия решения о лечении гриппоподобных заболеваний у детей. Показаны узел решения (квадрат), случайные события (кружки) и конечные узлы (ромбы). Фактическая модель содержит отдельные противовирусные ветви для амантадина гидрохлорида и осельтамивира фосфата, а также отдельные ветви экспресс-тестирования для двух оцениваемых экспресс-тестов. ED указывает на отделение неотложной помощи.
Мы рассматривали здоровых детей в возрасте 2, 7 и 15 лет как репрезентативных для детей ясельного возраста, детей и подростков. Исходные различия для этих возрастных групп включают вероятность госпитализации, стоимость лекарств, основанных на весе, стоимость сиропа по сравнению с таблетками, а также необходимость того, чтобы взрослый человек, осуществляющий уход, пропустил работу в последний день болезни. Кроме того, в настоящее время вакцинация рекомендуется для всех детей в возрасте от 6 до 23 месяцев. Поскольку эта рекомендация является новой, мы провели все анализы дважды, один раз для привитых детей и еще раз для непривитых. Мы рассмотрели пациентов, обратившихся к врачу первичного звена с лихорадкой и кашлем или насморком в течение 48 часов после появления симптомов во время местной вспышки гриппа. Модель учитывает распространенность гриппа, чувствительность и специфичность тестов, а также следующие неблагоприятные события: противовирусные побочные эффекты, средний отит, обращения в отделение неотложной помощи, госпитализации и смерти. Инфекция гриппа может быть вызвана типом А или типом В, которые, как мы предполагали, имеют одинаковую степень тяжести. Мы предположили, что только осельтамивир эффективен при лечении гриппа В9.0003
Кроме того, в настоящее время вакцинация рекомендуется для всех детей в возрасте от 6 до 23 месяцев. Поскольку эта рекомендация является новой, мы провели все анализы дважды, один раз для привитых детей и еще раз для непривитых. Мы рассмотрели пациентов, обратившихся к врачу первичного звена с лихорадкой и кашлем или насморком в течение 48 часов после появления симптомов во время местной вспышки гриппа. Модель учитывает распространенность гриппа, чувствительность и специфичность тестов, а также следующие неблагоприятные события: противовирусные побочные эффекты, средний отит, обращения в отделение неотложной помощи, госпитализации и смерти. Инфекция гриппа может быть вызвана типом А или типом В, которые, как мы предполагали, имеют одинаковую степень тяжести. Мы предположили, что только осельтамивир эффективен при лечении гриппа В9.0003
Данные и допущения
Базовые оценки и диапазоны для анализа чувствительности представлены в таблице 1. Мы провели базовый анализ, анализ чувствительности и вероятностный анализ чувствительности для каждой возрастной группы как для сезона с преобладанием гриппа А, так и для смешанных типов А и Сезон Б.
Таблица 1.
Просмотреть увеличенную загрузку
Исходные значения для модели принятия решений и диапазоны, используемые в анализе чувствительности*
Диагностика гриппа и осложнения
Грипп трудно диагностировать у детей. Тем не менее, в проспективных исследованиях противовирусных препаратов, проведенных, когда было известно, что грипп циркулирует локально, у детей с температурой выше 37,8°C и по крайней мере 1 респираторным симптомом (кашлем или насморком) вероятность заболевания гриппом составляла от 65% до 73%. 11 ,12 Правило клинического прогнозирования, включающее кашель, головную боль и фарингит, имело положительную прогностическую ценность 77% у детей. 30
Быстрое тестирование может повысить точность диагностики. Доступно несколько тестов, но, насколько нам известно, в педиатрической практике было проведено только одно прямое сравнение. 17 Из этого испытания мы выбрали 2 теста, достаточно простых для проведения в кабинете врача (QuickVue [Quidel Corp, Сан-Диего, Калифорния] и ZstatFlu [ZymeTx Inc, Оклахома-Сити, Оклахома]). Оба выявляют инфекцию гриппа, но не различают типы А и В.
Оба выявляют инфекцию гриппа, но не различают типы А и В.
Осложнения, требующие назначения антибиотиков, чаще всего средний отит, возникали у 15-28% здоровых детей в группах плацебо в исследованиях противовирусных препаратов и вакцин. 11 ,12,14 Более серьезные осложнения включают пневмонию, энцефалопатию и смерть. Чтобы рассчитать вероятность госпитализации после визита в клинику, мы разделили избыточное количество госпитализаций на избыточное количество посещений амбулатории по оценке Neuzil et al. 3 Смертность на госпитализацию взята из базы данных Проекта затрат на здравоохранение и использования. 15
Противовирусная терапия
Мы рассмотрели все испытания противогриппозных препаратов у детей. В двух исследованиях амантадина 18 ,19 было показано, что он сокращал фебрильные симптомы на 12 и 28 часов (на 43% и 44% короче, чем в группе плацебо). Одно исследование 11 ,16 осельтамивира показало, что он снижает лихорадку на 25 часов (на 35% короче, чем в группе плацебо), возвращает детей к нормальной деятельности на 45 часов раньше и снижает количество назначений антибиотиков на 44%. В метаанализе было показано, что осельтамивир предотвращает госпитализацию у взрослых, 31 , но исследование у детей было слишком маленьким, чтобы это оценить; исследование пациентов с астмой не было опубликовано. 32 Мы предположили, что оба препарата будут одинаково эффективны для сокращения продолжительности болезни и предотвращения среднего отита, но ни один из них не предотвратит госпитализацию. Мы проверили эти предположения в анализе чувствительности.
В метаанализе было показано, что осельтамивир предотвращает госпитализацию у взрослых, 31 , но исследование у детей было слишком маленьким, чтобы это оценить; исследование пациентов с астмой не было опубликовано. 32 Мы предположили, что оба препарата будут одинаково эффективны для сокращения продолжительности болезни и предотвращения среднего отита, но ни один из них не предотвратит госпитализацию. Мы проверили эти предположения в анализе чувствительности.
По сравнению с плацебо амантадин лучше переносится детьми, чем осельтамивир. В испытаниях с участием 599 детей те, кто был рандомизирован в группу амантадина, испытывали меньше головокружения, возбуждения или бессонницы, чем дети, принимавшие плацебо (1,9).% против 2,4%), а также меньше тошноты или рвоты (6% против 10% для плацебо). 18 ,19 Пять дополнительных исследований профилактики амантадином, в которых участвовало более 1200 детей, также не выявили побочных эффектов. 20 -24 Осельтамивир, однако, ассоциировался с усилением тошноты и рвоты (14% в группе осельтамивира против 9% в группе плацебо, n = 695). 11 Побочные эффекты редко приводили к отмене препарата. Мы предполагали, что побочные эффекты начнутся на второй день лечения и продлятся 4 дня.
11 Побочные эффекты редко приводили к отмене препарата. Мы предполагали, что побочные эффекты начнутся на второй день лечения и продлятся 4 дня.
Коммунальные услуги
Поскольку ни одно из лекарств не снижает смертность, преимущества противовирусной терапии должны заключаться в улучшении качества жизни. Ожидаемая продолжительность жизни с поправкой на качество, обычно выражаемая в QALY, рассчитывается путем умножения лет (или, в данном случае, дней) в данном состоянии здоровья на полезность этого состояния. Утилиты, которые используются для корректировки качества, выражают предпочтения пациента в отношении различных состояний здоровья по шкале от 0 до 1, где 0 означает смерть, а 1 — полное здоровье. Например, 4 дня в гипотетическом состоянии здоровья с полезностью 0,4 переводятся в 1,6 дня жизни с поправкой на качество — сокращение ожидаемой продолжительности жизни с поправкой на качество на 2,4 дня или 0,0066 QALY. Преобразование всех исходов в единую единицу позволяет напрямую сравнивать разрозненные исходы для здоровья, такие как заболевание гриппом, средний отит и побочные эффекты лекарств. Наши оценки полезности для гриппа были основаны на неопубликованных данных испытаний занамивира у детей, в которых использовался инструмент EQ-5D из группы EuroQOL. 33 Оценки были аналогичны оценкам, полученным у здоровых взрослых. 34 Наша утилита для лечения среднего отита объединила оценки родителей, педиатров и членов сообщества. 25 ,35
Наши оценки полезности для гриппа были основаны на неопубликованных данных испытаний занамивира у детей, в которых использовался инструмент EQ-5D из группы EuroQOL. 33 Оценки были аналогичны оценкам, полученным у здоровых взрослых. 34 Наша утилита для лечения среднего отита объединила оценки родителей, педиатров и членов сообщества. 25 ,35
Мы приняли социальную точку зрения в соответствии с рекомендациями Группы экспертов по рентабельности в здравоохранении и медицине. 36 Таким образом, мы учитывали прямые медицинские затраты, включающие визиты к врачу, диагностические исследования, лекарства и госпитализации, а также косвенные затраты в виде потери производительности от родителей, остающихся дома для ухода за больными детьми. На основе данных опроса, проведенного в 3 начальных школах штата Вирджиния, мы подсчитали, что половина родителей с детьми младше 15 лет пропустят работу, чтобы ухаживать за детьми, больными гриппом. 8 Потеря производительности оценивалась с помощью среднего общего вознаграждения гражданских служащих США. 29 Гонорары врачей были основаны на относительных единицах стоимости Medicare для несложного визита к установленному пациенту ( Текущая процедурная терминология 37 , код 99213). Розничные затраты были использованы для экспресс-тестов. Затраты на лекарства отражали среднюю оптовую цену за 5-дневный курс плюс стоимость приобретения в размере 5 долларов. 26 Расходы на госпитализацию отражают данные Проекта затрат на здравоохранение и использования. 15 Все расходы были обновлены до долларов США 2003 года с помощью компонента медицинского обслуживания индекса потребительских цен. 38
8 Потеря производительности оценивалась с помощью среднего общего вознаграждения гражданских служащих США. 29 Гонорары врачей были основаны на относительных единицах стоимости Medicare для несложного визита к установленному пациенту ( Текущая процедурная терминология 37 , код 99213). Розничные затраты были использованы для экспресс-тестов. Затраты на лекарства отражали среднюю оптовую цену за 5-дневный курс плюс стоимость приобретения в размере 5 долларов. 26 Расходы на госпитализацию отражают данные Проекта затрат на здравоохранение и использования. 15 Все расходы были обновлены до долларов США 2003 года с помощью компонента медицинского обслуживания индекса потребительских цен. 38
Анализ чувствительности
Поскольку значение некоторых переменных является неопределенным, а другие различаются у разных пациентов, мы провели одно-, двух- и трехсторонний анализ чувствительности для всех переменных в таблице 1, чтобы оценить влияние на стоимость и эффективность. Мы также провели вероятностный анализ чувствительности N . Все переменные, кроме стоимости лекарств, вероятности заболевания гриппом и доли гриппа В, были введены как распределения вероятностей на основе 95% доверительные интервалы. Затем мы выполнили 1000 симуляций методом Монте-Карло. Для каждого моделирования случайным образом выбирались новые значения переменных из каждого распределения вероятностей, после чего рассчитывались связанные с этим затраты и ожидаемая продолжительность жизни с поправкой на качество. Мы использовали β-распределения для переменных от 0 до 1 (например, чувствительность теста или эффективность антибиотиков), равномерное распределение для полезности гриппа и нормальное распределение для остальных переменных (например, эффективность противовирусных препаратов для сокращения продолжительности болезни).
Мы также провели вероятностный анализ чувствительности N . Все переменные, кроме стоимости лекарств, вероятности заболевания гриппом и доли гриппа В, были введены как распределения вероятностей на основе 95% доверительные интервалы. Затем мы выполнили 1000 симуляций методом Монте-Карло. Для каждого моделирования случайным образом выбирались новые значения переменных из каждого распределения вероятностей, после чего рассчитывались связанные с этим затраты и ожидаемая продолжительность жизни с поправкой на качество. Мы использовали β-распределения для переменных от 0 до 1 (например, чувствительность теста или эффективность антибиотиков), равномерное распределение для полезности гриппа и нормальное распределение для остальных переменных (например, эффективность противовирусных препаратов для сокращения продолжительности болезни).
Результаты
Анализ базового случая
Мы рассмотрели 3 детей разного возраста, обратившихся к врачу первичного звена во время местной вспышки гриппа с высокой или низкой долей гриппа В (таблица 2). Эмпирическая терапия противовирусными препаратами привела к наибольшей ожидаемой продолжительности жизни с поправкой на качество во всех возрастных группах. По сравнению с отсутствием лечения противовирусная терапия улучшила ожидаемую продолжительность жизни с поправкой на качество на 0,003 QALY во всех возрастных группах за счет сокращения продолжительности болезни и предотвращения среднего отита. Вакцинированные дети имели более низкие затраты и лучшие результаты для здоровья, чем непривитые дети, независимо от выбранной стратегии. Экономит ли противовирусная терапия деньги и какой противовирусный препарат предпочтительнее, зависело от распространенности гриппа В и возраста ребенка.
Эмпирическая терапия противовирусными препаратами привела к наибольшей ожидаемой продолжительности жизни с поправкой на качество во всех возрастных группах. По сравнению с отсутствием лечения противовирусная терапия улучшила ожидаемую продолжительность жизни с поправкой на качество на 0,003 QALY во всех возрастных группах за счет сокращения продолжительности болезни и предотвращения среднего отита. Вакцинированные дети имели более низкие затраты и лучшие результаты для здоровья, чем непривитые дети, независимо от выбранной стратегии. Экономит ли противовирусная терапия деньги и какой противовирусный препарат предпочтительнее, зависело от распространенности гриппа В и возраста ребенка.
Таблица 2.
Просмотреть большую загрузку
Затраты, средняя ожидаемая продолжительность жизни и возрастающая экономическая эффективность стратегий борьбы с гриппом у детей разного возраста в течение 2 сезонов гриппа
была также наименее затратной стратегией для детей младше 15 лет, потому что экономия от родителей, возвращающихся на работу раньше, намного превышала стоимость лекарства. По сравнению с отсутствием лечения терапия амантадином позволила сэкономить 121 доллар на ребенка. Для детей, достаточно взрослых, чтобы оставаться дома одни в последний день болезни, отказ от лечения был наименее затратной стратегией. Эмпирическая терапия амантадином также увеличила ожидаемую продолжительность жизни в этой группе на 0,003 QALY при дополнительных затратах в размере 5 долларов США, что дало дополнительный коэффициент эффективности затрат в размере 1800 долларов США на каждый сохраненный QALY. По сравнению с амантадином эмпирический осельтамивир стоил дороже и давал худшие результаты, поскольку осельтамивир имеет больше побочных эффектов, чем амантадин.
По сравнению с отсутствием лечения терапия амантадином позволила сэкономить 121 доллар на ребенка. Для детей, достаточно взрослых, чтобы оставаться дома одни в последний день болезни, отказ от лечения был наименее затратной стратегией. Эмпирическая терапия амантадином также увеличила ожидаемую продолжительность жизни в этой группе на 0,003 QALY при дополнительных затратах в размере 5 долларов США, что дало дополнительный коэффициент эффективности затрат в размере 1800 долларов США на каждый сохраненный QALY. По сравнению с амантадином эмпирический осельтамивир стоил дороже и давал худшие результаты, поскольку осельтамивир имеет больше побочных эффектов, чем амантадин.
Во время сезонов, когда грипп B был обычным явлением, эмпирический осельтамивир заменял амантадин как наименее дорогой вариант для 2-летних детей; для детей старшего возраста прирост экономической эффективности осельтамивира по сравнению с амантадином варьировался от 7400 долларов США за сэкономленный QALY у 7-летних детей до 47 000 долларов США за сэкономленный QALY у 15-летних. Лечение 7-летних детей было менее рентабельным, чем лечение 2-летних, поскольку детям с массой тела более 15 кг требовались большие дозы лекарств.
Лечение 7-летних детей было менее рентабельным, чем лечение 2-летних, поскольку детям с массой тела более 15 кг требовались большие дозы лекарств.
Экспресс-тестирование на грипп не было полезным ни в один из сезонов гриппа, поскольку предтестовая вероятность гриппа была высокой, а тесты были недостаточно чувствительными. Тестирование было и более дорогим, и менее эффективным, чем эмпирическая терапия.
Анализ чувствительности
Во всех протестированных диапазонах эмпирическая терапия амантадином всегда была либо экономичной, либо недорогой (менее 20 000 долларов США за сэкономленный QALY) по сравнению с отсутствием лечения. Оставшийся вопрос, оправдывает ли дополнительная польза осельтамивира его более высокую стоимость, зависел от распространенности только гриппа B (рис. 2). Когда грипп В был редким, предпочтение всегда отдавалось амантадину. Однако, когда грипп В был обычным явлением, на выбор противовирусного препарата у детей старше 3 лет влияли следующие переменные: вероятность гриппа, стоимость и специфичность теста QuickVue, эффективность противовирусных препаратов в сокращении течения болезни, короткий -срочная заболеваемость гриппом, стоимость рабочего дня и стоимость осельтамивира. Из них клиницист при поступлении может оценить возраст пациента, долю гриппа, вызванного типом В, вероятность гриппа и краткосрочную заболеваемость, представленную тяжестью заболевания. В таблице 3 показана оптимальная стратегия, определяемая как та, которая обеспечивает наибольшее количество QALY при предельном коэффициенте экономической эффективности не более 50 000 долларов США на каждый сэкономленный QALY для всех комбинаций этих переменных.
Из них клиницист при поступлении может оценить возраст пациента, долю гриппа, вызванного типом В, вероятность гриппа и краткосрочную заболеваемость, представленную тяжестью заболевания. В таблице 3 показана оптимальная стратегия, определяемая как та, которая обеспечивает наибольшее количество QALY при предельном коэффициенте экономической эффективности не более 50 000 долларов США на каждый сэкономленный QALY для всех комбинаций этих переменных.
Рисунок 2.
Просмотреть в большом размере
Увеличение экономической эффективности осельтамивира фосфата в зависимости от доли гриппа типа B. Затраты и эффективность соотнесены с эмпирической терапией гидрохлоридом амантадина. Коэффициенты, превышающие 100 000 долларов США за год жизни с поправкой на качество (QALY), обычно считаются дорогими, а коэффициенты менее 50 000 долларов США за QALY считаются привлекательными.
Таблица 3.
Просмотреть в большом размереЗагрузить
Стратегия Обеспечение наибольшего количества QALY при предельной экономической эффективности на уровне 50 000 долл. США на каждый сэкономленный QALY или ниже* избегать дорогостоящих курсов осельтамивира, когда распространенность гриппа была от низкой до умеренной (30–50%), или если стоимость теста составляла менее 10 долларов США.
США на каждый сэкономленный QALY или ниже* избегать дорогостоящих курсов осельтамивира, когда распространенность гриппа была от низкой до умеренной (30–50%), или если стоимость теста составляла менее 10 долларов США.
Вероятностный анализ чувствительности
Результаты анализа методом Монте-Карло с использованием порога социальной готовности платить в размере 50 000 долларов США за каждый сэкономленный QALY подтверждают результаты базового сценария. Во время сезонов с преобладанием гриппа А эмпирический амантадин был предпочтительной стратегией во всех возрастных группах с максимальной дополнительной экономической эффективностью 9 долларов США.600 за каждый сохраненный QALY.
В смешанные сезоны гриппа эмпирический осельтамивир был предпочтительной стратегией для детей 2, 7 и 15 лет в 99,9%, 80% и 42% моделирования соответственно. Эмпирический амантадин обычно был наименее дорогой стратегией, но ему редко отдавали предпочтение, за исключением 15-летних, когда он был предпочтительнее в 51% симуляций. Повышение порога готовности платить сделало осельтамивир привлекательным и для 15-летних (рис. 3).
Повышение порога готовности платить сделало осельтамивир привлекательным и для 15-летних (рис. 3).
Рисунок 3.
Просмотреть в большом размере
Вероятностный анализ чувствительности Монте-Карло для 15-летнего больного гриппом во время локальной эпидемии в смешанный сезон гриппа А и В. Каждая строка показывает долю симуляций, в которых конкретная стратегия была бы предпочтительнее для значения готовности платить на сохраненный год жизни с поправкой на качество (QALY).
Комментарий
Этот анализ экономической эффективности показывает, что во время локальных вспышек гриппа дети с симптомами гриппоподобного заболевания получают пользу от противовирусной терапии, если она начата в течение 48 часов после появления симптомов. В то же время противовирусная терапия экономит деньги, если родители раньше выходят на работу. В этом случае нет компромисса между стоимостью и эффективностью. Когда родители не пропускают работу, противовирусная терапия по-прежнему увеличивает ожидаемую продолжительность жизни с поправкой на качество, но за счет денежных затрат. Экономическая эффективность противовирусной терапии, особенно амантадина, выгодно отличается от эффективности других рекомендуемых вмешательств, таких как вакцинация против ветряной оспы, 39 пневмококковый менингит, 40 и гепатит В. 41
Экономическая эффективность противовирусной терапии, особенно амантадина, выгодно отличается от эффективности других рекомендуемых вмешательств, таких как вакцинация против ветряной оспы, 39 пневмококковый менингит, 40 и гепатит В. 41
Предпочтительный противовирусный препарат почти полностью зависит от доли случаев гриппа, вызванных гриппом типа В. Осельтамивир намного дороже амантадина, но мало что известно об их относительной эффективности против инфекции гриппа А, поскольку сравнительных испытаний не проводилось. Когда преобладает грипп А, оба препарата кажутся одинаково эффективными, но амантадин может лучше переноситься и дешевле. Однако, поскольку амантадин не активен против гриппа B, осельтамивир будет более эффективен при преобладании гриппа B. Чтобы практиковать экономически эффективно, клиницисты должны знать о доле гриппа B, которую еженедельно можно получить в департаментах здравоохранения штатов и в Интернете в Центрах по контролю и профилактике заболеваний 13 и другие.
Мы не обнаружили никакой роли экспресс-диагностики во время локальных вспышек, поскольку клинический диагноз является высокопредсказательным, 30 , в то время как экспресс-тестирование приводит к частым ложноотрицательным результатам, 17 , таким образом увеличивая затраты без улучшения результатов. Аналогичные выводы были сделаны из анализов у взрослых. 34 ,42 Экспресс-тестирование полезно, когда вероятность гриппа составляет менее 50%, особенно во время вспышек гриппа В, поскольку осельтамивир дорог по сравнению со стоимостью тестирования, а чувствительность не так важна, когда вероятность до тестирования низкая (таблица 3).
Есть несколько препятствий для практической реализации нашей модели. Во-первых, некоторым практикующим врачам будет неудобно назначать эмпирическую терапию. Такая осторожность позволяет избежать ненужных побочных эффектов, но приводит к недостаточному лечению, даже если используется экспресс-тестирование. Поскольку частота побочных эффектов от осельтамивира и частота ложноотрицательных результатов для QuickVue идентичны, эмпирический осельтамивир скорее поможет ребенку, чем навредит ему, когда вероятность гриппа превышает 50%. Амантадин, который вызывает спутанность сознания у пожилых людей, по-видимому, лучше переносится детьми, его побочные эффекты сравнимы с таковыми у плацебо. В результате преимущества эмпирической терапии амантадином распространяются на детей с гораздо более низкой вероятностью заболевания.
Поскольку частота побочных эффектов от осельтамивира и частота ложноотрицательных результатов для QuickVue идентичны, эмпирический осельтамивир скорее поможет ребенку, чем навредит ему, когда вероятность гриппа превышает 50%. Амантадин, который вызывает спутанность сознания у пожилых людей, по-видимому, лучше переносится детьми, его побочные эффекты сравнимы с таковыми у плацебо. В результате преимущества эмпирической терапии амантадином распространяются на детей с гораздо более низкой вероятностью заболевания.
Во-вторых, наш анализ проводился с социальной точки зрения. Родители, оплачивающие лекарства из своего кармана, могут не захотеть покупать осельтамивир, особенно если они не ожидают потери заработной платы. Общий амантадин, с другой стороны, всегда должен быть привлекательным.
Наконец, мы не включили в нашу модель развитие резистентности к вирусам, потому что значение резистентности изучено недостаточно. Резистентность к осельтамивиру встречается редко, 11 , но резистентные вирусы быстро появляются во время терапии амантадином и могут передаваться в закрытом помещении, например в доме престарелых. 43 Устойчивые вирусы не являются более вирулентными и не вызывают эпидемий. 5 Тем не менее, если лечение приведет к широко распространенной резистентности к амантадину, амантадин больше не будет полезен для профилактики или лечения. В отличие от антибиотиков противовирусные препараты не могут вызывать резистентность у людей, которые в настоящее время не инфицированы вирусом. В результате эмпирическое лечение, которое включает лечение некоторых пациентов без гриппа, с меньшей вероятностью вызовет резистентность, чем терапия, направленная на тестирование. Если будет принято широкое использование короткого курса терапии амантадином, следует контролировать передачу резистентных вирусов, и приветствуется крупное клиническое исследование.
43 Устойчивые вирусы не являются более вирулентными и не вызывают эпидемий. 5 Тем не менее, если лечение приведет к широко распространенной резистентности к амантадину, амантадин больше не будет полезен для профилактики или лечения. В отличие от антибиотиков противовирусные препараты не могут вызывать резистентность у людей, которые в настоящее время не инфицированы вирусом. В результате эмпирическое лечение, которое включает лечение некоторых пациентов без гриппа, с меньшей вероятностью вызовет резистентность, чем терапия, направленная на тестирование. Если будет принято широкое использование короткого курса терапии амантадином, следует контролировать передачу резистентных вирусов, и приветствуется крупное клиническое исследование.
Наша модель не учитывала некоторые потенциальные преимущества противовирусной терапии. Если бы противовирусная терапия позволила сократить количество госпитализаций, она могла бы сэкономить средства для детей из групп высокого риска в любом возрасте. Однако единственное исследование осельтамивира у детей с астмой не показало значительного сокращения продолжительности болезни, и оно не было опубликовано. 32
Однако единственное исследование осельтамивира у детей с астмой не показало значительного сокращения продолжительности болезни, и оно не было опубликовано. 32
Противовирусные препараты также могут снизить передачу гриппа другим членам семьи, особенно непривитым младенцам или пожилым людям. Даже небольшое снижение передачи будет иметь большие экономические последствия и последствия для здоровья. На основе объединенного анализа Couch et al 44 сообщили, что противовирусная терапия привела к снижению передачи инфекции на 30% по сравнению с плацебо, но эти результаты никогда не публиковались. В двух рандомизированных исследованиях сравнивали постконтактную профилактику домохозяйств с помощью осельтамивира. В одном испытании 45 основной случай не получал противовирусную терапию, а у 21% отдельных контактов, получавших плацебо, развился грипп. В другом, 46 , индексный случай также получил противовирусную терапию, и только у 13% контактов, получавших плацебо, развился грипп (снижение на 38%). Необходимо проспективное исследование, чтобы увидеть, снижает ли лечение индексного случая распространение.
Необходимо проспективное исследование, чтобы увидеть, снижает ли лечение индексного случая распространение.
Наш анализ может переоценить пользу терапии для пациентов с гриппом B, который может быть более легким, чем грипп A. На основании небольшой выборки исследования мы предположили, что осельтамивир будет одинаково эффективен против гриппа A и B. 31 ,47 Если осельтамивир менее эффективен против гриппа B, чем A, то осельтамивир также будет менее рентабелен.
Еще одним препятствием для широкого применения противовирусных препаратов у детей является их незнание. Несмотря на то, что лекарства были доступны в течение многих лет, немногие врачи регулярно назначают их, а пациенты редко обращаются достаточно рано, чтобы получить лечение. Врачи, которые прописывают суспензию осельтамивира или сироп амантадина, могут быть разочарованы, обнаружив, что их нет в местных аптеках.
Серьезность эпидемии гриппа 2003-2004 гг. в некоторых районах США пробудила интерес к гриппу как к причине заболеваемости и смертности детей. 48 Хотя новые усилия по вакцинации должны несколько уменьшить бремя гриппа для экономики и здоровья, оно никоим образом не устранит его. Как это часто бывает, данные об эффективности противовирусных препаратов у детей очень ограничены. Нет ни сравнительных испытаний, ни исследований детей из группы высокого риска, ни исследований амантадина через 20 лет. Однако имеющиеся доказательства не противоречат друг другу. Противовирусная терапия сокращает продолжительность болезни, уменьшает средний отит и может уменьшить распространение среди других людей. Наш анализ показывает, что это также может сэкономить деньги.
48 Хотя новые усилия по вакцинации должны несколько уменьшить бремя гриппа для экономики и здоровья, оно никоим образом не устранит его. Как это часто бывает, данные об эффективности противовирусных препаратов у детей очень ограничены. Нет ни сравнительных испытаний, ни исследований детей из группы высокого риска, ни исследований амантадина через 20 лет. Однако имеющиеся доказательства не противоречат друг другу. Противовирусная терапия сокращает продолжительность болезни, уменьшает средний отит и может уменьшить распространение среди других людей. Наш анализ показывает, что это также может сэкономить деньги.
Наша модель предлагает основу для принятия решений. Большую пользу получают более молодые пациенты, особенно невакцинированные, но даже детей старшего возраста можно экономически эффективно лечить амантадином, когда циркулирует грипп А. При распространении гриппа B решение о тестировании или лечении должно включать тщательный анализ вероятности заболевания, ожидаемой потери работы и тяжести заболевания.
Адрес для переписки: Майкл Б. Ротберг, доктор медицины, магистр здравоохранения, отделение общей медицины и гериатрии, Медицинский центр Бэйстейт, 759Chestnut St, Springfield, MA 01199 ([email protected]).
Наверх
Информация о статье
Принято к публикации: 21 июля 2005 г.
Ссылки
1.
Neuzil КМЖу YГриффин Г-Н и другие. Бремя межпандемического гриппа у детей младше 5 лет: 25-летнее проспективное исследование. J Infect Dis 2002;185147-152PubMedGoogle ScholarCrossref
2.
Глезен WPTaber LHFrank А. Л. Грубер WCPiedra PA Вирусные инфекции гриппа у младенцев. Pediatr Infect Dis J 1997;161065- 1068PubMedGoogle ScholarCrossref
3.
Neuzil К.Меллен BGWright П. Ф. Митчел ЭФ МладшийГриффин MR Влияние гриппа на госпитализации, амбулаторные посещения и курсы антибиотиков у детей. N Engl J Med 2000;342225-231PubMedGoogle ScholarCrossref
4.
Izurieta Х. С. Томпсон WWKramarz п и другие. Грипп и частота госпитализаций по поводу респираторных заболеваний среди младенцев и детей раннего возраста. N Engl J Med 2000;342232-239PubMedGoogle ScholarCrossref
5.
Harper САФукуда КУеки ТМСокс Нью-Джерси CB Профилактика гриппа и борьба с ним: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep 2004;531- 40PubMedGoogle Scholar
6.
Комитет по инфекционным заболеваниям, Рекомендации по иммунизации детей против гриппа. Педиатрия 2004;1131441-1447PubMedGoogle ScholarCrossref
7.
Szucs T Социально-экономическое бремя гриппа. J Antimicrob Chemother 1999; 44 ((приложение Б)) 11- 15PubMedGoogle ScholarCrossref
8.
Nettleman MDБелый ТЛавуа Шафин C Пропуски занятий в школе, потеря работы родителями и согласие на вакцинацию против гриппа в детстве. Am J Med Sci 2001;321178- 180PubMedGoogle ScholarCrossref
9.
Neuzil
К.М.Хольбейн
Чжу
Y Заболевания школьников в сезон гриппа: влияние на пропуски занятий в школе, невыходы родителей на работу и вторичные заболевания в семьях. Arch Pediatr Adolesc Med 2002; 156986-991PubMedGoogle ScholarCrossref
Arch Pediatr Adolesc Med 2002; 156986-991PubMedGoogle ScholarCrossref
10.
Principi NEsposito SMarchisio Гаспарини RКровари P Социально-экономическое воздействие гриппа на здоровых детей и их семьи. г. Педиатр Infect Dis J 2003; 22 ((дополнение)) S207- S210PubMedGoogle ScholarCrossref
11.
Уитли Р.Дж. Хайден Ф. Г. Райзингер КС и другие. Пероральное лечение гриппа у детей осельтамивиром. Pediatr Infect Dis J 2001;20127- 133PubMedGoogle ScholarCrossref
12.
Hedrick
Ж.А.Барзилай
ABehre
U
и другие. Занамивир для лечения симптоматической инфекции гриппа А и В у детей в возрасте от пяти до двенадцати лет: рандомизированное контролируемое исследование. Pediatr Infect Dis J 2000;19410- 417PubMedGoogle ScholarCrossref
Pediatr Infect Dis J 2000;19410- 417PubMedGoogle ScholarCrossref
13.
Центры по контролю и профилактике заболеваний, Отчеты и методы наблюдения в Соединенных Штатах: текущий отчет о гриппе в США. Доступно на: http://www.cdc.gov/flu/weekly/fluactivity.htmДоступно 28 июня 2004 г.
14.
Белше Р.Б.Мендельман ПМТреанор Дж и другие. Эффективность живой аттенуированной холодоадаптированной трехвалентной интраназальной гриппозной вакцины у детей. N Engl J Med 1998;3381405- 1412PubMedGoogle ScholarCrossref
15.
Agency for Healthcare Research and Quality, HCUPnet, Healthcare Cost and Usage Project, 2000. Доступно по адресу: http://www.ahrq.gov/data/ hcup/hcupnet.htmПо состоянию на 7 июня 2004 г.
16.
Тернер ДВайлу Николсон К. Купер Н.Саттон Абрамс K Систематический обзор и моделирование экономических решений для профилактики и лечения гриппа А и В. Health Technol Assess 2003;7iii-iv, xi-xiii, 1-170PubMedGoogle Scholar
17.
Rodriguez WJSchwartz РХторн ММ Оценка диагностических тестов на грипп в педиатрической практике. Pediatr Infect Dis J 2002; 21193- 196PubMedGoogle ScholarCrossref
18.
Китамото O Терапевтическая эффективность гидрохлорида амантадина при гриппе A2 — двойные слепые исследования. Jpn J Tuberc Chest Dis 1968;1517- 26PubMedGoogle Scholar
19.
Китамото
O Терапевтическая эффективность гидрохлорида амантадина при природном гонконгском гриппе — двойное слепое исследование. Jpn J Tuberc Chest Dis 1971;171- 7PubMedGoogle Scholar
Jpn J Tuberc Chest Dis 1971;171- 7PubMedGoogle Scholar
20.
Payler Д.К.Пурдэм PA Профилактика гриппа А амантадином в школе-интернате. Lancet 1984;1502- 504PubMedGoogle ScholarCrossref
21.
Куиллиган ДжейДжей младший Хираяма МБернштайн HD Jr Подавление гриппа А2 у детей с помощью химиопрофилактического применения амантадина. J Pediatr 1966;69572- 575PubMedGoogle ScholarCrossref
22.
Rose HJ Использование амантадина и вакцины против гриппа во время эпидемии гриппа типа А в школе-интернате. JR Coll Gen Pract 1980;30619-621PubMedGoogle Scholar
23.
Финклея
Дж. Ф. Хеннесси
АВДавенпорт
FM Полевые испытания профилактики амантадином при естественных острых респираторных заболеваниях. Am J Epidemiol 1967;85403- 412PubMedGoogle Scholar
Ф. Хеннесси
АВДавенпорт
FM Полевые испытания профилактики амантадином при естественных острых респираторных заболеваниях. Am J Epidemiol 1967;85403- 412PubMedGoogle Scholar
24.
Davies Дж.Р.Грилли EASmith А.Дж.Хоскинс TW Профилактическое использование амантадина при вспышке гриппа А в школе-интернате.0003
25.
Проссер LARay GTO’Брайен М.Клейнман К.Сантоли JLieu TA Предпочтения и готовность платить за состояние здоровья, предотвращенное пневмококковой конъюгированной вакциной. Pediatrics 2004; 113283-290PubMedGoogle ScholarCrossref
26.
Mosby’s Drug Consult 2004. 14-е изд. Сент-Луис, Mo Mosby-Ежегодник Inc 2004;
27.
Поиск по тарифам врача Medicare. Центры услуг Medicare и Medicaid, 2003 г. Доступно по адресу: http://www.cms.hhs.gov/providers/Accessed 22 июня 2004 г.
28.
Кокс FMCobb ММЧуа WQMcLaughlin ТПОкамото LJ Стоимость лечения гриппа в отделениях неотложной помощи и больницах. Am J Manag Care 2000;6205- 214 PubMedGoogle Scholar
29.
Бюро трудовой статистики США, Расходы работодателя на оплату труда сотрудников. 2003; доступно по адресу: http://www.bls.gov/ncs/ect/home.htmДоступно 7 июня 2004 г.
30.
Фридман MJAttia MW Клинические предикторы гриппа у детей. Arch Pediatr Adolesc Med 2004;158391- 394PubMedGoogle ScholarCrossref
31.
Kaiser
LWat
СМиллс
ТМахони
PWard
ПХайден
F Влияние лечения осельтамивиром на связанные с гриппом осложнения нижних дыхательных путей и госпитализации. Arch Intern Med 2003;1631667- 1672PubMedGoogle ScholarCrossref
Arch Intern Med 2003;1631667- 1672PubMedGoogle ScholarCrossref
32.
Matheson Н. Дж. Симмондс-Абрахамс Шейх АШепперд Шарнден Ингибиторы нейраминидазы для профилактики и лечения гриппа у детей. Кокрановская база данных Syst Rev 2003;CD002744PubMedGoogle Scholar
33.
Brooks R EuroQol: текущее состояние дел. Health Policy 1996;3753- 72PubMedGoogle ScholarCrossref
34.
Rothberg МБHe Роза DN Лечение симптомов гриппа у здоровых взрослых. J Gen Intern Med 2003;18808- 815PubMedGoogle ScholarCrossref
35.
Oh
П.И.Маеров
Притчард
ДКноулз
С. Р.Эйнарсон
TRСдвиг
NH Анализ эффективности затрат антибиотиков второго ряда при лечении острого среднего отита у детей. Clin Ther 1996;18160- 182PubMedGoogle ScholarCrossref
Р.Эйнарсон
TRСдвиг
NH Анализ эффективности затрат антибиотиков второго ряда при лечении острого среднего отита у детей. Clin Ther 1996;18160- 182PubMedGoogle ScholarCrossref
36.
Золото МедСигель Джед Рассел ЛедВайнштейн Med Экономическая эффективность в здравоохранении и медицине. Нью-Йорк, NY Oxford University Press, 1996;425
37.
CPT 2004: Current Procedural Terminology: Professional Edition. Чикаго, Американская медицинская ассоциация, 2004 г.;
38.
Бюро статистики труда США, Индекс потребительских цен — все городские потребители, 2004 г. Доступно по адресу: http://www.bls.gov/data/Доступно 7 июня 2004 г.
39.
Заместитель
ТАКочи
SLЧерный
СБ
и другие. Экономическая эффективность программы плановой вакцинации против ветряной оспы для детей в США. JAMA 1994;271375- 381PubMedGoogle ScholarCrossref
Экономическая эффективность программы плановой вакцинации против ветряной оспы для детей в США. JAMA 1994;271375- 381PubMedGoogle ScholarCrossref
40.
Lieu TARay GTЧерный СБ и другие. Прогноз экономической эффективности пневмококковой конъюгированной вакцинации здоровых младенцев и детей раннего возраста. JAMA 2000;2831460- 1468PubMedGoogle ScholarCrossref
41.
Кран М.Гуаспарини Шерман МДецкий AS Затраты и экономическая эффективность универсальной школьной программы вакцинации против гепатита В. Am J Public Health 1998;881638- 1644PubMedGoogle ScholarCrossref
42.
Smith
К.Дж.Робертс
MS Экономическая эффективность новых стратегий лечения гриппа. Am J Med 2002;113300- 307PubMedGoogle ScholarCrossref
Am J Med 2002;113300- 307PubMedGoogle ScholarCrossref
43.
Шираиси КМитамура Ксакаи-Тагава YGoto Хсугая НКаваока Y Высокая частота резистентных вирусов с различными мутациями у детей с гриппом, получавших лечение амантадином. J Infect Dis 2003;18857- 61PubMedGoogle ScholarCrossref
44.
Диван РБКасел JAGlezen ВП и другие. Грипп: его контроль среди людей и населения. J Infect Dis 1986;153431- 440PubMedGoogle ScholarCrossref
45.
Welliver РМонто А.С.Каревич О и другие. Эффективность осельтамивира в профилактике гриппа при бытовых контактах: рандомизированное контролируемое исследование. JAMA 2001;285748- 754PubMedGoogle ScholarCrossref
46.
Хайден ФГБельше Р.Вильянуэва С и другие. Ведение гриппа в домашних хозяйствах: проспективное рандомизированное сравнение лечения осельтамивиром с постконтактной профилактикой или без нее. J Infect Dis 2004;189440- 449PubMedGoogle ScholarCrossref
47.
Kaiser ЛКин ОНХаммонд Дж. М. Эллиотт Мхайден FG Влияние занамивира на использование антибиотиков при респираторных заболеваниях после острого гриппа у подростков и взрослых. Arch Intern Med 2000;1603234- 3240PubMedGoogle ScholarCrossref
48.
Центры по контролю и профилактике заболеваний (CDC), обновленная информация: зарегистрированы случаи смерти, связанные с гриппом, среди детей в возрасте до 18 лет — США, сезон гриппа 2003–2004 гг. MMWR Morb Mortal Wkly Rep 2004;521286- 1288PubMedGoogle Scholar
Тамифлю: побочные эффекты у детей
Тамифлю – это лекарство, отпускаемое по рецепту, для лечения гриппа у детей и взрослых.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило использование Тамифлю в 1999 году.
В 2009 году правительства по всему миру создали запасы этого препарата в ответ на всемирное распространение штамма гриппа h2N1, или «свиного гриппа».
Однако недавние исследования поставили под сомнение эффективность Тамифлю и вызвали опасения по поводу возможных побочных эффектов.
В этой статье представлены современные данные об эффективности и безопасности Тамифлю у детей.
Противовирусные препараты против гриппа — это препараты, сокращающие продолжительность симптомов гриппа. Тамифлю — торговая марка противовирусного препарата осельтамивир.
Осельтамивир относится к противовирусным препаратам класса ингибиторов нейраминидазы (NAI).
Нейраминидаза — это фермент, который позволяет вирусу размножаться внутри организма. NAI блокируют эти ферменты и помогают предотвратить репликацию вируса.
Врач может назначить Тамифлю для облегчения тяжелых симптомов гриппа у детей в возрасте от 2 недель или для профилактики гриппа у детей в возрасте 1 года и старше.
Для получения дополнительной информации и ресурсов, которые помогут сохранить здоровье вам и вашим близким в этот сезон гриппа, посетите наш специальный центр .
Тамифлю может вызывать различные побочные эффекты. Большинство распространенных побочных эффектов не являются серьезными, но возможны более редкие и более серьезные побочные эффекты.
Общие побочные эффекты
По данным FDA, наиболее распространенными побочными эффектами Тамифлю являются тошнота и рвота. Оба, как правило, возникают в течение первых 2 дней лечения.
Прием Тамифлю во время еды может снизить риск расстройства желудка.
Другие потенциальные побочные эффекты
Другие побочные эффекты осельтамивира могут включать:
- боль в животе
- головную боль
- носовое кровотечение
- усталость
В некоторых случаях озелтамивир может вызывать более серьезные побочные эффекты. Ребенку или взрослому, у которого наблюдается любое из следующих явлений, следует немедленно обратиться к врачу или обратиться в службу неотложной помощи:
- allergic skin rash, hives, or blisters
- itching
- swelling of the face or tongue
- difficulty breathing or swallowing
- mouth sores
- hoarseness
- speech problems
- confusion
- shaky movements
- hallucinations
Нейропсихиатрические побочные эффекты
В обзоре 2012 года изучался риск нейропсихиатрических побочных эффектов у детей и взрослых, получающих осельтамивир. Нейропсихиатрические эффекты — это те, которые медицинские работники связывают с психическим здоровьем человека и нервной системой.
Нейропсихиатрические эффекты — это те, которые медицинские работники связывают с психическим здоровьем человека и нервной системой.
Согласно обзору, в период с сентября 2007 г. по май 2010 г. около 1330 человек во всем мире испытали так называемые нейропсихиатрические нежелательные явления (НПЯ) при приеме осельтамивира.
В общей сложности 1072 таких НПЯ произошли у детей в возрасте 16 лет и младше.
Наиболее распространенными НППП среди детей были аномальное поведение, бред и нарушения восприятия.
Однако авторы предположили, что NPAE, возможно, не были связаны с осельтамивиром, а были симптомом вируса гриппа.
Авторы основывали этот вывод на следующих наблюдениях:
- NPAE также встречались среди людей, которые не принимали осельтамивир.
- Большинство случаев NPAE происходило, когда у людей была лихорадка.
- Лихорадка может непосредственно вызывать психические симптомы.
Для некоторых детей польза от приема Тамифлю может перевешивать любые потенциальные риски. Сюда входят дети с тяжелыми симптомами гриппа и дети со следующими сопутствующими заболеваниями:
Сюда входят дети с тяжелыми симптомами гриппа и дети со следующими сопутствующими заболеваниями:
- болезни сердца
- заболевания легких
- заболевания почек
- заболевания печени
- Рак
- Неревромассулярные расстройства
- Серплевая болезнь
- Диабез . детей с одним или несколькими из вышеперечисленных состояний.
- диарея
- Тошнота
- Головная боль
- Гловолюбие
- Синусит
- Симптомы носа
- Кашель
- Бронхит
- ух, нос и горло. Врач может назначить перамивир для лечения гриппа, но не для его предотвращения.
Перамивир может помочь в лечении гриппа у детей в возрасте 2 лет и старше. Это особенно удобно для детей, которые не могут принимать противовирусные препараты перорально или ингаляционно.
Согласно обзору 2016 года, побочные эффекты перамивира чаще встречаются у детей, но они, как правило, от легкой до умеренной степени тяжести.
Побочные эффекты у детей включают:
- ненормальное поведение
- кашель
- лихорадка
- желудочно-кишечные расстройства
Исследования показывают, что Тамифлю, как правило, более полезен для детей и взрослых с тяжелыми симптомами гриппа и теми, у кого есть серьезные сопутствующие заболевания.
 .
.Преимущества Тамифлю для здоровых людей с легкими симптомами следует сопоставлять с риском потенциальных побочных эффектов.
Реленза (занамивир) и Рапиваб (перамивир) — две альтернативы Тамифлю, подходящие для детей. Врач решит, какое противовирусное лекарство от гриппа является наиболее подходящим в каждом конкретном случае.
Педиатрический опоясывающий герпес (опоясывающий лишай) — условия и лечение
Обновление COVID-19: Узнайте больше о том, как мы защищаем наших пациентов, семьи и персонал, а также другие важные факты о COVID-19.Основные сведения об опоясывающем лишае у детей
- Опоясывающий лишай (опоясывающий герпес) представляет собой болезненную кожную сыпь. Это вызвано вирусом, вызывающим ветряную оспу.
- Опоясывающий лишай у детей встречается редко.
- Симптомы начинаются с боли, жжения, покалывания или зуда на одной части лица или тела. Затем вирус может вызвать красную сыпь или небольшие волдыри, обычно на одной стороне тела.

- Немедленное лечение противовирусными препаратами может уменьшить продолжительность симптомов и их серьезность.
- Если у вашего ребенка сильная боль, поставщик медицинских услуг может выписать сильное обезболивающее.
- Существует вакцина против опоясывающего лишая для пожилых людей, но не для детей. Но у ребенка, которому была сделана прививка от ветряной оспы, могут быть более легкие симптомы опоясывающего лишая.
Опоясывающий лишай (опоясывающий герпес) представляет собой болезненную кожную сыпь. Вызывается вирусом ветряной оспы (VZV). Это тот же вирус, который вызывает ветрянку.
После того, как человек переболел ветряной оспой, вирус остается в нервных клетках организма, но неактивен. Спустя месяцы или годы вирус ветряной оспы может снова стать активным. Затем вирус может вызвать красную сыпь или небольшие волдыри, обычно на одной стороне тела.
 Сыпь или волдыри распространяются по нервным путям, где живет вирус.
Сыпь или волдыри распространяются по нервным путям, где живет вирус.Опоясывающий лишай у детей встречается нечасто. Ребенок больше подвержен риску заболеть опоясывающим лишаем, если верно одно из следующих утверждений:
- У них была ветряная оспа в возрасте до 1 года.
- Мать ребенка болела ветряной оспой на очень поздних сроках беременности.
- У ребенка слабая иммунная система из-за состояния здоровья или некоторых видов лечения, таких как терапия рака.
Дети, получающие вакцину против ветряной оспы, по-прежнему имеют небольшой риск заболеть опоясывающим лишаем. Но это может быть более низкий риск, чем после заражения ветряной оспой. И симптомы могут быть менее серьезными.
Симптомы начинаются с боли, жжения, покалывания или зуда на одной части лица или тела. Сыпь может появиться до пяти дней после появления этих симптомов.
Опоясывающая сыпь чаще всего возникает на туловище и ягодицах.
 Он также может появиться на руках, ногах или лице. Сыпь начинается с небольших красных пятен, которые превращаются в волдыри. Волдыри желтеют и засыхают. Сыпь обычно бывает только на одной стороне или части тела. Он проходит через две-четыре недели.
Он также может появиться на руках, ногах или лице. Сыпь начинается с небольших красных пятен, которые превращаются в волдыри. Волдыри желтеют и засыхают. Сыпь обычно бывает только на одной стороне или части тела. Он проходит через две-четыре недели.У вашего ребенка также могут быть такие симптомы, как:
- Лихорадка и озноб
- Головная боль
- Тошнота
Симптомы опоясывающего лишая могут быть такими же, как и при других заболеваниях. Убедитесь, что ваш ребенок посещает врача для диагностики.
Медицинский работник спросит о симптомах и истории болезни вашего ребенка. Вашему ребенку предстоит медицинский осмотр. Опоясывающий лишай обычно можно диагностировать только на основании осмотра. У вашего ребенка также могут быть тесты, такие как:
- Соскобы кожи. Пузыри осторожно соскабливают, чтобы удалить крошечные образцы. Образцы проверяются на наличие вируса.
Лечение будет зависеть от симптомов, возраста и общего состояния здоровья вашего ребенка.
 Это также будет зависеть от того, насколько тяжелым является состояние.
Это также будет зависеть от того, насколько тяжелым является состояние.Немедленное лечение противовирусными препаратами может уменьшить продолжительность симптомов и их серьезность. Эти противовирусные препараты работают лучше, чем раньше они начинаются. Вашему ребенку могут назначить ацикловир, фамцикловир или валацикловир. Поговорите с лечащим врачом вашего ребенка о рисках, преимуществах и возможных побочных эффектах всех лекарств.
Узнайте у поставщика медицинских услуг о безрецептурных обезболивающих препаратах. Вы можете дать ацетаминофен или ибупрофен от лихорадки и дискомфорта. Не давайте ибупрофен ребенку младше 6 месяцев, если только ваш лечащий врач не скажет вам об этом. Не давайте аспирин детям. Аспирин может вызвать серьезное заболевание, называемое синдромом Рея.
Если у вашего ребенка сильная боль, поставщик медицинских услуг может выписать более сильное обезболивающее.
Сыпь при опоясывающем лишае может инфицироваться бактериями, вызывая кожную инфекцию (флегмону).
 После исчезновения опоясывающей сыпи боль может сохраняться в течение длительного времени. Это осложнение называется постгерпетической невралгией (ПГН). Поговорите с поставщиком медицинских услуг, если боль вашего ребенка остается после исчезновения сыпи.
После исчезновения опоясывающей сыпи боль может сохраняться в течение длительного времени. Это осложнение называется постгерпетической невралгией (ПГН). Поговорите с поставщиком медицинских услуг, если боль вашего ребенка остается после исчезновения сыпи.Существует вакцина против опоясывающего лишая для пожилых людей, но не для детей. Это связано с тем, что опоясывающий лишай протекает более тяжело у пожилых людей. Но у ребенка, которому была сделана прививка от ветряной оспы, могут быть более легкие симптомы опоясывающего лишая. Если ваш ребенок не болел ветряной оспой, поговорите с врачом о вакцине против ветряной оспы.
Позвоните поставщику медицинских услуг, если у вашего ребенка:
- Симптомы, которые не улучшаются или ухудшаются
- Новые симптомы
Лечение дерматологии в Детской национальной больнице
Педиатрические специалисты Детской национальной больницы обладают опытом диагностики, лечения и лечения заболеваний кожи, ногтей и волос, характерных для младенцев и детей младшего возраста.

Исследования показывают, что эффективность Тамифлю различается у здоровых людей с легким гриппом и у людей с тяжелым гриппом или другими проблемами со здоровьем.
Воздействие на здоровых людей
Ранние клинические испытания показали, что Тамифлю очень эффективен при лечении гриппа у здоровых людей. В 1999 году последовало одобрение препарата FDA. Авторы обнаружили, что препарат сокращает продолжительность симптомов гриппа менее чем на сутки.
Осельтамивир, общее название Тамифлю, не оказывал существенного влияния на то, должны ли врачи впоследствии госпитализировать людей. Препарат существенно не уменьшал серьезные осложнения гриппа, такие как бронхит, синусит и инфекции среднего уха. Некоторые люди также испытывали побочные эффекты при приеме препарата.
Препарат существенно не уменьшал серьезные осложнения гриппа, такие как бронхит, синусит и инфекции среднего уха. Некоторые люди также испытывали побочные эффекты при приеме препарата.
Авторы этого обзора предположили, что осельтамивир помогает лечить симптомы гриппа, но не препятствует размножению вируса.
Roche, компания, которая продавала оригинальный препарат, совместно финансировала отдельное исследование, которое не согласилось с этим утверждением и поддержало использование NAI.
Последствия для госпитализированных пациентов
В 2009 г. в странах мира произошла вспышка вируса h2N1 или «свиного гриппа». Впервые исследователи смогли собрать данные наблюдений об эффективности Тамифлю у госпитализированных пациентов.
В исследовании 2013 года были проанализированы медицинские карты 784 детей, госпитализированных врачами по поводу гриппа.
Из них 8 процентов, не получавших лечение NAI, умерли в результате инфекции. Это на 2 процента больше, чем число детей, умерших после лечения ингибиторами анестетика.
Кроме того, дети, получавшие лечение ингибиторами анестетика на ранних стадиях развития болезни, имели больше шансов выжить.
Авторы обзора 2016 года предположили, что данные, полученные от людей с легкими симптомами, не следует использовать для определения того, эффективны ли NAI для людей с тяжелыми случаями гриппа.
Как правило, у здоровых людей иммунная система организма может бороться с вирусом гриппа. У людей с более слабой иммунной системой противовирусные препараты могут укрепить иммунную систему и помочь избавить организм от вируса.
Занамивир и перамивир — два альтернативных ИПН, которые подходят для детей.
Занамивир
Занамивир (Реленза) представляет собой порошок, который человек вдыхает с помощью специального ингалятора.
Врач может назначить занамивир для лечения гриппа у детей в возрасте 7 лет и старше или для профилактики гриппа у детей в возрасте 5 лет и старше.
Занамивир не подходит для людей с астмой или другими респираторными заболеваниями, так как он увеличивает риск бронхоспазма, когда мышцы легких напрягаются и ограничивают поток воздуха.
По данным Центров по контролю и профилактике заболеваний (CDC), менее 5 процентов людей, участвующих в клинических испытаниях, испытывали побочные эффекты в ответ на вдыхание занамивира.
Несмотря на это, возможные побочные эффекты могут включать: