Модель пентана из пластилина: 2. Изготовление моделей молекул углеводородов
Лабораторная работа № 7 — Студопедия
Поделись с друзьями:
«Моделирование молекул алканов и их производных»
Цели работы
· изучить особенности строения молекул органических веществ;
· найти общие признаки и различия гомологов и изомеров;
· научиться составлять модели молекул различной сложности.
Краткие теоретические сведения
| Для того чтобы понять сущность работы, надо знать, что: 1. Простейшим представителем насыщенных углеводородов является метан, структурная формула которого | |
| 2. sp3– гибридизация характерна для атомов углерода в (алканах) – в частности, в метане. | рис. 10 |
3. Атом углерода в молекуле метана расположен в центре тетраэдра, атомы водорода – в его вершинах.
4. Валентные углы между направлениями связей равны между собой и составляют угол 109°28′. | |
| 5. В этане есть углерод-углеродные связи. L (С-С) = 0,154 нм. Оборудование пластилин, спички. | рис. 11 |
Задание № 1. Составление сокращённых структурных формул углеводородов.
1. Формула молекулы метана.
2. Формула молекулы этана.
3. Формула молекулы пропана.
4. Формулы молекул бутана и изобутана.
5. Формулы молекулы пентана и всех его изомеров.
Задание № 2. Изготовление моделей молекул углеводородов
1. Модель молекулы метана. Соберите модель молекулы метана, используя для этого спички и пластилин. Для этого из пластилина (в наборе 16 шариков) выберите четыре шарика, а из пластилина (в наборе 7 шариков) – один шарик. В качестве стержней можно использовать спички. Учтите, что в молекуле метана угол между химическими связями С–Н составляет 109°28′, т. е. молекула имеет тетраэдрическое строение (см. рис. 10).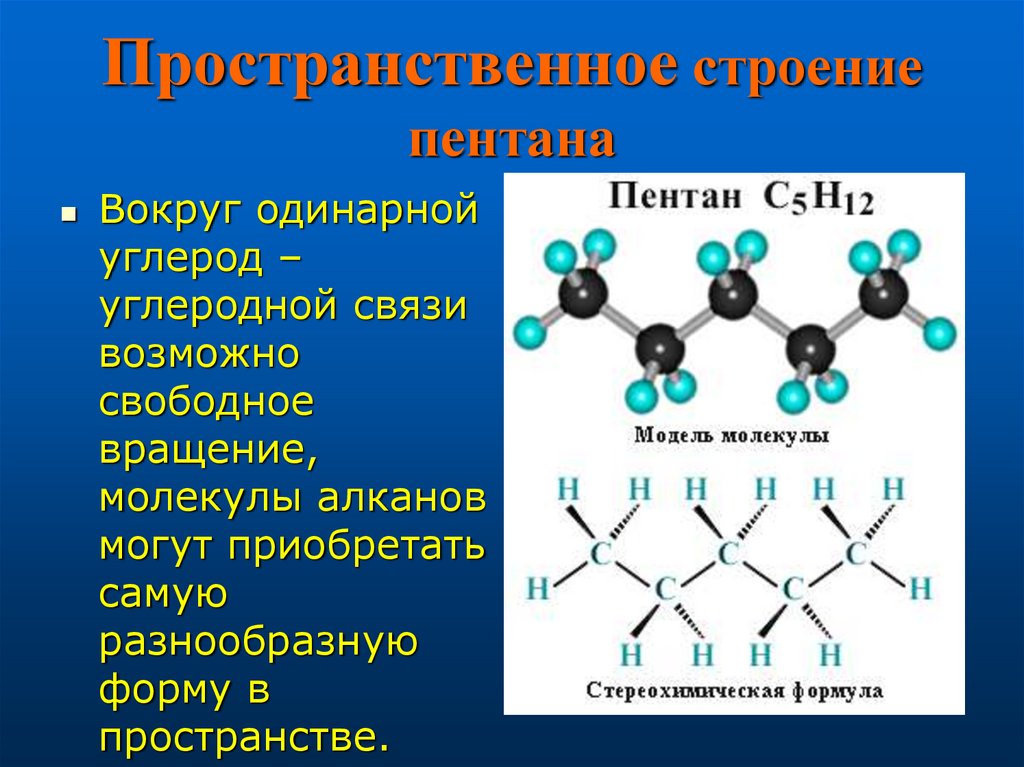
2. Модель молекулы этана. Соберите модель молекулы этана, используя для этого спички и пластилин. Учтите, что в молекуле этана угол между химическими связями С–Н составляет 109°28′, а углерод-углеродные связи L (С-С) = 0,154 нм. (см. рис. 11).
3. Модель молекулы пропана. Соберите модель молекулы пропана, используя для этого спички и пластилин.
4. Модели молекул бутана и изобутана. Соберите модель молекулы н-бутана, используя пластилин. Подумайте и переделайте модель н-бутана в модель молекулы изобутана. Учтите, что в бутане атомы углерода расположены по отношению друг к другу под углом 109°, т. е. углеродная цепь должна иметь зигзагообразное строение. В молекуле изобутана все связи центрального атома углерода направлены к вершинам правильного тетраэдра. Сравните строение этих углеводородов.
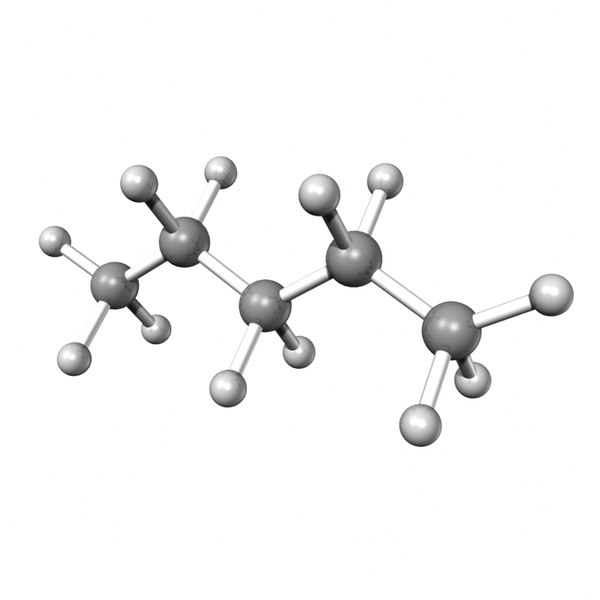
5. Модели молекул пентана и всех его изомеров. Соберите модель молекулы
Вопросы для выводов
1. Сколько моделей: а) гомологов, б) изомеров было собрано во время лабораторной работы
Сколько моделей: а) гомологов, б) изомеров было собрано во время лабораторной работы
2. Что общего и в чём различия в строении а) гомологов, б) изомеров
Контрольные вопросы
1) Какие вещества называют органическими?
2) В чем отличие органических веществ от неорганических веществ?
3) Определите молекулярную формулу вещества, если оно содержит С-80%,Н-20%, а плотность вещества по водороду равна 15.
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Поурочный план лабораторной работы по теме: “Изготовление моделей молекул углеводородов”
Урок: Химия
Группа: БУ-15
Тема: Изготовление моделей молекул углеводородов и их галогенопроизводных.
Цель работы:
1. Изучить пространственное строение молекул алканов и их галогенопроизводных.
2. Изготовить шаростержневые
модели молекул метана, этана, бутана, хлорэтана и трихлорметана.
3. Развивать представления о существовании различных способов моделирования молекул органических соединений.
Оборудование: разноцветный пластелин,спички.
Тип урока: закрепление знаний. Лабораторная работа.
Цель урока:
1. научить составлять структурные формулы и шаростержневые модели молекул алканов по их молекулярным формулам;
2. организовать исследовательскую деятельность, направленную на усвоение знаний по изомерии и гомологии органических веществ.
Задачи:
образовательные: закрепить знания учащихся о составе, структурных формулах и шаростержневых моделях молекул органических веществ, изомерии и гомологии алканов;
развивающие: развивать творческую активность и самостоятельность учеников, образное и логическое мышление, объективную самооценку;
воспитывающие: дисциплинированность,
аккуратность, внимательность, ответственное отношение к учебному труду, умение
работать в парах.
Оборудование: презентация «Изготовление шаростержневых моделей молекул углеводородов», наборы «Комплекты для составления шаростержневых моделей молекул различных веществ», инструктивные карточки.
Литература: Органическая химия 11 класс. Н. Нурахметов. Параграф 3.1-3.5 стр.64-80
Материалы: Учебник, карточки.
Структура урока.
Этап урока | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
Минуты | 2 | До 25 | 10 | 45 | 3 | 5 | 2 |
Ход урока
1. Организационный
момент.
Организационный
момент.
2. Опрос домашнего материала:
a) Проверка домашнего задания. Индивидуальный устный опрос:
– Свойства алканов. Применение алканов.
-Особенности органических соединений.
-Классификация органических соединений. Определение алканов.
b) Проверка знаний формул и названий гомологов алканов. У доски, фронтальный опрос, 2 учащихся. Проведение совместной работы (учитель и учащиеся).
c) Составление изомеров – 2,3ди метил гептан, 2,3 диметил 4 этил октан,3ди метил пентан- 2 учащихся. Проведение совместной работы (учитель и учащиеся).
d) Работа по карточкам, по 3 вариантам. (Самостоятельно).
1 вариант.
1. Гомологический ряд алканов (С1-С5).Название и молекулярная формула.
2. Составить изомер – 2, 3 диметил пентан 2, 3 метил бутан.
3. Реакция замещения метана с хлором.
2 вариант.
1.
Гомологический
ряд алканов (С5-С10).
2. Составить изомер – 2, 3 диметил бутан 1, 3,4 метил пентан.
3. Реакция получения этана (реакция Вюрца).
Вариант 3
1. Назовите по систематической номенклатуре следующие вещества:
а) СН3 – СН – СН2 – СН3; б) СН3 – СН2 – СН – СН2 – СН2 – СН3; в) СН3 – СН – СН3
I l l
СН3 СН3 СН3
2. Напишите структурные формулы следующих веществ:
а) н-бутан; б) 2-метилпропан; в) 2,4-диметилпентан, г) 3 метил 4 этилгексан
3. Напишите уравнения реакций, позволяющие осуществить следующие превращения:
3. Подготовка
к проведению лабораторной работы.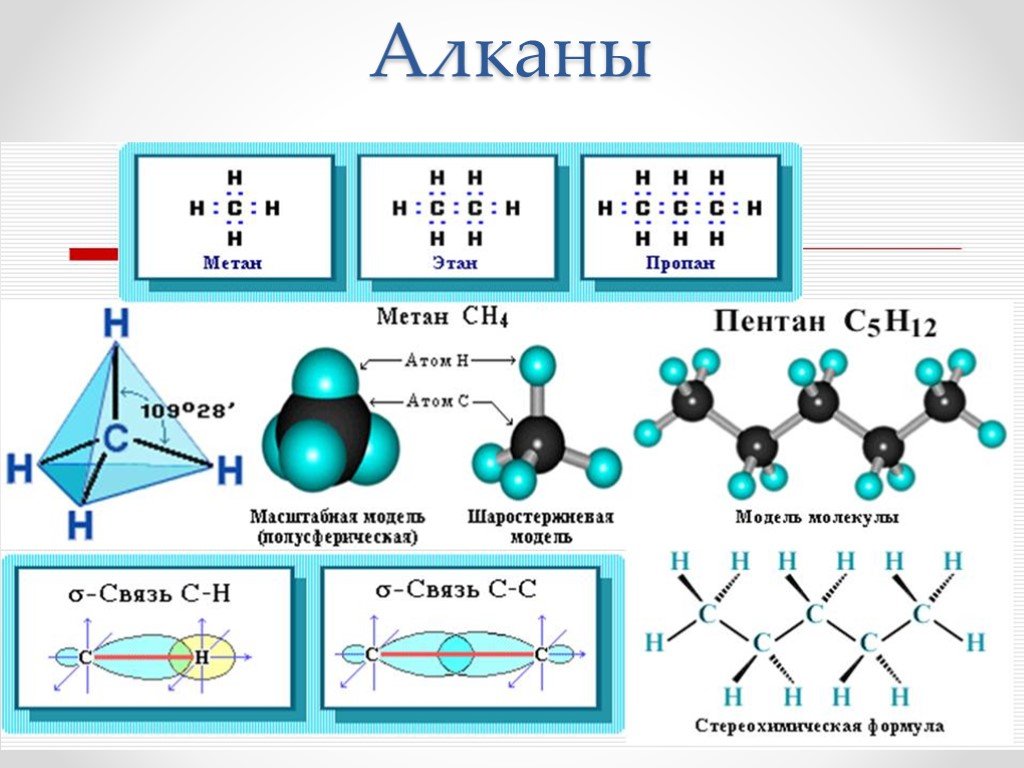
Вы изучили тему алканы. Познакомились с их получением, свойствами, применением. Научились составлять гомологи и изомеры алканов. Записывать структурные и молекулярные формулы алканов. Но как выглядят представители алканов и их галогенопроизводные их модели в пространстве мы узнаем сегодня на уроке.
Внимательно изучим инструкционную карту.
Инструкция по работе с инструкционной картой
Запишем в тетрадях тему занятия, его цель и оформить таблицу.
Тема: Изготовление моделей молекул углеводородов и их галогенопроизводных.
Цель работы:
1. Изучить пространственное строение молекул алканов и их галогенопроизводных.
2. Изготовить шаростержневые модели молекул метана, этана, бутана, хлорэтана и трихлорметана.
3. Развивать представления о существовании различных способов моделирования молекул органических соединений.
Оборудование:
разноцветный пластелин,спички.
4. Оформление таблицы в тетраде.
№ | Вещество | Структурная формула | Пространственная шаростержневая модель (Рисунок) |
1 | Метан – СН4 |
Проблемный вопрос | Деятельность учителя | Деятельность ученика |
1. Какое строение имеют алканы? | стр.68-71. рассказ. | Слушают, смотрят. |
2. Какие структурные и молекулярные формулы метана, этана, бутана, хлорэтана и трихлорметана.? | Оформление столбцов таблицы на доске – Вещество и его структурные и молекулярные формулы. рассказ. | Работа у доски 1 учащегося. Заполнение таблицы. Оформление 1-2 столбца в тетради.
|
Физ. Минутка. |
|
|
4. Как составить модель молекул акканов? | 1.Показ слайдов презентации с рассказом. 2.Инструкция по работе с инструкционной картой. | Изготовление моделей. |
5. Как зарисовать модель молекулы? | 1.Помощь в оформление
рисунка – показ рисунка на доске. 2. Беседа по выполненному заданию. | Запись 4 столбца. Беседа. |
6. Выводы по работе? | беседа с учащимися по выполненной работе. | Делают выводы по работе, записи в тетради. |
7. Контрольные вопросы по защите работы. | 1.Инструктаж по оформлению ответов в тетради. 2.краткое описание поставленных вопросов. | Делают работу по вопросам в тетради. |
6. Подведение итогов лабораторной работы.
7. Уборка рабочего места.
8. Выставление оценок за домашний материал и работу на уроке.
Инструкционная
карта.
Приложение 1.
Лабораторная работа
Тема: Изготовление моделей молекул углеводородов и их галогенопроизводных.
Цель работы:
3. Изучить пространственное строение молекул алканов и их галогенопроизводных.
4. Изготовить шаростержневые модели молекул метана, этана, бутана, хлорэтана и трихлорметана.
5. Развивать представления о существовании различных способов моделирования молекул органических соединений.
Оборудование: разноцветный пластелин,спички.
Теоретическая часть.
Представители
углеводородов и их производные можно представить в виде структурных,
электронных и молекулярных формул. В пространстве углеводороды и их производные
можно представить в виде плоскостных (полные скелетные структурные) и объемных
(масштабных и шаростержневых) моделей.
а) структурных, электронных и молекулярных формулы этана.
б) объемные – масштабные(д) и шаростержневые(г) модели этана.
Ход работы
1. Оформить в тетради таблицу.
2. Запишите в таблицу структурные и молекулярные формулы метана, этана, бутана, хлорэтана и трихлорметана.
3. В четвертом столбце зарисуйте составленную шаростержневую модель молекулы, отражающую пространственное изображение связей, используя обозначения:
пунктирная линия — связи, уходящие за плоскость рисунка,
сплошная линия — связи, лежащие в плоскости рисунка.
№ | Вещество | Структурная формула | Пространственная шаростержневая модель (Рисунок) |
1 | Метан – СН4 |
4. Составить шаростержневую модель молекулы метана:
Составить шаростержневую модель молекулы метана:
– сделать из черного пластилина один шарик, который будет символизировать атом углерода, и из белого пластилина сделать четыре шарика, которые будут символизировать атомы водорода. Причем диаметр черного шарика должен превышать диаметр белых шариков в 1,5 раза.
– на черном шарике (атом углерода) наметьте четыре равноудаленные друг от друга точки и вставьте в них палочки, к концам палочек присоедините четыре белых шарика (атомы водорода).
5. Составить шаростержневую модель молекулы трихлорметана:
– исходя из модели молекулы метана, составьте модель молекулы трихлорметана.
– сделать из синего пластилина три шарика, которые будут символизировать атом хлора. Причем диаметр синих шариков должен превышать диаметр белых шариков в 2 раза.
– отнимите от модели молекулы метана три шарика белого цвета
(символ атома водорода) и на освободившиеся места прикрепите синие шарики
(символ атома хлора).
6. Составить шаростержневую модель молекулы этана:
– сделать из черного пластилина два шарика, которые будут символизировать атом углерода, и из белого пластилина сделать шесть шариков, которые будут символизировать атомы водорода. Причем диаметр черных шариков должен превышать диаметр белых шариков в 1,5 раза.
– соедините между собой палочкой шарики черного цвета.
– на каждом черном шарике (атом углерода) наметьте три равноудаленные друг от друга точки и вставьте в них палочки, к концам палочек присоедините белый шарик (атомы водорода).
7. Составить шаростержневую модель молекулы хлорэтана:
– исходя из модели молекулы этана, составьте модель молекулы хлорэтана.
– сделать из синего пластилина шарик, которые будут символизировать атом хлора. Причем диаметр синего шарика должен превышать диаметр белых шариков в 2 раза.
– отнимите от модели молекулы этана один шарик белого цвета
(символ атома водорода) и на освободившееся место прикрепите синий шарик
(символ атома хлора).
8. Составить шаростержневую модель молекулы бутана:
– сделать из черного пластилина четыре шарика, которые будут символизировать атом углерода, и из белого пластилина сделать десять шариков, которые будут символизировать атомы водорода. Причем диаметр черных шариков должен превышать диаметр белых шариков в 1,5 раза.
– соедините между собой палочками шарики черного цвета.
– на первый и четвертый черный шарик (атом углерода) наметьте три равноудаленные друг от друга точки и вставьте в них палочки, к концам палочек присоедините белый шарик (атомы водорода). Ко второму и третьему черному шарику вставить по две палочки, к концам палочек присоедините белый шарик (атомы водорода).
Выводы по лабораторной работе: _______________________________________________________.
Контрольные вопросы по защите лабораторной работе:
1. Какие существуют способы моделирования молекул органических соединений?
2. Какие положения теории химического строения органических соединений
учитывались при составлении моделей молекул углеводородов?
Какие положения теории химического строения органических соединений
учитывались при составлении моделей молекул углеводородов?
3. Записать название соединений их структурные формулы. С6Н14, С7Н16. Составить изомеры этих соединений, назвать их.
Структура Все глинистые минералы состоят из частиц, содержащих анионные слоистые силикаты и катионы металлов. Они входят в группу филлосиликатных минералов.  Большинство из них имеют структуру «сэндвич» с 2 слоями листовых силикатов, связанных с октаэдрическими катионами. Другие, слабосвязанные катионы располагаются между слоями и сольватируются водой. Большинство из них имеют структуру «сэндвич» с 2 слоями листовых силикатов, связанных с октаэдрическими катионами. Другие, слабосвязанные катионы располагаются между слоями и сольватируются водой.Частицы глины в почве образуются в результате физического и химического выветривания силикатсодержащих пород. Существует 4 основных класса глинистых минералов.
На рисунке ниже показана структура смектит-иллитовых глин с повторяющимся звеном сэндвичевого типа. На следующем рисунке показана структура каолинитовых глин с одиночным силикатным листом, связанным с октаэдрическим слоем оксида металла в повторяющемся блоке. Ионообменник Пространство между «бутербродами» содержит воду и слабосвязанные катионы. Катионы уравновешивают общий отрицательный заряд многослойного силикатно-алюминатного блока. Когда концентрация определенного катиона снаружи частицы глины больше, чем внутри, этот катион будет диффундировать в частицу, а какой-то другой катион будет диффундировать наружу. Таким образом, глинистые минералы захватывают ионы, необходимые для роста растений, когда растения разлагаются в конце вегетационного цикла, и медленно отдают эти питательные вещества растущим растениям в течение вегетационного периода. Особенно важны для выращивания растений K + , Ca 2+ , Мг 2+ . Растения также получают меньшие количества Fe 2+ , Mn 2+ , Cu + , Zn 2+ , B 3+ , Mo 3+ .
Анионы, такие как нитраты и фосфаты, также могут накапливаться и обмениваться в пространстве между сэндвичами. Удержание воды Та же область, которая содержит слабосвязанные катионы, соли и полярные молекулы, также может удерживать большое количество воды. Некоторые глины могут удвоить свой объем за счет увеличения количества воды между слоями сэндвича. Эта вода медленно высвобождается обратно в почву вокруг корней растений. |
3D-модель атома для детей
••• Игнасио Лопес/Demand Media
Обновлено 24 апреля 2017 г. . Трехмерная модель атома дает ему лучшее представление о том, как выглядят атомы и как они работают. Для дополнительного образовательного эффекта попросите его написать короткую статью о типе атома, который он создает.
Выбор атома
••• Игнасио Лопез/Demand Media
Существует множество различных атомов, которые вы можете выбрать, начиная свой проект трехмерного атома. Некоторые атомы имеют больше компонентов, чем другие. Если у вашего ребенка короткая продолжительность концентрации внимания, используйте атом с очень небольшим количеством компонентов, чтобы ему было легче закончить проект. Например, водород — самый маленький из существующих атомов, и вы можете без особых проблем создать его трехмерную модель. Чем больше у атомов атомного веса, тем больше компонентов у атома.
Например, водород — самый маленький из существующих атомов, и вы можете без особых проблем создать его трехмерную модель. Чем больше у атомов атомного веса, тем больше компонентов у атома.
Atom Components
••• Ignacio Lopez/Demand Media
Три физически твердых компонента атома — это протоны, нейтроны и электроны. Вы можете использовать широкий спектр материалов для изготовления различных компонентов атома. Детям может понравиться использовать зефир для различных компонентов атома, но почти все, что вы можете проколоть, будет работать. Например, вы можете использовать пенопластовые шарики, глиняные или ватные шарики. Используйте предметы сферической формы для точности, так как компоненты атома являются сферами.
Идентификация компонентов
••• Игнасио Лопес/Demand Media
Ваш ребенок должен уметь определять различные компоненты атома. Когда вы используете одинаковые материалы для создания разных компонентов атома, ему может быть трудно определить, какая часть есть какая. Вы можете использовать разноцветные материалы (например, разноцветную глину для каждого компонента или можете раскрасить материалы самостоятельно. Если вы используете зефир для компонентов атома, вы можете окунуть их в смесь воды и пищевого красителя, чтобы придать им цвет. Если окраска материалов невозможна, используйте этикетки, чтобы идентифицировать каждый компонент.
Вы можете использовать разноцветные материалы (например, разноцветную глину для каждого компонента или можете раскрасить материалы самостоятельно. Если вы используете зефир для компонентов атома, вы можете окунуть их в смесь воды и пищевого красителя, чтобы придать им цвет. Если окраска материалов невозможна, используйте этикетки, чтобы идентифицировать каждый компонент.
Connections
••• Ignacio Lopez/Demand Media
Ядро атома представляет собой одну большую массу нейтронов и протонов. Вы можете использовать клей или палочки от эскимо, чтобы скрепить ядро. Электроны вращаются вокруг ядра, поэтому вам понадобится длинная проволока, воткнутая в стороны ядра, которая будет удерживать электроны на расстоянии. Вы можете использовать старые проволочные подвесы, чтобы соединить электроны с ядром, или вы можете использовать отрезки спиральной проволоки. Провод должен быть достаточно прочным, чтобы удерживать электроны на месте, не изгибаясь.
Статьи по теме
Ссылки
- Школы Sask: Компоненты атома
Об авторе
Шей Хейзелтон — профессиональный писатель, чьи статьи публикуются на различных веб-сайтах.
