Гель бактериофаг: Аптека Ригла – забронировать лекарства в аптеке и забрать самовывозом по низкой цене в Москва г.
Отофаг гель 50мл бактериофаг
Агроветзащита С.-П. НВЦ ООО (Россия)
гель для местного применения
Вакцины, сыворотки, фаги и анатоксины
H93.9 Болезнь уха неуточненная
Z29.8 Другие уточненные профилактические меры
| Гель для местного применения | 1 фл. |
| активное вещество: | |
| стерильная суспензия фаговых частиц в физиологическом растворе | |
| вспомогательные вещества: вода очищенная; карбопол; экстракт календулы |
антибактериальное местное
Местно. В домашних условиях Отофаг наносить на обрабатываемый участок непосредственно из флакона или салфеткой (ватным тампоном). Обработанный участок не мочить (гель не смывать) в течение 40 мин после применения Отофага.
В условиях приема специалистом пораженные или травмированные участки уха и других лор-органов обрабатываются Отофагом.
Отофаг безопасен при попадании на слизистую и проглатывании.
Не вносить Отофаг в закрытые очаги воспаления, не имеющие или имеющие ограниченный отток экссудата из очага (например ушитые раны). Внесение Отофага в такие очаги может привести к выраженному обострению воспалительного процесса и/или отекам и/или лимфостазу.
Схемы применения
Гигиена ушных раковин у здоровых людей, в т.ч. в период неблагоприятной эпидемиологической обстановки, при смене климатических поясов, вредных воздействиях внешней среды и других рисках заражения бактериальными инфекциями: 1 мл Отофага (одно нажатие) наносят 2–3 раза в день после гигиенических мероприятий. Длительность профилактического курса — от 7 до 14 дней. Курс рекомендуется повторять каждый месяц. Длительность применения Отофага в профилактических целях не ограничена.
Профилактика бактериальных воспалительных заболеваний уха при наличии факторов риска, в т.ч. сахарного диабета, онкологических заболеваний (особенно в период проведения лучевой и химиотерапии), сниженного местного и общего иммунитета, грибковых и вирусных инфекциях лор-органов, аутоиммунных и других системных заболеваниях:
1 мл Отофага (одно нажатие) 2–3 раза в день после гигиенических мероприятий. Длительность курса соответствует длительности действия фактора риска. При прекращении действия фактора риска рекомендуется схема применения для здоровых людей.
Длительность курса соответствует длительности действия фактора риска. При прекращении действия фактора риска рекомендуется схема применения для здоровых людей.Профилактика бактериальных воспалительных заболеваний уха (наружный и средний отит) и их рецидивов, носа (гайморит, ринит), горла (фарингит, абсцессы, ангина, хронический тонзиллит) и других респираторных заболеваниях (бронхит, эпиглоттит, грипп, ОРВИ): доза Отофага определяется врачом, исходя из конкретной клинической ситуации. Рекомендуется сочетать с применением в домашних условиях — 1 мл Отофага (одно нажатие) 3–4 раза в день после гигиенических мероприятий. Длительность курса домашних процедур — 3–4 нед. Частота повторения курсов — по рекомендации врача. Далее рекомендуется схема применения для здоровых людей.
Профилактика бактериальных осложнений при хирургических вмешательствах и других лечебных манипуляциях в области уха и других лор-органов: доза Отофага определяется врачом, исходя из конкретной клинической ситуации. Перед хирургическим вмешательством — 2–3 раза в день после гигиенических мероприятий в течение 7 дней до начала вмешательства. После хирургического вмешательства — 2–3 раза в день после гигиенических мероприятий в течение 7 дней. Далее рекомендуется схема применения для здоровых людей.
Перед хирургическим вмешательством — 2–3 раза в день после гигиенических мероприятий в течение 7 дней до начала вмешательства. После хирургического вмешательства — 2–3 раза в день после гигиенических мероприятий в течение 7 дней. Далее рекомендуется схема применения для здоровых людей.
По назначению врача в других клинических ситуациях, при которых важно обеспечить высокую антибактериальную защиту и отсутствие побочных эффектов:
врач определяет схему применения, кратность и объем использования Отофага, исходя из конкретной клинической ситуации.На начальном этапе при наличии воспалительного очага рекомендуется более частое применение Отофага с интервалом 1–2 ч.
Гель для местного применения. Во флаконе 50 мл с дозатором и защитным колпачком.
ООО «НВЦ Агроветзащита С.-П.». 141315, Россия, Московская обл., г. Сергиев Посад, ул. Центральная, 1; по заказу ООО НПЦ «МикроМир». 107031, Россия, Москва, пер. Нижний Кисельный, 5/23, стр. 1.
Реквизиты организации, уполномоченной принимать претензии от потребителей: ООО НПЦ «МикроМир».
Тел.: (499) 152-52-81, 653-79-59, (8800) 500-63-70.
www.vitabio.ru, www.micro-world.ru
24 мес
Хранить в недоступном для детей месте.
В сухом, защищенном от света месте, при температуре 2–8 °C. После начала использования допускается хранение Отофага при комнатной температуре (не более 25 °C) при условиях соблюдения стерильности и использования всего содержимого флакона в течение 60 дней. Предпочтительным местом хранения Отофага является холодильник.
Не применять по истечении срока годности, указанного на упаковке.
Отофаг гель с бактериофагами д/гиг.ушн.раковин 50мл с бесплатной доставкой на дом из «ВкусВилл»
ВкусВилл
Взаимодействие с другими лекарственными средствами • Антибактериальные препараты системного действия: Отофаг можно применять одновременно с системной антибактериальной терапией. • Антисептические, антибактериальные и другие препараты местного действия: допустимо совместное применение Отофага с растворами хлоргексидина биглюконата 0,05% и 0,2%, гидроксиметилхиноксалиндиоксида 2,0%, гелями с метронидазолом, мазями с хлорамфениколом и метилурацилом. • Допустимо последовательное применение Отофага с интервалом не менее 20 мин. после использования следующих средств: на основе окгенидина и феноксиэтанола, на основе солей полиакриловой кислоты, растворов перекиси водорода, на основе повидон-йода.
• Допустимо последовательное применение Отофага с интервалом не менее 20 мин. после использования следующих средств: на основе окгенидина и феноксиэтанола, на основе солей полиакриловой кислоты, растворов перекиси водорода, на основе повидон-йода.
Отофаг гель с бактериофагами д/гиг.ушн.раковин 50мл
ВкусВилл
1 298 руб/шт 1298.00 1298.00
от партнера «Аптека Диалог Центр»
Описание
Взаимодействие с другими лекарственными средствами
• Антибактериальные препараты системного действия: Отофаг можно применять одновременно с системной антибактериальной терапией.
• Антисептические, антибактериальные и другие препараты местного действия: допустимо совместное применение Отофага с растворами хлоргексидина биглюконата 0,05% и 0,2%, гидроксиметилхиноксалиндиоксида 2,0%, гелями с метронидазолом, мазями с хлорамфениколом и метилурацилом.
• Допустимо последовательное применение Отофага с интервалом не менее 20 мин. после использования следующих средств: на основе окгенидина и феноксиэтанола, на основе солей полиакриловой кислоты, растворов перекиси водорода, на основе повидон-йода.
Показания к применению
Повышенная чувствительность к компонентам Отофага.
ПроизводительМикромир НПЦ
МНН/Действующее вещество Форма выпуска Количество в упаковке Состав Способ приготовления Особые условия Побочные действия Противопоказания Условия хранения Срок годности Рецептурный препарат ПартнерАптека Диалог Центр
Данный товар может поставляться сразу несколькими производителями. По этой причине информация отличаться. Соответствующие конкретному товару данные всегда представлены на этикетке. Внешний вид продукта в магазине также может отличаться от изображения на фото.
По этой причине информация отличаться. Соответствующие конкретному товару данные всегда представлены на этикетке. Внешний вид продукта в магазине также может отличаться от изображения на фото.
Показать наличие в магазинах
Гидрогели, доставляющие бактериофаги: текущий прогресс в борьбе с антибиотикорезистентными бактериальными инфекциями и перспективы. Мед. Рез. 2020;40:459–463. doi: 10.1002/med.21593. [PubMed] [CrossRef] [Google Scholar]
2. Balcão V.M., Moreira A.R., Moutinho C.G., Chaud M.V., Tubino M., Vila M.M.D.C. Структурно-функциональная стабилизация фаговых частиц в углеводных матрицах для бактериального биосенсора. фермент. микроб. Технол. 2013;53:55–69. doi: 10.1016/j.enzmictec.2013.03.001. [PubMed] [CrossRef] [Google Scholar]
3. Ventola C.L. Кризис устойчивости к антибиотикам: Часть 1: Причины и угрозы. фарм. тер. 2015;40:277–283. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Chang R. Y.K., Wallin M., Lin Y., Leung S.S.Y., Wang H., Morales S., Chan H.K. Фаготерапия респираторных инфекций. Доп. Наркотик Делив. 2018; 133:76–86. doi: 10.1016/j.addr.2018.08.001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Y.K., Wallin M., Lin Y., Leung S.S.Y., Wang H., Morales S., Chan H.K. Фаготерапия респираторных инфекций. Доп. Наркотик Делив. 2018; 133:76–86. doi: 10.1016/j.addr.2018.08.001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Huh H., Wong S., St Jean J., Slavcev R. Взаимодействие бактериофагов с тканями млекопитающих: терапевтические применения. Доп. Наркотик Делив. 2019; 145:4–17. doi: 10.1016/j.addr.2019.01.003. [PubMed] [CrossRef] [Google Scholar]
6. Мело Л.Д.Р., Оливейра Х., Пирес Д.П., Дабровска К., Азередо Дж. Эффективность фаготерапии: обзор доклинических исследований за последние 10 лет. крит. Преподобный Микробиолог. 2020;46:78–99. doi: 10.1080/1040841x.2020.1729695. [PubMed] [CrossRef] [Академия Google]
7. Гриль М.Ф., Маганти Р.К. Нейротоксические эффекты, связанные с использованием антибиотиков: соображения управления. бр. Дж. Клин. Фармакол. 2011;72:381–393. doi: 10.1111/j.1365-2125.2011.03991.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
8. Spapen H., Jacobs R., Van Gorp V., Troubleyn J., Honoré P.M. Почечные и неврологические побочные эффекты колистина у пациентов в критическом состоянии. Анна. Интенсивная терапия. 2011;1:14. дои: 10.1186/2110-5820-1-14. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Spapen H., Jacobs R., Van Gorp V., Troubleyn J., Honoré P.M. Почечные и неврологические побочные эффекты колистина у пациентов в критическом состоянии. Анна. Интенсивная терапия. 2011;1:14. дои: 10.1186/2110-5820-1-14. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Лин Ю., Чанг Р.Ю.К., Бриттон В.Дж., Моралес С., Каттер Э., Чан Х.-К. Синергизм комбинации распыляемого фага PEV20 и ципрофлоксацина против Pseudomonas aeruginosa . Междунар. Дж. Фарм. 2018; 551: 158–165. doi: 10.1016/j.ijpharm.2018.09.024. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Lin Y., Chang R.Y.K., Britton W.J., Morales S., Kutter E., Li J., Chan H.K. Ингаляционные комбинированные порошковые препараты фага и ципрофлоксацина для P. aeruginosa респираторные инфекции. Евро. Дж. Фарм. Биофарм. 2019; 142: 543–552. doi: 10.1016/j.ejpb.2019.08.004. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Lin Y., Quan D., Yoon Kyung Chang R. , Chow MYT., Wang Y., Li M., Morales S., Britton W.J. , Каттер Э., Ли Дж. и др. Синергическая активность фага PEV20-ципрофлоксацина в виде порошка комбинированного препарата — исследование, подтверждающее принцип действия, на модели легочной инфекции P. aeruginosa . Евро. Дж. Фарм. Биофарм. 2021; 158: 166–171. doi: 10.1016/j.ejpb.2020.11.019. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Chow MYT., Wang Y., Li M., Morales S., Britton W.J. , Каттер Э., Ли Дж. и др. Синергическая активность фага PEV20-ципрофлоксацина в виде порошка комбинированного препарата — исследование, подтверждающее принцип действия, на модели легочной инфекции P. aeruginosa . Евро. Дж. Фарм. Биофарм. 2021; 158: 166–171. doi: 10.1016/j.ejpb.2020.11.019. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Дахил К.Х., Рахим Р.А., Нила В.К., Аль-Обаиди Дж.Р., Хун Т.Г., Иса М.Н.М., Юсофф К. Геномный анализ двух новых биопленок, разлагающих метициллинрезистентные Staphylococcus aureus фаги. БМС микробиол. 2019;19:114. doi: 10.1186/s12866-019-1484-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Фонг С.А., Дриллинг А., Моралес С., Корнет М.Е., Вудворт Б.А., Фоккенс В.Дж., Псалтис А.Дж., Врейгде С., Вормолд П.- Дж. Активность бактериофагов в удалении биопленок Pseudomonas aeruginosa изолируется от пациентов с хроническим риносинуситом. Передний. Заражение клетки. микробиол. 2017;7:418. doi: 10.3389/fcimb.2017.00418. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Передний. Заражение клетки. микробиол. 2017;7:418. doi: 10.3389/fcimb.2017.00418. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Chang R.Y.K., Das T., Manos J., Kutter E., Morales S., Chan H.K. Комбинированное лечение бактериофагом PEV20 и ципрофлоксацином способствует удалению биопленки Pseudomonas aeruginosa , выделенной у пациентов с муковисцидозом и раневых больных. AAPS J. 2019; 21:49. doi: 10.1208/s12248-019-0315-0. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Гебрейоханнес Г., Ньерере А., Бии К., Сбхату Д.Б. Проблемы вмешательства, лечения и антибиотикорезистентности биопленкообразующих микроорганизмов. Гелион. 2019;5:e02192. doi: 10.1016/j.heliyon.2019.e02192. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Harper D.R., Parracho H.M.R.T., Walker J., Sharp R., Hughes G., Werthén M., Lehman S., Morales S. Bacteriophages and биопленки. Антибиотики (Базель) 2014;3:270–284. дои: 10.3390/антибиотики3030270. [CrossRef] [Google Scholar]
[CrossRef] [Google Scholar]
17. Абедон С.Т., Куль С.Дж., Бласдел Б.Г., Каттер Э.М. Фаговое лечение инфекций человека. Бактериофаг. 2011; 1:66–85. doi: 10.4161/bact.1.2.15845. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
18. Мерабишвили М., Пирнай Ж.П., Вербекен Г., Чанишвили Н., Тедиашвили М., Лашхи Н., Глонти Т., Крылов В., Маст Дж., Ван Пэрис Л. и др. Контролируемое качество мелкосерийного производства четко определенного коктейля бактериофагов для использования в клинических испытаниях на людях. ПЛОС ОДИН. 2009 г.;4:e4944. doi: 10.1371/journal.pone.0004944. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
19. Rhoads D.D., Wolcott R.D., Kuskowski M.A., Wolcott B.M., Ward L.S., Sulakvelidze A. Бактериофаговая терапия венозных язв нижних конечностей у человека: результаты фазы Я испытание безопасности. Дж. Уход за ранами. 2009; 18: 237–243. doi: 10.12968/jowc.2009.18.6.42801. [PubMed] [CrossRef] [Google Scholar]
20. Райт А., Хокинс Ч. Х., Ангард Э.Е., Харпер Д.Р. Контролируемое клиническое исследование лечебного препарата бактериофага при хроническом отите, вызванном антибиотикорезистентностью Синегнойная палочка; предварительный отчет об эффективности. клин. Отоларингол. 2009; 34: 349–357. doi: 10.1111/j.1749-4486.2009.01973.x. [PubMed] [CrossRef] [Google Scholar]
Х., Ангард Э.Е., Харпер Д.Р. Контролируемое клиническое исследование лечебного препарата бактериофага при хроническом отите, вызванном антибиотикорезистентностью Синегнойная палочка; предварительный отчет об эффективности. клин. Отоларингол. 2009; 34: 349–357. doi: 10.1111/j.1749-4486.2009.01973.x. [PubMed] [CrossRef] [Google Scholar]
21. Ooi M.L., Drilling A.J., Morales S., Fong S., Moraitis S., Macias-Valle L., Vreugde S., Psaltis A.J., Wormald P.J. Безопасность и переносимость бактериофаговой терапии хронического риносинусита, вызванного Staphylococcus aureus . JAMA Отоларингол. Хирургия головы и шеи. 2019; 145:723–729. дои: 10.1001/jamaoto.2019.1191. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
22. Chang R.Y.K., Kwok P.C.L., Khanal D., Morales S., Kutter E., Li J., Chan H.K. Ингаляционные порошки бактериофагов: температура стеклования и стабилизация биоактивности. биоинж. Перевод Мед. 2020;5:e10159. doi: 10.1002/btm2.10159. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
23. Clark W.A. Сравнение нескольких методов сохранения бактериофагов. Дж. Заявл. микробиол. 1962; 10: 466–471. дои: 10.1128/AM.10.5.466-471.1962. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Clark W.A. Сравнение нескольких методов сохранения бактериофагов. Дж. Заявл. микробиол. 1962; 10: 466–471. дои: 10.1128/AM.10.5.466-471.1962. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24. Chang R.Y., Wong J., Mathai A., Morales S., Kutter E., Britton W., Li J., Chan H.K. Производство высокостабильных составов фагов, высушенных распылением, для лечения легочной инфекции Pseudomonas aeruginosa . Евро. Дж. Фарм. Биофарм. 2017; 121:1–13. doi: 10.1016/j.ejpb.2017.09.002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Chang R.Y.K., Wallin M., Kutter E., Morales S., Britton W., Li J., Chan H.K. Стабильность хранения ингаляционных порошков фагов, содержащих лактозу, в условиях окружающей среды. Междунар. Дж. Фарм. 2019;560:11–18. doi: 10.1016/j.ijpharm.2019.01.050. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
26. Kaur P., Gondil V.S., Chhibber S. Новая раневая повязка, состоящая из гибридной гидрогелевой мембраны PVA-SA для местной доставки бактериофагов и антибиотиков. Междунар. Дж. Фарм. 2019;572:118779. doi: 10.1016/j.ijpharm.2019.118779. [PubMed] [CrossRef] [Google Scholar]
Междунар. Дж. Фарм. 2019;572:118779. doi: 10.1016/j.ijpharm.2019.118779. [PubMed] [CrossRef] [Google Scholar]
27. Kumari S., Harjai K., Chhibber S. Местное лечение Klebsiella pneumoniae B5055, индуцированной ожоговой раневой инфекцией у мышей, с использованием натуральных продуктов. Дж. Заразить. Дев. Попытки. 2010;4:367–377. [PubMed] [Академия Google]
28. Кумари С., Харджай К., Чхиббер С. Бактериофаг против противомикробных препаратов для лечения мышиной ожоговой раневой инфекции, вызванной Klebsiella pneumoniae B5055. Дж. Мед. микробиол. 2011;60:205–210. doi: 10.1099/jmm.0.018580-0. [PubMed] [CrossRef] [Google Scholar]
29. Barros J.A.R., Melo L.D.R.D., Silva R.A.R.D., Ferraz M.P., Azeredo J.C.V.D.R., Pinheiro V.M.D.C., Colaço B.J.A., Fernandes M.H.R.R.R.R.ReLELALER. в качестве новой системы доставки для предотвращения инфекций, связанных с ортопедическими имплантатами. Наномед. нанотехнологии. биол. Мед. 2020;24:102145. дои: 10.1016/j. nano.2019.102145. [PubMed] [CrossRef] [Google Scholar]
nano.2019.102145. [PubMed] [CrossRef] [Google Scholar]
30. Wroe J.A., Johnson C.T., García A.J. Бактериофаги, доставляющие гидрогели, уменьшают образование биопленок in vitro и инфекцию in vivo. Дж. Биомед. Матер. Рез. Часть А. 2020; 108:39–49. doi: 10.1002/jbm.a.36790. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Cobb L.H., Park J., Swanson E.A., Beard M.C., McCabe E.M., Rourke A.S., Seo K.S., Olivier A.K., Priddy L.B. Модифицированный CRISPR-Cas9 бактериофаг для лечения Staphylococcus aureus вызывал остеомиелит и инфекцию мягких тканей. ПЛОС ОДИН. 2019;14:e0220421. doi: 10.1371/journal.pone.0220421. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Ахмед Э. М. Гидрогель: подготовка, характеристика и применение: обзор. Дж. Адв. Рез. 2015;6:105–121. doi: 10.1016/j.jare.2013.07.006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
33. Перес-Луна В.Х., Гонсалес-Рейносо О. Инкапсулирование биологических агентов в гидрогелях для терапевтических применений. Гели. 2018;4:61. дои: 10.3390/гельс4030061. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
Гели. 2018;4:61. дои: 10.3390/гельс4030061. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
34. Кало Э., Хуторянский В.В. Биомедицинские применения гидрогелей: обзор патентов и коммерческих продуктов. Евро. Полим. Дж. 2015; 65: 252–267. doi: 10.1016/j.eurpolymj.2014.11.024. [CrossRef][Google Scholar]
35. Нараянасвами Р., Торчилин В.П. Гидрогели и их применение в адресной доставке лекарств. Молекулы. 2019;24:603. doi: 10.3390/молекулы24030603. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
36. Ли Дж., Муни Д.Дж. Разработка гидрогелей для контролируемой доставки лекарств. Нац. Преподобный Матер. 2016;1:16071. doi: 10.1038/natrevmats.2016.71. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Lee K.Y., Mooney D.J. Альгинат: свойства и биомедицинские применения. прог. Полим. науч. 2012; 37: 106–126. doi: 10.1016/j.progpolymsci.2011.06.003. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
38. Маррелла А. , Лагаццо А., Деллакаса Э., Пасквини К., Финоккио Э., Барберис Ф., Пасторино Л., Джаннони П. , Scaglione S. Трехмерный пористый желатин/гидрогель ПВА в качестве заменителя мениска с использованием микрочастиц альгината в качестве порообразователя. Полимеры (Базель) 2018;10:380. дои: 10.3390/полим10040380. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Лагаццо А., Деллакаса Э., Пасквини К., Финоккио Э., Барберис Ф., Пасторино Л., Джаннони П. , Scaglione S. Трехмерный пористый желатин/гидрогель ПВА в качестве заменителя мениска с использованием микрочастиц альгината в качестве порообразователя. Полимеры (Базель) 2018;10:380. дои: 10.3390/полим10040380. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Cheng Y., Shi X., Jiang X., Wang X., Qin H. Возможность печати производного целлюлозы для экструзионной 3D-печати: Применение на биоразлагаемом материале поддержки. Передний. Матер. 2020;7 doi: 10.3389/fmats.2020.00086. [CrossRef] [Google Scholar]
40. Янсен Л.Э., Негрон-Пиньейро Л.Дж., Галарза С., Пейтон С.Р. Контроль кинетики тиол-малеимидной реакции в гидрогелевых сетях ПЭГ. Акта Биоматер. 2018;70:120–128. doi: 10.1016/j.actbio.2018.01.043. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41. Johnson C., Dinjaski N., Prieto M., García A. Инкапсуляция бактериофага в гидрогелях из полиэтиленгликоля значительно снижает количество бактерий в модели восстановления кости, связанной с имплантатом. Игарсс. 2014;2014:281. [Google Scholar]
Игарсс. 2014;2014:281. [Google Scholar]
42. Liu Y., Vrana N.E., Cahill P.A., McGuinness G.B. Физически сшитые композитные гидрогели ПВС с природными макромолекулами: структура, механические свойства и совместимость с эндотелиальными клетками. Дж. Биомед. Матер. Рез. Б заявл. Биоматер. 2009 г.;90:492–502. doi: 10.1002/jbm.b.31310. [PubMed] [CrossRef] [Google Scholar]
43. Milo S., Hathaway H., Nzakizwanayo J., Alves D.R., Esteban P.P., Jones B.V., Jenkins A.T.A. Профилактика инкрустации и закупорки мочевых катетеров с помощью Proteus mirabilis посредством pH-зависимого высвобождения бактериофага. Дж. Матер. хим. Б. 2017;5:5403–5411. doi: 10.1039/C7TB01302G. [PubMed] [CrossRef] [Google Scholar]
44. Элтон Р.К. Гибкие смазывающие органические покрытия. США5179174А. Патент США. 1993 12 января;
45. Чжоу Г., Ма С., Чжан Г. Синтез сополимеров полиуретана и поли(этиленгликоля) макроинфертерами и их устойчивость к белкам. Полим. хим. 2011;2:1409–1414. doi: 10.1039/c1py00016k. [CrossRef] [Google Scholar]
doi: 10.1039/c1py00016k. [CrossRef] [Google Scholar]
46. Хэтэуэй Х., Алвес Д.Р., Бин Дж., Эстебан П.П., Уади К., Саттон Дж.М., Дженкинс А.Т. Поли(N-изопропилакриламид-со-аллиламин) (PNIPAM-со-ALA) наносферы для термически запускаемого высвобождения бактериофага K. Eur. Дж. Фарм. Биофарм. 2015;96: 437–441. doi: 10.1016/j.ejpb.2015.09.013. [PubMed] [CrossRef] [Google Scholar]
47. Роуч Б., Новер А., Атешян Г., Хунг К. Биоматериалы природы для передовых устройств и методов лечения. Джон Уайли и сыновья; Хобокен, штат Нью-Джерси, США: 2016. Характеристика агарозного гидрогеля для применения в регенеративной медицине: основное внимание уделяется инженерному хрящу; стр. 258–273. [CrossRef] [Google Scholar]
48. Bean J.E., Alves D.R., Laabei M., Esteban P.P., Thet N.T., Enright M.C., Jenkins A.T.A. Триггерное высвобождение бактериофага К из матриксов гидрогеля сагароза/гиалуронан с помощью Staphylococcus aureus факторы вирулентности. хим. Матер. 2014; 26:7201–7208. doi: 10.1021/см503974г. [CrossRef] [Google Scholar]
doi: 10.1021/см503974г. [CrossRef] [Google Scholar]
49. Chhibber S., Kaur T., Kaur S. Существенная роль кальция в инфекционном процессе метициллин-резистентного Staphylococcus aureus бактериофага. J. Основная микробиол. 2014;54:775–780. doi: 10.1002/jobm.201300051. [PubMed] [CrossRef] [Google Scholar]
50. Бурден Г., Шмитт Б., Марвин Гай Л., Джермонд Дж.-Э., Зубер С., Мишо Л., Рейтелер Г., Брюссов Х. Амплификация и очистка Т4-подобных фагов кишечной палочки для фаговой терапии: от лаборатории до экспериментального масштаба. заявл. Окружающая среда. микробиол. 2014;80:1469–1476. doi: 10.1128/AEM.03357-13. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
51. Фелпс Э.А., Энемчукву Н.О., Фиоре В.Ф., Си Дж.К., Мурти Н., Сульчек Т.А., Баркер Т.Х., Гарсия А.Дж. Сшитый малеимидом биоактивный гидрогель ПЭГ демонстрирует улучшенную кинетику реакции и перекрестное связывание для инкапсуляции клеток и доставки in situ. Доп. Матер. 2012; 24:64–70. doi: 10. 1002/adma.201103574. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
1002/adma.201103574. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Фостер Г.А., Хеден Д.М., Гонсалес-Гарсия К., Салмерон-Санчес М., Ширван Х., Гарсия А.Дж. Разлагаемые протеазой микрогели для доставки белка для васкуляризации. Биоматериалы. 2017;113:170–175. doi: 10.1016/j.biomaterials.2016.10.044. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Фу В., Форстер Т., Майер О., Кертин Дж.Дж., Леман С.М., Донлан Р.М. Бактериофаговый коктейль для предотвращения образования биопленки Pseudomonas aeruginosa на катетерах в модельной системе in vitro. Антимикроб. Агенты Чемотер. 2010;54:397–404. doi: 10.1128/AAC.00669-09. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
54. Карсон Л., Горман С.П., Гилмор Б.Ф. Использование литических бактериофагов для предотвращения и уничтожения биопленок Proteus mirabilis и Escherichia coli . ФЭМС Иммунол. Мед. микробиол. 2010;59:447–455. doi: 10.1111/j.1574-695X. 2010.00696.x. [PubMed] [CrossRef] [Google Scholar]
2010.00696.x. [PubMed] [CrossRef] [Google Scholar]
55. Кертин Дж.Дж., Донлан Р.М. Использование бактериофагов для уменьшения образования катетер-ассоциированных биопленок с помощью Staphylococcus epidermidis . Антимикроб. Агенты Чемотер. 2006; 50:1268–1275. doi: 10.1128/AAC.50.4.1268-1275.2006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
56. Lehman S.M., Donlan R.M. Опосредованный бактериофагами контроль биопленки двух видов, образованной микроорганизмами, вызывающими инфекции мочевыводящих путей, связанные с катетером, в модели мочевого катетера in vitro. Антимикроб. Агенты Чемотер. 2015;59: 1127–1137. doi: 10.1128/AAC.03786-14. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
57. Родни М., Донлан С.М.Л., Андрес Дж. Гарсия Контролируемое ковалентное присоединение биактивного бактериофага для регуляции развития биопленки. US9457132B2. Патент США. 2016 4 октября;
58. Малик Д.Дж., Соколов И.Дж., Виннер Г.К., Манкузо Ф. , Синкерруи С., Владисавлевич Г.Т., Клоки М.Р.Дж., Гартон Н.Дж., Стэпли А.Г.Ф., Кирпичникова А. Составление, стабилизация и инкапсуляция бактериофага для фаговой терапии. Доп. Коллоидный интерфейс Sci. 2017;249: 100–133. doi: 10.1016/j.cis.2017.05.014. [PubMed] [CrossRef] [Google Scholar]
, Синкерруи С., Владисавлевич Г.Т., Клоки М.Р.Дж., Гартон Н.Дж., Стэпли А.Г.Ф., Кирпичникова А. Составление, стабилизация и инкапсуляция бактериофага для фаговой терапии. Доп. Коллоидный интерфейс Sci. 2017;249: 100–133. doi: 10.1016/j.cis.2017.05.014. [PubMed] [CrossRef] [Google Scholar]
59. Мерабишвили М., Вервает С., Пирнай Дж.П., Де Вос Д., Вербекен Г., Маст Дж., Чанишвили Н., Ванечутте М. Стабильность Staphylococcus aureus фаг ISP после сушки вымораживанием (лиофилизация) PLoS ONE. 2013;8:e68797. doi: 10.1371/journal.pone.0068797. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
60. Miguel S.P., Ribeiro M.P., Brancal H., Coutinho P., Correia I.J. Термочувствительный хитозан-агарозный гидрогель для регенерации кожи. углевод. Полим. 2014; 111:366–373. doi: 10.1016/j.carbpol.2014.04.093. [PubMed] [CrossRef] [Google Scholar]
. Вебер-Домбровска Б., Гурски А. Факторы, определяющие стабильность/активность фага: проблемы практического применения фагов. Эксперт Преподобный Анти-Инфект. тер. 2019;17:583–606. doi: 10.1080/14787210.2019.1646126. [PubMed] [CrossRef] [Google Scholar]
Эксперт Преподобный Анти-Инфект. тер. 2019;17:583–606. doi: 10.1080/14787210.2019.1646126. [PubMed] [CrossRef] [Google Scholar]
62. Чанг Р.Ю.К., Моралес С., Окамото Ю., Чан Х.К. Местное применение бактериофагов для лечения раневых инфекций. Перевод Рез. 2020; 220: 153–166. doi: 10.1016/j.trsl.2020.03.010. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
63. Карбол Дж., Тан П., Варма Ю., Осборн Д. Разработка продуктов для местного применения, содержащих живые микроорганизмы в качестве активного ингредиента. фарм. Технол. Евро. 2018;42:24–27. [Google Scholar]
64. McConoughey S.J., Howlin R., Granger J.F., Manring M.M., Calhoun J.H., Shirtliff M., Kathju S., Stoodley P. Биопленки при перипротезных ортопедических инфекциях. Будущая микробиология. 2014; 9: 987–1007. doi: 10.2217/fmb.14.64. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
65. Caplin J.D., García A.J. Имплантируемые противомикробные биоматериалы для местной доставки лекарств в моделях костной инфекции. Акта Биоматер. 2019;93:2–11. doi: 10.1016/j.actbio.2019.01.015. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Акта Биоматер. 2019;93:2–11. doi: 10.1016/j.actbio.2019.01.015. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
66. Николь Л.Е. Катетерассоциированные инфекции мочевыводящих путей. Антимикроб. Сопротивляться. Заразить. Контроль. 2014;3:23. doi: 10.1186/2047-2994-3-23. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
67. Ma L., Green S.I., Trautner B.W., Ramig R.F., Maresso A.W. Металлы усиливают уничтожение бактерий бактериофагом в крови человека. науч. Отчет 2018; 8: 2326. doi: 10.1038/s41598-018-20698-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
68. Гарибальди Р.А., Муни Б.Р., Эпштейн Б.Дж., Бритт М.Р. Оценка ежедневного бактериологического мониторинга для выявления предотвратимых эпизодов катетер-ассоциированной инфекции мочевыводящих путей. Заразить. Контроль. 1982; 3: 466–470. doi: 10.1017/S0195941700056599. [PubMed] [CrossRef] [Google Scholar]
69. Tambyah P.A., Halvorson K.T., Maki D.G. Проспективное исследование патогенеза катетер-ассоциированных инфекций мочевыводящих путей.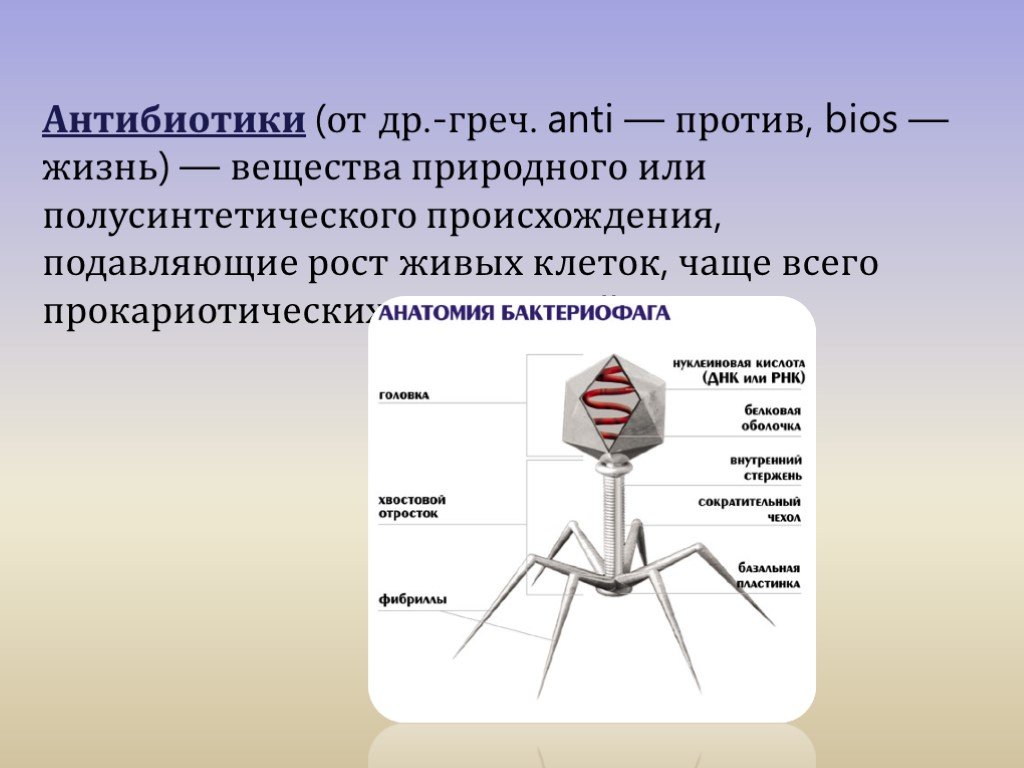 Мэйо Клин. проц. 1999;74:131–136. дои: 10.4065/74.2.131. [PubMed] [CrossRef] [Google Scholar]
Мэйо Клин. проц. 1999;74:131–136. дои: 10.4065/74.2.131. [PubMed] [CrossRef] [Google Scholar]
70. Алгбури А., Комито Н., Каштанов Д., Дикс Л.М.Т., Чикиндас М.Л. Контроль образования биопленки: антибиотики и не только. заявл. Окружающая среда. микробиол. 2017; 83:e02508–e02516. doi: 10.1128/aem.02508-16. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
71. Хоулин Р.П., Кэти К., Холл-Студли Л., Корнелиус В., Дуиньян К., Аллан Р.Н., Фернандес Б.О., Барро Н., Брюс К.Д., Джеффрис Дж. и др. Низкие дозы оксида азота в качестве целевой антибиопленочной дополнительной терапии для лечения хронической Инфекция Pseudomonas aeruginosa при муковисцидозе. Мол. тер. 2017;25:2104–2116. doi: 10.1016/j.ymthe.2017.06.021. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
72. Rouillard K.R., Markovetz M.R., Bacudio L.G., Hill D.B., Schoenfisch M.H. Pseudomonas aeruginosa уничтожение биопленки с помощью циклодекстринов, высвобождающих оксид азота. Заражение АКС. Дис. 2020; 6: 1940–1950. doi: 10.1021/acsinfecdis.0c00246. [PubMed] [CrossRef] [Google Scholar]
Заражение АКС. Дис. 2020; 6: 1940–1950. doi: 10.1021/acsinfecdis.0c00246. [PubMed] [CrossRef] [Google Scholar]
73. Колодкин-Гал И., Ромеро Д., Цао С., Кларди Дж., Колтер Р., Лосик Р. D-аминокислоты запускают разборку биопленки. Наука. 2010;328:627–629. doi: 10.1126/science.1188628. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
74. Хохбаум А.И., Колодкин-Гал И., Фоулстон Л., Колтер Р., Айзенберг Дж., Лосик Р. Ингибирующие эффекты D-аминокислот о развитии биопленки Staphylococcus aureus . Дж. Бактериол. 2011;193:5616–5622. doi: 10.1128/JB.05534-11. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
75. Мерабишвили М., Монсерез Р., ван Беллегхем Дж., Роуз Т., Дженнес С., Де Вос Д., Вербекен Г., Ванихутте М., Пирнай Дж. П. Стабильность бактериофагов в средствах по уходу за ожоговыми ранами. ПЛОС ОДИН. 2017;12:e0182121. doi: 10.1371/journal.pone.0182121. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
76. Бесса Л. Дж., Фазии П., Ди Джулио М., Челлини Л. Бактериальные изоляты из инфицированных ран и характер их чувствительности к антибиотикам: некоторые замечания о раневой инфекции. Междунар. Раненый Дж. 2015; 12:47–52. doi: 10.1111/iwj.12049. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Дж., Фазии П., Ди Джулио М., Челлини Л. Бактериальные изоляты из инфицированных ран и характер их чувствительности к антибиотикам: некоторые замечания о раневой инфекции. Междунар. Раненый Дж. 2015; 12:47–52. doi: 10.1111/iwj.12049. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
77. Maciejewska B., Olszak T., Drulis-Kawa Z. Применение бактериофагов по сравнению с фаговыми ферментами для борьбы и лечения бактериальных инфекций: амбициозная и одновременно реалистичное приложение? заявл. микробиол. Биотехнолог. 2018;102:2563–2581. doi: 10.1007/s00253-018-8811-1. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
78. Weber M., Steinle H., Golombek S., Hann L., Schlensak C., Wendel H.P., Avci-Adali M. Биоматериалы, контактирующие с кровью: оценка гемосовместимости in vitro. Передний. биоинж. Биотехнолог. 2018;6:99. doi: 10.3389/fbioe.2018.00099. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
79. Александр Н., Рибейро Дж., Гертнер А. , Перейра Т., Аморим И., Фрагозо Дж., Лопес А., Фернандес Дж. , Коста Э., Сантос-Сильва А. и др. Биосовместимость и гемосовместимость гидрогеля поливинилового спирта, используемого для трансплантации сосудов – исследования in vitro и in vivo. Дж. Биомед. Матер. Рез. Часть А. 2014; 102:4262–4275. дои: 10.1002/jbm.a.35098. [PubMed] [CrossRef] [Google Scholar]
, Перейра Т., Аморим И., Фрагозо Дж., Лопес А., Фернандес Дж. , Коста Э., Сантос-Сильва А. и др. Биосовместимость и гемосовместимость гидрогеля поливинилового спирта, используемого для трансплантации сосудов – исследования in vitro и in vivo. Дж. Биомед. Матер. Рез. Часть А. 2014; 102:4262–4275. дои: 10.1002/jbm.a.35098. [PubMed] [CrossRef] [Google Scholar]
80. Hietala V., Horsma-Heikkinen J., Carron A., Skurnik M., Kiljunen S. Удаление эндо- и энтеротоксинов из препаратов бактериофагов. Передний. микробиол. 2019; 10 doi: 10.3389/fmicb.2019.01674. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
Фагодерм Бактериофаг гель 50 мл для защиты кожи от бактериальной инфекции: купить в Kalinka-Store
ФАГОДЕРМ гель с бактериофагами 50 мл
Фагодерм Бактериофаг 50 мл.
Гель Фагодерм быстро и эффективно лечит кожные заболевания, нормализуя местную и общую микрофлору организма и надежно защищая его от бактериальной инфекции. Бактериофаги — это вирусы, убивающие бактерии избирательно: каждый тип бактериофага активен только в отношении определенных видов бактерий.
Бактериофаги — это вирусы, убивающие бактерии избирательно: каждый тип бактериофага активен только в отношении определенных видов бактерий.
Применяемые в клинической практике бактериофаги уничтожают патогенные бактерии, не влияют на нормальную микробную флору человека и не взаимодействуют с его органами и системами.
Позволяет назначать фаги всем категориям больных как эффективное и безопасное антибактериальное средство для лечения и профилактики. Практически оправдан профилактический прием бактериофагов в тех случаях, когда отсутствуют клинические признаки бактериальной инфекции, а применение антибиотиков нежелательно из-за их побочных эффектов.
Важным условием эффективной фаготерапии является предварительное определение чувствительности возбудителя к бактериофагу, а также раннее применение препарата.
Действующее вещество: стерильная взвесь фаговых частиц в физиологическом растворе, вода очищенная, карбопол, экстракт календулы, нипазол. Происхождение: Россия.
Происхождение: Россия.
Гель Фагодерм содержит комплекс из 47 видов бактериофагов, подавляющих рост следующих патогенных бактерий:
• Acinetobacter baumannii
• Bacteroides fragilis
• Bacteroides spp.
• Citrobacter freundii
• Corynebacterium spp.
• Enterobacter spp.
• Escherichia coli
• Klebsiella spp.
• Propionibacterium acnes
• Providencia rettgeri
• Proteus mirabilis
• Proteus vulgaris
• Pseudomonas aeruginosa
• Staphylococcus aureus
• Staphylococcoccus aremencus
. Antodelers
. Antodelress
. Antodelress
. абсолютно безвредны для вашего организма, но высокоэффективны против болезнетворных бактерий. Гель Фагодерм представляет собой комплекс из 47 полезных живых бактериофагов; показывает свою высокую эффективность в тех случаях, когда даже самые сильные антибиотики не справляются с болезнью. В отличие от искусственных препаратов, Фагодерм не наносит вреда вашему здоровью, а, наоборот, создает все условия для комплексного оздоровления вашего организма.
Фагодерм наносят тонким слоем (не втирая) 2-3 раза в сутки на кожу или перевязочный материал после гигиенических мероприятий. Не мочить обработанный участок кожи (не смывать гель) в течение 40 минут после нанесения Фагодерма. Дозы Фагодерма определяются индивидуально в зависимости от площади обрабатываемого участка кожи. См. полную инструкцию по применению, прилагаемую к препарату.
Бактериофаги (от др.-греч. «поедатели бактерий») – вирусы, убивающие бактерии избирательно: каждый вид бактериофагов активен только по отношению к определенным видам бактерий и нейтрален по отношению к нормальной микробной флоре человека и не взаимодействует с его органами и системы.
Гель Phagoderm представляет собой комплекс из 47 полезных живых бактериофагов. Применяется для нормализации местной и общей микрофлоры кожи и надежной защиты ее от бактериального заражения.
Фаги можно назначать всем категориям как эффективное и безопасное антибактериальное средство для лечения и профилактики, в том числе в сочетании с антибиотиками.
Комбинированное и защитное действие бактериофагов помогает организму бороться с инфекцией и ее последствиями.
Профилактическое применение бактериофагов предотвращает новые случаи инфекционного воспаления или значительно снижает тяжесть заболевания.
Не используйте, если у вас аллергия на какие-либо ингредиенты. В сухом, защищенном от света месте при температуре от +2°С до +8°С в течение 24 месяцев. После вскрытия желательно хранить Фагодерм в холодильнике. Выбросьте любое неиспользованное количество геля через 60 дней после первого открытия.
Эти заявления не были оценены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов. Этот продукт не предназначен для диагностики, лечения, лечения или предотвращения каких-либо заболеваний. Фактическая упаковка продукта и материалы могут содержать больше и другую информацию, чем та, что показана на нашем веб-сайте. Мы рекомендуем проконсультироваться с врачом, прежде чем использовать эту или любую другую добавку.
- Бактериофаги (от др.-греч. «поедатели бактерий») – вирусы, убивающие бактерии избирательно: каждый вид бактериофагов активен только в отношении определенных видов бактерий и нейтрален в отношении нормальной микробной флоры человека и не взаимодействует с его органами и системы.
- Гель Phagoderm представляет собой комплекс из 47 полезных живых бактериофагов. Применяется для нормализации местной и общей микрофлоры кожи и надежной защиты ее от бактериального заражения.
- Фаги можно назначать всем категориям как эффективное и безопасное антибактериальное средство для лечения и профилактики, в том числе в сочетании с антибиотиками.
- Комбинированное и защитное действие бактериофагов помогает организму бороться с инфекцией и ее последствиями.
- Профилактическое применение бактериофагов предотвращает новые случаи инфекционного воспаления или значительно снижает тяжесть заболевания.
Показания:
Прекратить использование Показания: Являясь природным антибиотиком, гель Phagoderm абсолютно безвреден для вашего организма, однако высокоэффективен против патогенных бактерий.
