Детский мононуклеоз: Мононуклеоз у детей – причины, симптомы, методы диагностики и лечения в СПб
ИНФЕКЦИОННЫЙ МОНОНУКЛЕОЗ У ДЕТЕЙ: клиника, диагностика, лечение
Кудин А.П.
УЗ «Городская детская инфекционная больница» г. Минска.
Инфекционный мононуклеоз является полиэтиологичным заболеванием и может вызываться различными лимфотропными инфекциями. В соответствии с МКБ 10 выделяют ИМ, вызванный гамма-герпесвирусом (вирусом Эпштейна-Барр (ВЭБ) или герпесвирусом 4-го типа), цитомегаловирусный ИМ, ИМ другой этиологии (на фоне аденовирусной инфекции, токсоплазмоза; инфекции, вызванной герпесвирусом 6-го или 7-го типа; в острую стадию ВИЧ-инфекции и т.д.) и ИМ неуточненной этиологии (в тех случаях, когда у пациентов с клиническими признаками ИМ не удается обнаружить ни один из известных возбудителей данного заболевания). Однако, как правило, если отдельно вопрос этиологии ИМ не оговаривается, это заболевание связывают с ВЭБ-инфекцией (ВЭБИ). Считается, что более 80-95% всех случаев типичного ИМ ассоциировано с ВЭБИ.
ВЭБ обладает тропизмом к различным клеткам, но основной мишенью для него являются В-лимфоциты и дендритные клетки, несущие на себе рецептор CD21 (или CR2 – рецептор для C3d компонента системы комплемента). Кроме В-лимфоцитов, поражается эпителий слизистой носоглотки и протоков слюнных желез. В определенных ситуациях могут инфицироваться Т-лимфоциты и NK-клетки, моноциты/макрофаги, нейтрофилы, миоэпителиальные и гладкомышечные клетки. Как и при других инфекционных заболеваниях, вызывающихся лимфотропными вирусами, исходы острой ВЭБ-инфекции (ВЭБИ) могут быть разными и являются интегративным показателем взаимодействия вируса и иммунной системы человека.
В организме человека ВЭБ может находиться в двух состояниях: в фазе активной инфекции и в латентном состоянии. Активная фаза ВЭБИ характеризуется значительным накоплением вирусных частиц, гибелью пораженных клеток, выходом вируса во внеклеточное пространство и инфицированием доступных для ВЭБ чувствительных клеток. Такой вариант развития вируса касается, в первую очередь, эпителиальных клеток ротоглотки и в значительно меньшей степени – В-лимфоцитов.
Латентная фаза ВЭБИ означает, что вирус находится в ядре инфицированной клетки (в первую очередь, это В-лимфоциты памяти]) в виде эписомы. При этом вирус продуцирует минимальное количество веществ, закодированных в его ДНК (латентные мембранные протеиды, ядерные белки, мелкие РНК), которые необходимы для репликации вируса вместе с клеткой-хозяином, но без образования дополнительных вирусных частиц и без гибели инфицированной клетки. Более того, вирус «заинтересован» в том, чтобы клетка-хозяин жила как можно дольше и чтобы вирус воспроизводился вместе с ней. Оказалось, что некоторые вирусные белки способны подавлять программу апоптоза ВЭБ(+) В-лимфоцитов, индуцируя феномен «клеточного бессмертия».
При отсутствии адекватного контроля со стороны основных факторов противовирусного иммунитета (цитотоксические лимфоциты, NK-клетки, Th2-зависимые механизмы иммунного ответа) возможна неконтролируемая пролиферация ВЭБ(+) В-лимфоцитов (т.е. клеток, несущих чужеродную генетическую информацию). Потенциально это может привести к развитию В-клеточной лимфопролиферативной болезни (нередко проявляющейся малигнизацией, особенно у людей с исходным иммунодефицитом). ВЭБ-ассоциированными более чем в половине случаев являются лимфома Беркитта (в странах Африки), назофарингеальная карцинома, смешанно-клеточная лимфома Ходжкина, ряд опухолей у больных со СПИД-ом (лимфомы головного мозга, гладко-мышечная опухоль, плазмобластная лимфома, ходжкинская лимфома им др.), внеузловая NK/T-лимфома, NK-лейкемия и др.
Кроме того, ВЭБ способен вызывать поликлональную стимуляцию В-лимфоцитов, что в ряде случаев может привести к развитию аутоиммунных заболеваний (иммунные цитопении, рассеянный склероз и некоторые другие).
В тех случаях, когда происходит значительное (по экспансии и уровню вирусной нагрузки) инфицирование клеток, участвующих в защите от вируса, развиваются тяжелые, угрожающие жизни человека варианты течения ВЭБИ. Преимущественное инфицирование CD8+ лимфоцитов приводит к развитию гемофагоцитарного синдрома. В основе формирования двух вариантов хронической активной ВЭБИ лежит поражение соответственно CD4+ лимфоцитов или NK- клеток. Значительно более редкими формами хронической ВЭБИ (ХВЭБИ) являются интерстициальная пневмония, поражения ЦНС, аневризмы коронарных артерий (как при болезни Кавасаки). Одним из необычных проявлений хронической ВЭБИ является гиперчувствительность к укусам комаров.
Хорошо известно, что у детей раннего возраста острая ВЭБИ в большинстве случаев протекает субклинически или в стертой форме, без развития клиники ИМ. По некоторым данным, наиболее распространенной формой первичной ВЭБИ у детей является ОРИ, на долю которой приходится более 40 % всех случаев. Однако этот вариант течения острой ВЭБИ не имеет каких-либо специфических проявлений и обычно не верифицируется. Наиболее известным вариантом острой ВЭБИ и вторым по частоте (около 18 % всех случаев инфекции) является ИМ, имеющий очень специфические клинические проявления. Эта форма острой ВЭБИ считается характерной, в первую очередь, для подростков и молодых людей.
Таким образом, главное, что следует помнить про патогенез ИМ – в основе развития заболевания лежит индуцированное вирусом иммунное воспаление (иммуно-патологический процесс), протекающее с поражением ВЭБ-инфицированных клеток, в первую очередь В-лимфоцитов и эпителиоцитов слизистой небных миндалин. В период разгара ИМ около 10-20 % всех циркулирующих в периферической крови В-лимфоцитов. С учетом того, что в периферической крови в каждый момент времени находится всего 0,2-2% всех лимфоцитов организма человека, основным местом поражающего действия вируса являются лимфоидные органы, а в них — В-зоны (где находятся В-лимфоциты) и дендритные клетки.
По мере выздоровления количество ВЭБ(+) В-лимфоцитов уменьшается до определенного стабильного минимального уровня и в последующем сохраняется пожизненно. В крови здоровых людей содержится от 1 до 50 инфицированных ВЭБ-ом клеток на один миллион В-лимфоцитов. При этом у здоровых носителей около 5% периферических мононуклеарных клеток (в первую очередь, Т-лимфоцитов) направлены против ВЭБ, что говорит о значимости для организма человека постоянного контроля над этой инфекцией.
При благоприятном течении острой ВЭБИ по мере снижения вирусной и антигенной нагрузки параллельно с этим основная часть активированных Т-лимфоцитов, выполнивших свою функцию, погибает по механизму апоптоза, а остальные превращаются в клетки памяти.
Клинические проявления ИМ складываются из признаков синдрома системного воспалительного ответа (ССВО), поражений лимфоидных органов и ангины. Манифестация происходит, как правило, бурно с резкого повышения температуры, появления признаков интоксикации (чаще умеренно выраженных), болей в горле, заложенности носа без насморка (вследствие аденоидита) и храпа во сне. Увеличиваются шейные (прежде всего, заднешейные) и подчелюстные лимфоузлы, и нередко может отмечаться генерализованная лимфоаденопатия. Иногда лимфоаденопатия предшествует появлению развернутой клиники ИМ, опережая ее на 5-7 дней. Часто, но не всегда, образуются налеты на миндалинах, которые могут плохо сниматься шпателем (т.к. представляют собой не только компоненты воспалительного экссудата, но и погибший эпителий слизистой). Более чем у половины больных определяется увеличение печени и/или селезенки. Важным в дифференциальной диагностике между банальной стрептококковой ангиной (требующей антибактериальной терапии) и экссудативным тонзиллитом при ИМ является отсутствие или незначительная боль в горле. Т.е. когда налетына миндалинах – большие, а горло не болит, это должно заставить задуматься врача о ИМ!!!
Развитие всех клинических проявлений ИМ происходит в течение нескольких суток. В эти сроки симптоматика может нарастать и дополняться. Важно помнить, что развернутая клиника ИМ, все перечисленные симптомы у одного больного встречают редко. Обычно один или несколько симптомом отсутствуют. И в этом случае следует подтверждать диагноз лабораторно.
В эти сроки симптоматика может нарастать и дополняться. Важно помнить, что развернутая клиника ИМ, все перечисленные симптомы у одного больного встречают редко. Обычно один или несколько симптомом отсутствуют. И в этом случае следует подтверждать диагноз лабораторно.
Как правило, большинство врачей ориентируется на наличие в общем анализе крови (ОАК) атипичных мононуклеаров (АМ) в количестве >10%. Это действительно позволяет констатировать ИМ. Однако, следует помнить, что АМ появляются в крови не сразу, часто с 4-5-го дня болезни, а иногда только на второй неделе заболевания. Кроме того, примерно у 5% пациентов они могут вовсе отсутствовать. В этом случае следует ориентироваться на клинические проявления и наличие в ОАК преобладания лимфоцитов и моноцитов: наличие у ребенка ангины, которая сопровождается лимфоцитозом должно навести врача на мысль о том, что ангина какая-то специфическая.
Банальные стрептококковые тонзиллиты обычно вызывают выраженные воспалительные изменения в ОАК (лейкоцитоз, нейтрофилез, выраженный сдвиг лейкоцитограммы влево, когда молодые формы нейтрофилов составляют 15-20% и более). При ИМ небольшой сдвиг формулы крови влево тоже часто имеет место (обычно в пределах 6-12%, как одно из проявлений ССВО), однако при этом отмечается лимфомоноцитоз. Кроме того, некоторые инфекции, способные протекать с мононуклеозоподобным синдромом (аденовирусная, например), не сопровождаются лимфоцитозом в лейкоцитограмме, а протекают с нейтрофилезом или нормоцитозом [Melon2005].
Косвенным признаком ИМ можно считать повышение в крови содержания трансаминаз (АсАТ обычно больше, чем АлАТ). Эта, так называемая адаптивная ферментемия, связана с перестройкой метаболизма вследствие выраженного ССВО на фоне ИМ. Поэтому у пациентов с «подозрительной» ангиной имеет смысл проведение биохимического анализа крови.
Следует помнить, что тяжелое поражение печени с развитием желтушной формы гепатита (и иногда даже фульминантного гепатита) связано не с вирусным цитолизом гепатоцитов (ВЭБ не имеет тропизма к этим клеткам), а с инфицированием в печени местных Т- и T/NK-лимфоцитов, которые и вызывают поражение гепатоцитов (клеточно-опосредованный цитолиз).
В качестве дополнительных лабораторных тестов для доказательства ВЭБИ могут быть использованы:
- методы определения титра гетерофильных антител (у нас – это реакция Пауль-Буннеля, за рубежом – monospot test). Диагностическая значимость его невелика, но в определенных ситуациях это исследование помогает в диагностике. Основным его достоинством является то, что гетерофильные антитела обнаруживаются при первичном ВЭБ-ассоциированном ИМ и не определяются при ИМ другой этиологии. Недостатком метода является его частый ложноотрицательный ответ у дошкольников и младших школьников,
- серологические методы: обнаружение IgM к капсидному антигену (viral capsid antigen) и IgG к раннему антигену ВЭБ (Epstein-Barr early antigen), соответственно анти-VCA IgM и анти EB EA IgG,
- определение ДНК ВЭБ методом ПЦР в крови (плазме или сыворотке), что всегда свидетельствует об активной репликации вируса (в отличие от ее обнаружения в мононуклеарах – в основном, в В-лимфоцитах – периферической крови).
Из всех клинических проявлений ИМ, пожалуй, только изменения миндалин могут быть связаны с прямым цитопатогенным действием вируса на эпителий слизистой оболочки этих структур. Но и здесь свой вклад в местные изменения вносит иммунное воспаление. Это означает, что тонзиллит (включая варианты с образованием налетов на миндалинах) по сути является асептическим воспалением, часто протекающим без присоединения вторичной бактериальной инфекции (как бы «страшно» не выглядела ротоглотка при осмотре). Поэтому без наличия косвенных признаков бактериальной суперинфекции нет необходимости в назначении антибактериальной терапии (АБТ). Такими признаками можно считать (с некоторыми оговорками) выраженные воспалительные изменения в ОАК (о чем говорилось ранее). Из острофазовых показателей, по-видимому, следует иметь в виду повышение уровня СРБ более 70-100 мг/л. Что же касается повышения СОЭ, то ее уровень при ИМ часто превышает 30 мм/ч, очевидно, вследствие увеличения в крови глобулиновой фракции белков, отражающей поликлональную стимуляцию В-лимфоцитов.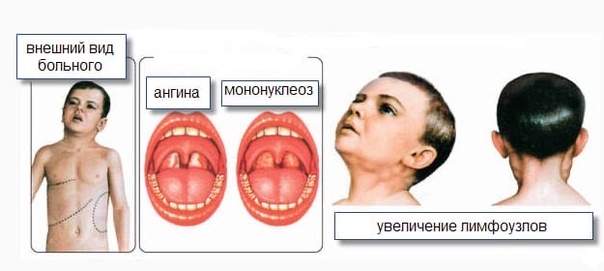 При отсутствии признаков бактериальной суперинфекции назначение АБТ неоправданно. Есть данные о том, что АБТ увеличивает продолжительность сохранения ангины.
При отсутствии признаков бактериальной суперинфекции назначение АБТ неоправданно. Есть данные о том, что АБТ увеличивает продолжительность сохранения ангины.
При наличии показаний к АБТ следует применять цефалоспорины 1-2 поколения, макролиды или линкосамиды и помнить, что при ИМ НЕЛЬЗЯ применять аминопенициллины из-за высокого риска развития «ампициллиновой сыпи» – как правило, обильной мелко- и крупно-пятнистопапулезной сыпи, нередко с геморрагическим компонентом, внешне сходную с полиморфной экссудативной эритемой. В основе ее генеза лежит реакция гиперчувствительности замедленного типа. Поэтому в тяжелых случаях эта экзантема способна прогрессировать с развитием синдрома Стивенса-Джонсона или даже токсического эпидермального некролиза.
Здесь будет уместно обратить внимание на то, что Н1-блокаторы не имеет смысла назначать не только при обычном течении ИМ, но и при появлении «ампициллиновой сыпи» (как бы кому-то этого не хотелось). Ни в том, ни в другом случае IgE-зависимые реакции не развиваются, «работают» Т-клеточные реакции, поэтому гистамин является одним из многих медиаторов такого воспаления и при этом типе реакций не играет существенной роли. Естественно, в случае развития крапивницы на какой-либо из применяемых препаратов, назначение Н1-блокаторов будет обосновано. Но только в этом случае.
Показанием к назначению АБТ могут быть и некоторые осложнения ИМ. Так вследствие аденоидита повышается вероятность развития отитов и синуситов. Поэтому наряду с применением средств улучшающих носовое дыхание (об этом речь пойдет ниже) в комплексную терапию следует включать и АБ, эффективны в отношении наиболее вероятных этиологических факторов этих осложнений (пневмококк, гемофильная палочка): цефалоспорины 2-3-го поколения, при их непереносимости – азитромицин.
В ситуации, когда налеты на миндалинах есть, а воспалительные изменения в общем анализе крови отсутствуют (лимфомоноцитоз с нейтропенией и отсутствием или незначительным – до 10-12% молодых форм нейтрофилов – сдвигом лейкоцитограммы влево) и уровень СРБ невысокий (до 50-70 мг/л), боль в горле незначительная или отсутствует высока вероятность участия в воспалении нормальной анаэробной флоры , активировавшейся на фоне заболевания. В этом случае можно попытаться включить в схему терапии метронидазол 7,5-10 мг/кг 3 раза в день на 7-10 дней (с оценкой эффекта через 3-4 дня: если налеты не уменьшились или уменьшились незначительно, препарат стоит отменить).
В этом случае можно попытаться включить в схему терапии метронидазол 7,5-10 мг/кг 3 раза в день на 7-10 дней (с оценкой эффекта через 3-4 дня: если налеты не уменьшились или уменьшились незначительно, препарат стоит отменить).
Отношение к назначению противовирусных препаратов в настоящее время уже достаточно однозначное: они не нужны во время острой ВЭБИ. Как уже говорилось, клинические проявления ИМ связаны, прежде всего, с иммуноопосредованным воспалением, а не с цитолитическим действием самого вируса. Фактически, чем сильнее иммунный ответ на ВЭБ, тем тяжелее клинические проявления ИМ (иногда даже возникает необходимость в подавлении очень выраженного, «избыточного» иммунного воспаления). Поэтому практические попытки применения противовирусных препаратов (ацикловира) не оказали влияния на тяжесть и продолжительность ИМ, хотя при этом и снижали уровень вирусной нагрузки в слюне и в лимфоидных образованиях ротоглотки, не влияя на этот показатель в В-лимфоцитах (там, в основном, вирус находится в фазе латентного цикла). После прекращения применения этих препаратов репликация вируса возобновляется до момента формирования надежного противовирусного иммунитета.
Однако при хронических ВЭБ-ассоциированных заболеваниях, при которых вирус находится в литическом цикле развития, противовирусные препараты могут иметь эффект (волосатая лейкоплакия языка, хроническая активная ВЭБИ).
Кроме того, включение противовирусных препаратов, возможно, будет полезным при тяжелых атипичных формах острой ВЭБИ, протекающих с поражением внутренних органов (фульминантный гепатит, кардит, пульмонит) и ЦНС (энцефалит, менингоэнцефалит). По-видимому, это связано с тем, что развитие этих вариантов острой ВЭБИ обусловлено поражением вирусом нетипичных для этой инфекции клеток (CD8+ цитотоксических лимфоцитов, CD4+ клеток, NK-клеток, моноцитов/макрофагов).
Больше всего вопросов в лечении ИМ возникает в отношении применения глюкокортикостероидов (ГКС). В 50-60-х годах прошлого века эти препараты применялись широко и, как считалось, с хорошим эффектом. Затем в связи с потенциально онкогенными свойствами ВЭБ, иммуносупрессивным действием ГКС и неясными последствиями действия двух этих факторов на организм каждого конкретного больного, от применения ГКС при неосложненном течении ИМ отказались. Однако и в наше время проводятся исследования по оценке влияния ГКС на пациентов с ИМ. Существуют работы, в которых показывается как эффективность этих препаратов (по крайней мере, кратковременная и в отношении некоторых симптомов), так и отсутствие влияния ГКС на степень выраженности и продолжительность сохранения симптоматики ИМ.
Затем в связи с потенциально онкогенными свойствами ВЭБ, иммуносупрессивным действием ГКС и неясными последствиями действия двух этих факторов на организм каждого конкретного больного, от применения ГКС при неосложненном течении ИМ отказались. Однако и в наше время проводятся исследования по оценке влияния ГКС на пациентов с ИМ. Существуют работы, в которых показывается как эффективность этих препаратов (по крайней мере, кратковременная и в отношении некоторых симптомов), так и отсутствие влияния ГКС на степень выраженности и продолжительность сохранения симптоматики ИМ.
Мнение автора этой статьи совпадает с мнением первой группы ученых, т.к. я неоднократно видел клинический эффект от применения ГКС у детей с ИМ. Исходя из патогенеза заболевания, такого эффекта ГКС следует ожидать. Другое дело, надо ли всем детям с ИМ назначать ГКС? Однозначно – нет! ИМ – это самолимитирующееся заболевание, которое в подавляющем большинстве случаев заканчивается выздоровлением в течение 7-14 дней (здесь речь идет об острых проявлениях инфекции, т.к. остаточные явления в виде полиаденопатии, гепатолиенального синдрома, гипертрофии миндалин могут сохраняться от нескольких недель до нескольких месяцев). Показаниями к назначению ГКС должны быть только тяжелые формы ИМ, сопровождающиеся тяжелой обструкцией верхних дыхательных путей (обычно, верхних в виде тяжелого аденоидита), различными цитопениями, поражениями нервной системы. Причем, если ГКС назначаются, это не должно быть одно-двукратное введение. Обычно рекомендуется 7-14-дневный курс терапии: в течение половины этого срока назначают ГКС из расчета 1 мг/кг/сут по преднизолону (максимум – 60 мг/сут), внутрь, а затем в течение оставшегося срока дозу постепенно снижают вплоть до отмены. В некоторых случаях при неэффективности обычных доз ГКС прибегают к пульс-терапии метилпреднизолоном (15-30 мг/кг, в/вено, в течение часа, 1 раз в день, 3 дня подряд) с последующей постепенной отменой (ежедневно доза снижается на 50% вплоть до отмены).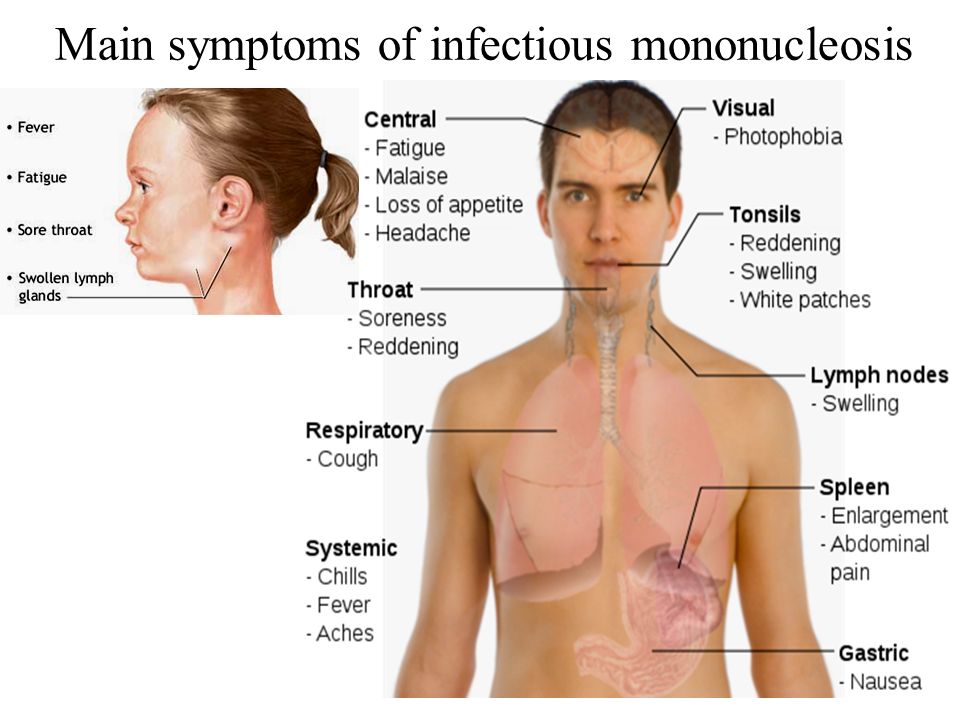
В русскоязычной литературе последние годы широко обсуждался вопрос о применении. Если исходить из представленных выше данных о патогенезе ИМ, становится понятным, что в острый период заболевания нет необходимости в дополнительной иммуностимуляции уже развившегося иммуноопосредованого воспаления. Такая необходимость может возникнуть в периоде поздней реконвалесценции (с 3-й недели до 3-х месяцев), т.к. в это время у людей, перенесших ИМ, развивается вторичный иммунодефицит, выраженный в разной степени. Резюмируя ту информацию, которая есть в литературе по применению иммуностимуляторов, следует сказать, что при наличии клинических признаков вторичного иммунодефицита (ребенок стал чаще и дольше болеть разными инфекционными заболеваниями после перенесенного ИМ) может возникнуть необходимость в иммунокоррекции. Но в настоящее время нет надежных и доступных методов оценки эффективности разных иммуностимуляторов у конкретного ребенка. Поэтому с учетом различной чувствительности иммунной системы ребенка к разным иммуномодуляторам, подбирать такую терапию придется эмпирически и без гарантии успеха. Успокаивает только то, что у большинства детей в течение 1,5-4 месяцев изменения в работе иммунной системы нивелируются. Хотя с учетом возможности формирования активной хронической ВЭБИ вопрос о необходимости и тактике применения иммуномодуляторов остается открытым.
Еще один момент в клинике ИМ нередко тревожит врачей и заставляет предпринимать «героические» усилия по спасению больного. Это – поражение печени, точнее – повышение уровня трансаминаз. На самом деле, как уже говорилось, далеко не всегда повышение уровня АлАТ и АсАТ связано с развитием гепатита (тем более что нередко содержание АсАТ выше, чем АлАТ, что, вроде бы, не характерно для поражений печени). Но даже в тех случаях, когда имеет место преимущественное повышение концентрации АлАТ и можно думать о легкой безжелтушной форме гепатита, он проходит самостоятельно в течение 7-10 дней без всякого лечения. Поэтому использование желчегонных препаратов, гепатопротекторов, препаратов урсодезоксихолиевой кислоты является лишним и необоснованным. Не исключено, что при тяжелом желтушном варианте ИМ может быть поднят вопрос об использовании двух последних групп препаратов, но этот вопрос должен решаться в каждом случае индивидуально. К тому же, если помнить о механизмах развития поражений печени, то применение ГКС здесь будет более оправданным, особенно в случае развития фульминантного гепатита.
Поэтому использование желчегонных препаратов, гепатопротекторов, препаратов урсодезоксихолиевой кислоты является лишним и необоснованным. Не исключено, что при тяжелом желтушном варианте ИМ может быть поднят вопрос об использовании двух последних групп препаратов, но этот вопрос должен решаться в каждом случае индивидуально. К тому же, если помнить о механизмах развития поражений печени, то применение ГКС здесь будет более оправданным, особенно в случае развития фульминантного гепатита.
Говоря о поражении печени при ИМ, нельзя обойти стороной и вопрос о правильном питании таких пациентов. Нередко в нашей литературе указывают на необходимость назначения молочно-растительной диеты. Серьезных исследований по этому вопросу не поводилось. На самом деле для этого нет никаких оснований и ориентироваться нужно только на потребности ребенка, его пищевые пристрастия, аппетит и переносимость пищи. Естественно, какие-то разумные ограничения должны быть (не запрещение, а ограничение жирных и жареных продуктов, острых блюд и т.д.), однако такой образ питания полезен не только больному, но и здоровому человеку. Таким образом, пациент с ИМ должен просто правильно питаться без больших ограничений. Только больные с тяжелыми желтушными формами ИМ будут нуждаться в более строгой диете, как и больные с аналогичными формами вирусных гепатитов.
Основное же место в лечении больных с ИМ занимает симптоматическая терапия. При высокой лихорадке назначают жаропонижающие препараты (у детей это обычно парацетамол 10-15 мг/кг до 4 раз в сутки и ли ибупрофен 5-10 мг/кг до 3 раз в сутки), лучше чередуя для сохранения эффекта. При выраженных болях в горле применяют ибупрофен в той же дозе 3 раза в день, не зависимо от температуры. Полоскать рот достаточно просто водой после каждого приема пищи (применение местных антисептиков не влияет на скорость выздоровления и выраженность клинической симптоматики). Тем пациентам, которым субъективно становится легче после соляно-содовых полосканий, не стоит запрещать это делать.
Одним из характерных признаков ВЭБ-ассоциированного ИМ является заложенность носа и храп во сне. В первую очередь это связано с асептическим (иммунным) воспалением глоточной миндалины. Небольшой вклад в нарушение носового дыхания может вносить и отечность слизистой носа, но без образования экссудата. Поэтому у таких детей обычно нет отделяемого из носа, и поэтому сосудосуживающие капли, как правило, неэффективны. Исходя из собственного опыта, можно предложить в тех случаях, когда носовое дыхание сильно затруднено, но других показаний для системного назначения ГКС нет, применять местно действующие ГКС (напр., «назонекс»). Курс его применения обычно составляет 5-14 дней.
Таким образом, в основе клинической манифестации ИМ лежит иммунопатологическое воспаление, индуцированное ВЭБ-ом и опосредованное, прежде всего, факторами клеточного иммунитета. Заболевание в большинстве случаев протекает благоприятно и самостоятельно заканчивается выздоровлением. Основную роль в лечении больных с ИМ играет симптоматическая терапия, направленная на облегчение симптомов болезни. Применение антибиотиков должно быть хорошо обоснованным. Наличие налетов на миндалинах не является достаточным основанием для АБТ. В тяжелых и осложненных случаях терапия дополняется назначением короткого курса ГКС. Они показаны пациентам с обструкцией дыхательных путей, с различными цитопениями, с поражением нервной системы. Назначение Н1-блокаторов, витаминов, гепатопротекторов, местных антисептиков и т.д. в подавляющем большинстве случаев не требуется. Никакая специальная диета детям с ИМ, как правило, не нужна.
КУДИН Александр Петрович, к.м.н., доцент, зав.отделением № 5 УЗ ГДИКБ.
Инфекционный мононуклеоз – симптомы, осложнения, лечение, профилактика
directions
Мононуклеоз – острое инфекционное заболевание, поражающее лимфоидную ткань. Вирус инфекционного мононуклеоза имеет широкое распространение, однако его течение в основном происходит в лёгких формах. Наиболее часто мононуклеоз встречается у детей старше 3-х лет и у взрослых до 40. Источником заражения является заболевший человек. Передача инфекции может произойти при поцелуях, через игрушки, либо воздушно-капельным путём, во время родов и при переливании крови. Даже спустя долгое время инфицированный человек может заразить своих близких. Для того, чтобы это не произошло, лучше всего сдать специальный анализ, способный подтвердить наличие заболевания и способствовать его диагностике.
Наиболее часто мононуклеоз встречается у детей старше 3-х лет и у взрослых до 40. Источником заражения является заболевший человек. Передача инфекции может произойти при поцелуях, через игрушки, либо воздушно-капельным путём, во время родов и при переливании крови. Даже спустя долгое время инфицированный человек может заразить своих близких. Для того, чтобы это не произошло, лучше всего сдать специальный анализ, способный подтвердить наличие заболевания и способствовать его диагностике.
Врачи-специалисты
Старшая медицинская сестра
Медицинская сестра
Медицинская сестра эндоскопического кабинета
Врач-терапевт
Медицинская сестра процедурной
Анализ на коронавирус методом ПЦР. Результат в течение 3-х дней
Результат в течение 3-х дней
Наши клиники в Санкт-Петербурге
Медицентр Юго-ЗападПр.Маршала Жукова 28к2
Кировский район
- Автово
- Проспект Ветеранов
- Ленинский проспект
Получить подробную информацию и записаться на прием Вы можете по телефону +7 (812) 640-55-25
Длительность инкубационного периода напрямую определяется состоянием иммунитета. В среднем он может составлять от 5 дней и до 2-х месяцев.
Симптомы и течение заболевания
Первые симптомы заболевания похожи на обычное простудное заболевание:
- воспаление миндалин;
- дыхание через рот;
- храп;
- повышение температуры;
- отсутствие аппетита;
- боль при глотании;
- вялость;
- ломота в теле;
- увеличение всех лимфатических узлов;
В период, когда болезнь входит в активную стадию, отмечается увеличение селезёнки и печени, развивается желтушный синдром, иногда может появляться экзантема. Разгар болезни имеет продолжительность около 2-3х недель, после чего самочувствие больного начинает постепенно улучшаться. При хроническом течении заболевания периоды обострений и ремиссий могут сменяться, и болезнь может продолжаться на протяжении 1,5 лет.
Разгар болезни имеет продолжительность около 2-3х недель, после чего самочувствие больного начинает постепенно улучшаться. При хроническом течении заболевания периоды обострений и ремиссий могут сменяться, и болезнь может продолжаться на протяжении 1,5 лет.
Осложнения:
- изменения со стороны крови;
- разрыв селезёнки;
- аритмия, блокада, перикардит;
- менингит;
- острая печёночная и почечная недостаточность;
- воспаление лёгких;
- асфиксия;
- ангина;
- отит.
Поражение лимфоидной системы, а как следствие и иммунитета, может сделать человека уязвимым к другим инфекциям. Поэтому у больных мононуклеозом очень легко развивается и любое другое заболевание. При этом лечение осложнений может вызывать появление сыпи на кожных покровах. Вирус обладает онкогенной активностью, поэтому следует очень внимательно следить за состоянием здоровья перенёсшего заболевание.
Лечение
Точно установить диагноз поможет клинический анализ крови. Инфекционный мононуклеоз поражает клетки крови, создавая в её плазме атипичные мононуклеары. Больным необходимо проходить обследование во время всего течения болезни, а также сдавать анализ на ВИЧ, так как при его возникновении может развиваться мононуклеозоподобный синдром. После болезни детям на протяжении 6-12 месяцев прекращают прививки. Больных мононуклеозом в лёгкой форме можно лечить на дому. Лечение проводится симптоматическими и общеукрепляющими препаратами, при осложнениях прописывают антибиотики.
Заболевшим людям противопоказано долго быть на солнце, необходимо соблюдать диету и абсолютный покой, обильно пить и принимать витамины. Повторные заболевания мононуклеозом встречаются редко, так как считается, что у человека перенёсшего мононуклеоз устанавливается стойкий иммунитет.
При неправильном лечении инфекция может перейти в хроническую форму, что увеличивает вероятность заражения гепатитом, ВИЧ, поражается нервная система, печень и сердце.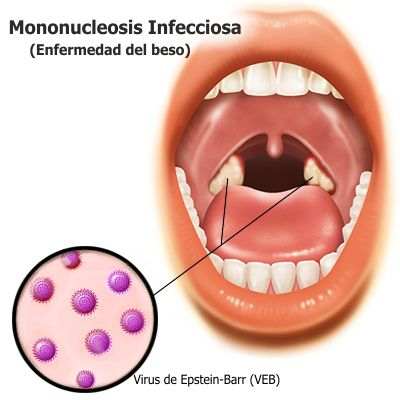
Инфекционный мононуклеоз у беременных
При планировании беременности нужно учитывать все обстоятельства, в том числе и прошлые заболевания. После мононуклеоза организму нужно очень долгое время, чтобы полностью восстановиться. Наступление беременности крайне нежелательно, пока в крови проявляются остаточные явления заболевания. Этот период в среднем может длиться от 6 до 12 месяцев. Болезнь может повлиять как на здоровье матери, так и ребёнка, и привести к невынашиванию плода. В утробе матери у него могут появиться какие-либо уродства, нарушения в развитии.
У беременных инфекционный мононуклеоз проявляется в виде недомогания, ангины, увеличения лимфоузлов, лихорадки, в большинстве случаев наблюдается спленомегалия (увеличение селезёнки).
Профилактика
Особых мер профилактики специалистами не было разработано. Есть только неспецифический способ, заключающийся в поддержании иммунологической резистентности организма.
845,837,814,860,1274,1285
Кириличев Кирилл Александрович 03.12.2020 10:44medi-center.ru
Хочу поблагодарить терапевта Дерешовского Александра Сергеевича, за профессионализм и внимательность к пациенту. Именно этими качествами должен обладать настоящий Врач. Доктор всегда был на связи, проявлял интерес к самочувствию и готов был ответить на любой поставленный мной вопрос. Побольше бы таких специалистов в такое непростое для всех время.
Жданова Анна Михайловна 25.11.2020 14:32medi-center.ru
Хочу выразить огромную благодарность врачу терапевту Дерешовскому Александру Сергеевичу.
На 28 неделе беременности не обошла стороной и нас эта зараза под названием COVID-19. В день вызова врача пришёл Александр Сергеевич, посмотрел, послушал, взял мазки на ковид, назначил грамотное лечение. И самое главное всегда со мной был на связи, и утром , и днём, и вечером.
Зараза отступила.
Спасибо Вам, Александр Сергеевич, за Ваш труд в столь не простое для всех время.
Здоровья Вам и Вашим близким!????
Была 21.06.20 у Гареевой Регины Гумеровны.Хочу поблагодарить ее за проффесионализм,хорошее отношение к пациентам и за здравое рассуждение!Она все подробно объяснила,не пугала и не делала поспешных выводов,как некоторые,а ,наоборот,подбадривала.На вид добрая и спокойная.Всем советую????????
добрый день! хочу сердечно поблагодарить гастроэнтеролога Банникову Татьяну Петровну за профессиональный прием. Я обратилась с болью, думая, что у меня проблемы с желчным пузырем, даже принимала соотвествующие лекарства, но после опроса симптоматики и осмотра мне был поставлен другой диагноз и назначено соотвествующее лечение. Очень чуткий и внимательный доктор! Спасибо! Ваше имя: Валентина. Дата события: 25 апреля Специализация врача: Гастроэнтеролог Банникова Т.П. Обследование: первичный прием с жалобами на боль в боку.
Здравствуйте! Хотим оставить хороший отзыв о работе медцентра. 11 марта 2020 года у дочери (3,5 года) случился вывих локтевого сустава. Сразу же обратились в травматологический пункт на Аллее Поликарпова, д.6, корп.2, лит.А. Приехали около 23:00. Нас сразу же на входе встретил врач Джораев А.О. Мгновенно нашел подход к плачущему ребенку. Проблема такая у маленьких детей часто встречается, поэтому врач сразу же понял, что произошло и что делать. Выполнил несколько манипуляций, сделал рентген, чтобы убедиться, что нет серьезной травмы, далее еще несколько манипуляций и ручка заработала. Врач и администратор медцентра терпимо и с пониманием отнеслись к плачущему ребенку и все сделали, как надо. Выражаем благодарность коллективу медцентра и лично врачу Джораеву А.О. за быструю и профессиональную работу!
Выражаем благодарность коллективу медцентра и лично врачу Джораеву А.О. за быструю и профессиональную работу!
Добрый день! Я хотела бы поблагодарить Клинику МедиЦентр (на алее Поликарпова) и ЛОР-врача Ершову Татьяну Викторовну за их работу. К Татьяне Викторовне на приём первый раз попала в 2016 году. С этого момента, при возникновении проблем с горлом или носом, обращаюсь только к Татьяне Викторовне. Всегда внимательное отношение к описанной симптоматике и тщательный осмотр, направления на уточняющие состояние анализы и, как результат, правильное лечение. Спасибо! С уважением, Мария
Мононуклеоз у детей: симптомы, лечение, профилактика
Многих мам пугает диагноз “инфекционный мононуклеоз”, хотя вирус Эпштейн-Барра — возбудитель болезни — один из самых распространенных в мире. Давайте разберемся, насколько опасен мононуклеоз для детей и как его лечить.
Мононуклеоз у детей: симптомы
Мононуклеоз классифицируется как вирус ВГЧ — то есть вирус герпеса человека, который присутствует у 95-98% населения. Многие люди, в крови которых обнаружен ВГЧ, удивляются, узнав, что болели мононуклеозом. А все потому, что одна из характеристик этого инфекционного заболевания — неясные симптомы. За мононуклеоз можно легко принять аденоидит, ангину или ОРВИ. Но так бывает не всегда — порой инфекция мононуклеоза дает неприятные осложнения и последствия, заставляя родителей понервничать.
Наиболее близка для среды мононуклеоза лимфатическая система: вирус “селится” на миндалинах, на печени и селезенке, вызывая их увеличение. У ребенка отекает носоглотка, появляется храп, сыпь, боль в горле и температура — главный признак. Главная ловушка мононуклеоза — это то, что его легко можно принять за ангину, начав лечить заболевание антибиотиками. Чтобы избежать этого, ребенку в качестве диагностики картины заболевания следует сделать клинический анализ крови, который сразу подскажет о наличии или отсутствии атипичных мононуклеаров и отобразит, в какой форме протекает болезнь: в вирусной, бактериальной или хронической./GettyImages-562434173-5990767aaf5d3a00112b1630.jpg)
Заражение мононуклеозом происходит через слюну — общую посуду, игрушки и т.д.
Лечение мононуклеоза:
- измерить температуру. Ребенку любого возраста можно легко измерить температуру при помощи термометров AGU, которым требуется всего 1-3 секунды для бесконтактного измерения;
- если температура более 38 °C, следует принять жаропонижающее средство, проконсультировавшись с врачом;
- полоскание горла;
- диетическое питание;
- постельный режим.
Профилактика мононуклеоза:
- отказ от массовых мероприятий;
- прием витаминов;
- закаливание;
- здоровое питание.
Мононуклеоз
О заболевании «детский мононуклеоз» многие родители никогда не слышали. И самое интересное, что большинство людей на планете когда-то уже перенесли этот недуг, но просто не заметили его. Чаще всего у взрослых заболевание протекает бессимптомно, в легкой форме. Ярко выраженные симптомы инфекционного мононуклеоза (увеличенные лимфоузлы, печень или селезенка) проявляются у детей со сниженным иммунитетом.
Причины
Инфекционный мононуклеоз путем при тесных контактах с больным человеком: при поцелуях, переливании крови, во время поездок в общественном транспорте и использовании средств личной гигиены. Дети же в основном заражаются, когда долгое время находятся в закрытых пространствах – в садиках и школах.
Инфекционный мононуклеоз у детей: понятие и признаки
Инфекционный мононуклеоз – это острое вирусное заболевание, которое также называется вирусом Эпштейна-Барр — по фамилиям ученых, открывших его. В основном оно поражает детей до 10 лет, притом в два раза чаще – мальчиков.
Чаще всего в начале развития заболевание протекает спокойно. Родители могут заметить у ребенка хроническую усталость, недомогание, першение в горле и заложенность носа.
Кульминацией являются следующие симптомы:
- ангина (зернистость задней стенки слизистой глотки)
- увеличенные печень и селезенка. Иногда селезенка увеличивается настолько, что это может закончится ее разрывом.
- увеличенные лимфоузлы (чаще всего воспаляются заднешейные лимфатические узлы. Это становится особенно заметно, когда ребенок поворачивает голову)
- высокая температура – сыпь на коже
Многие люди не испытывают симптомов заболевания, но при этом могут быть переносчиками вируса и легко заразить других. Поэтому если ребенок общался с больным инфекционным мононуклеозом, родителям необходимо внимательно следить за его здоровьем. Если в следующие 2-3 месяца заболевание не проявилось, значит ребенок не заразился, или его иммунитет справился с недугом.
Но если первые симптомы мононуклеоза у детей все же проявились, родители должны обратиться к врачу и ни в коем случае не пытаться вылечить заболевание самостоятельно. При неправильном лечении могут появиться осложнения.
Обращаем внимание, что в острой форме мононуклеоза ребенок должен быть обязательно госпитализирован в стационар.
Диагностика и лечение мононуклеоза у детей в Медицинском центре «АКАДЕМИК»
В медицинском центре «АКАДЕМИК» для диагностики мононуклеоза у ребенка врач назначит следующие исследования:
- Анализ крови на антитела к вирусу Эпштейна-Барр
- Общий биохимический анализ крови
- Мазок на флору из зева (горла) и носа
Если диагноз подтверждается, врачи составляют план лечения и назначают:
- Инфузионную терапию (внутривенные инъекции лекарственных препаратов)
- Противовирусные препараты
- Общеукрепляющую терапию (витамины группы B, C и Р)
- Гептопротекторы (предназначаются для лечения печени)
Осложнения инфекционного мононуклеоза у детей
При своевременной диагностике и лечении осложнения инфекционного мононуклеоза возникают не так часто. Тем не менее, самым распространенным среди них является воспаление печени, которое может вызвать желтуху у детей. В очень редких случаях случается разрыв селезенки – это самое опасное последствие мононуклеоза, которое иногда оборачивается летальным исходом.
Когда ребенок переболел мононуклеозом, его иммунитет остается ослабленным еще около года. Поэтому в этот период будет эффективным сделать плановые прививки после перенесенного заболевания и по возможности ограничить контакты ребенка с большим количеством людей, а также воздержаться от поездок в места с непривычным климатом.
Самая коварная особенность мононуклеоза – его вирус мононуклеоза является онкогенноактивным, т.е. он может оказать стимулирующее действие на развитие онкозаболеваний. Поэтому очень важно повторно сдать анализ крови после выздоровления, чтобы отследить, как идет восстановление состава крови. Чтобы предотвратить эти осложнения, при явных симптомах мононуклеоза у ребенка нужно обратиться к врачу, который в случае острой формы заболевания обеспечит госпитализацию в стационар. Наши врачи в короткие сроки проведут диагностику, назначат лечение и приложат все силы, чтобы ребенок скорее выздоровел.
Записаться на прием
Инфекционный мононуклеоз у детей. Симптомы и лечение
Инфекционный мононуклеоз у детей вызывается вирусом Эпштейн-Бара (ВЭБ). Это заболевание может протекать в различных формах. Заболевают дети в возрасте от 2 – 3 х лет и старше, как правило при контакте в организованных коллективах (детский сад, ясли, школа). Вирус от человека к человеку передается с инфицированной слюной от больного ребенка или носителя. Поэтому, иногда инфекционный мононуклеоз еще называют болезнью поцелуев.
Маленькие дети заражаются через игрушки в игровых комнатах. Чаще отмечается острое начало заболевания следующими симптомами:
- повышение температуры тела,
- головная боль,
- боли в мышцах и суставах,
- беспокоят боли в горле, значительно усиливающиеся при глотании,
- затрудненное носовое дыхание,
- увеличение лимфатических узлов шеи, реже в других локализациях (пах, подмышечные впадины).

Острота заболевания нарастает к 4–6-му дню, в ряде наиболее тяжелых случаев инфекционного мононуклеоза к 3–4-му дню отмечается увеличение живота у ребенка за счет увеличения размеров печени и селезенки (гепатоспленомегалия). В некоторых случаях возможно подострое начало болезни с невыраженными симптомами. Основными симптомами инфекционного мононуклеоза являются: лихорадка (повышение температуры тела до 39), тонзиллит, генерализованная лимфаденопатия (увеличение лимфоузлов всего тела), гепатоспленомегалия, кожная сыпь (у 30% больных — эритематозные, розеолезные, папулезные и др. высыпания).
Помимо клинических симптомов для постановки диагноза необходимо лабораторное исследование. С первых дней болезни в анализе крови лейкопения и нейтропения, лимфоцитоз, плазматические клетки. Характерные изменения в периферической крови появляются после 5-го дня болезни: развивается лейкоцитоз до 10–13 × 109/л (возможен гиперлейкоцитоз до 18–20 × 109/л), лимфомоноцитоз, возрастает количество плазматических клеток, появляются атипичные монолимфоциты (10–60% и выше).
Иммунологическое исследование крови показывает нарастание уровня антител к вирусу Эпштейн-Бара, так же этот вирус появляется в слюне ребенка при исследовании методом ПЦР диагностики. На УЗИ брюшной полости выявляются увеличенные печень и селезенка и мезентеральные лимфатические узлы. Диагноз инфекционного мононуклеоза выставляется врачом педиатром по совокупности клинических и лабораторно-инструментальных данных. При правильно назначенном лечении врачом педиатром выздоровление наступает через 2–4 недели, но могут сохраняться признаки лимфоаденопатии (увеличение аденоидов и небных миндалин, лимфоузлов), гепатоспленомегалия, атипичные мононуклеары в крови, что указывает на затяжное течение ВЭБ инфекции. При хроническом инфекционном мононуклеозе отмечаются персистирующая лимфоаденопатия, гепатит, спленомегалия, гипоплазия костного мозга, интерстициальная пневмония. Пациенты с такими формами заболевания должны лечиться при непосредственном участии врача иммунолога.
Инфекционный мононуклеоз | H-Clinic
19.08.2019
Инфекционный мононуклеоз – это заболевание, вызываемое герпес-вирусом 4 типа или, как его еще называют, вирусом Эпштейна-Барр (ВЭБ). Возникает оно чаще всего при первичном заражении подростков и взрослых. У детей эта инфекция при первом контакте может протекать как обычное ОРЗ, без специфических симптомов.
ВЭБ – один из наиболее часто встречающихся вирусов человека. В тот или иной период жизни большинство людей инфицируются вирусом Эпштейна-Барр. ВЭБ передается через различные жидкости организма, в первую очередь, через слюну.
Заразиться ВЭБ можно следующими путями:
·При поцелуях;
·Употреблении пищи и напитков из одной посуды;
·Использовании общих зубных щеток;
·Контакте с игрушками, на которые попала детская слюна;
·Через кровь и сперму при сексуальных контактах;
·При переливаниях крови и трансплантации органов.
Вирус остается жизнеспособным на окружающих объектах по крайней мере пока объект остается влажным. Человек, заразившийся таким образом, может выделять вирус во внешнюю среду даже до развития симптомов и впоследствии, при наличии клинических проявлений болезни, таким образом распространяя инфекцию дальше. Инкубационный период (время от контакта с источником инфекции до развития симптомов) при инфекционном мононуклеозе составляет от 2 дней до 2 месяцев. Наиболее часто этот период длится 5-20 дней.
Клинические проявления инфекционного мононуклеоза это:
• слабость
• лихорадка
• боли в ротоглотке и налеты на миндалинах
• увеличенные лимфатические узлы шеи
• увеличение печени и селезенки
• сыпь
Как правило, симптомы уходят через 2-4 недели. Однако некоторые пациенты могут ощущать слабость в течение нескольких недель и даже месяцев. Затем, как правило, самочувствие нормализуется. Лечение инфекционного мононуклеоза – симптоматическое (жаропонижающие, обильное питье, щадящий режим). Специфическая противовирусная терапия не разработана, и полностью избавиться от вируса невозможно, он, как и все остальные герпес-вирусы, остается в организме человека навсегда.
Однако некоторые пациенты могут ощущать слабость в течение нескольких недель и даже месяцев. Затем, как правило, самочувствие нормализуется. Лечение инфекционного мононуклеоза – симптоматическое (жаропонижающие, обильное питье, щадящий режим). Специфическая противовирусная терапия не разработана, и полностью избавиться от вируса невозможно, он, как и все остальные герпес-вирусы, остается в организме человека навсегда.
С того момента, как произошло заражение, вирус остается в организме, но переходит в латентную (неактивную форму заболевания). Периодически вирус может возобновлять размножение, и в этом случае он обнаруживается в слюне, и может инфицировать окружающих, вне зависимости от того, сколько времени прошло с первичного заражения. То есть человек может быть заразен, даже если у него нет никаких проявлений заболевания.
К сожалению, защитить себя от заболевания инфекционным мононуклеозом довольно сложно. Вакцина против этой инфекции пока не разработана. Можно снизить риск, если не целоваться, не употреблять пищу и напитки из одной посуды, не использовать общие зубные щетки с людьми, которые имеют ВЭБ-инфекцию.
Некоторые вирусные инфекции могут также протекать с клиникой мононуклеоза. К таким вирусами относится ЦМВ и ВИЧ. При первичном заражении этими вирусами развивается клиническая картина, похожая на мононуклеоз. Именно поэтому всем людям с симптомами мононуклеоза настоятельно рекомендуется сдать кровь на антитела к ВИЧ, чтобы вовремя выявить это серьезное заболевание и своевременно назначить терапию.
Автор: врач-инфекционист Дегтярева Светлана Юрьевна
Медицинский редактор: руководитель Университетской клиники, к.м.н., врач-инфекционист Коннов Данила Сергеевич
Возврат к списку
Лечение инфекционного мононуклеоза у детей.
SOVREMENNAYA PEDIATRIYA.2014. 4(60):55-62;doi 10.15574/SP.2014.60.55
4(60):55-62;doi 10.15574/SP.2014.60.55
Лечение инфекционного мононуклеоза у детей.
Крамарьов С. А., Выговская О. В., Тарадий Н. Н., Гриневич А. И.
Национальный медицинский университет имени А.А. Богомольца, г. Киев, Украина
Центр международных медикобиологических исследований НАНУ, г. Киев, Украина
Госинформнауки Украины, г. Киев, Украина
Цель: изучить эффективность использования лекарственного препарата «Флавозид сироп» в комплексном лечении детей, больных инфекционным мононуклеозом (ИМ) ЭБВ-этиологии, в условиях проспективного сравнительного постмаркетингового исследования.
Материалы и методы. Исследование экспрессии дифференцировочных маркеров CD включало изучение экспрессии антигенов CD3+, CD4+, СD8+, CD7+, CD16+, CD20+, CD22+, СD25+, CD45RA+, CD95+. В исследовании приняли участие 120 детей, больных ИМ, в возрасте от 4 месяцев до 18 лет, которые были разделены на две группы по 60 пациентов в каждой. Дети І группы получали базисную терапию в сочетании с препаратом «Флавозид» в возрастной дозировке два раза в сутки в течение 30 дней. Дети ІІ группы получали базисную терапию.
Результаты. У детей, получавших Флавозид, через месяц от начала терапии наблюдалась выраженная положительная динамика со стороны таких клинических симптомов, как интоксикационный, гипертермический синдромы, поражение носоглотки, острый тонзиллит, системная лимфаденопатия, гепатомегалия, гематологические нарушения, достоверное уменьшение частоты выявления анти-ЭБВIgM VCA, ДНК ЭБВ в крови и слюне по сравнению с больными, получавшими только базисную терапию (p<0,05). На фоне применения Флавозида отмечена также выраженная позитивная динамика показателей Т- и В-клеточного иммунитета, свидетельствующая о ликвидации воспалительной реакции и клиническом выздоровлении, отсутствии затяжного инфекционного процесса и угрозы перехода инфекции в хроническую форму.
Выводы. Сироп Флавозид обладает высокой клинической эффективностью, выраженной противовирусной и иммунокоррегирующей активностью при лечении ИМ ЭБВ-этиологии у детей. Применение препарата повышает эффективность базовой терапии ИМ в остром периоде и минимизирует риск перехода острой фазы заболевания в затяжную хроническую форму.
Сироп Флавозид обладает высокой клинической эффективностью, выраженной противовирусной и иммунокоррегирующей активностью при лечении ИМ ЭБВ-этиологии у детей. Применение препарата повышает эффективность базовой терапии ИМ в остром периоде и минимизирует риск перехода острой фазы заболевания в затяжную хроническую форму.
Ключевые слова: инфекционный мононуклеоз, Эпштейна—Барр вирус, дети, лечение, иммуногенез, Флавозид.
Литература:
1. Абатуров ОЄ, Височина ІЛ. 2008. Імунотропний ефект фітопрепарату «Флавозід». Совр педиатрия. 4: 99—102.
2. Блохина ЕБ. 2003. Роль латентной инфекции, вызванной вирусом Эпштейна—Барр, в развитии лимфопролиферативных заболеваний. Вопр гематол, онкол и иммунопатол в педиатрии. 2;3: 65—70.
3. Возіанова ЖІ, Глей АІ. 2005. Інфекційний мононуклеоз, спричинений вірусом Епштейна-Барр. Мистецтво лікування. 5: 8—12.
4. Волоха АП, Чернишова ЛІ. 2003. Епштейн-Барр вірусна інфекція у дітей. Суч інфекції. 4: 79—93.
5. Епштейн-Барр вірусна інфекція. Імунопатогенез. Клініка. Лікування. Метод реком. Під ред. ВЄ Казмірчук. К. 2004: 28.
6. Звіт про доклінічне дослідження безпечності препарату — генерику Флавозід. Інститут екогігієни і токсикології ім. Л.І. Медведя. К. 2004.
7. Иванова ВВ, Камальдинова ЭГ, Левина АС. 2004. Инфекционный мононуклеоз: тактика терапии больных с нелегким течением заболевания : информ. письмо для педиатров. СПб: 24.
8. Исаков ВА, Архипова ЕИ, Исаков ДВ. 2013. Герпесвирусные инфекции человека. Рук-во для врачей. 2-е изд, перераб и доп. СПб, СпецЛит: 670.
9. Краснов ВВ. 2003. Инфекционный мононуклеоз. Клиника, диагностика, современные принципы лечения. Сб ст. СПб-Нижний Новгород: 44.
10. Крючко ТА, Кинаш ЮМ. 2007. Актуальные вопросы лечения герпетической инфекции у детей. Перинатол и педиатрия. 3: 64—68.
11. Кудин АП. Лечение Эпштейн-Барр вирусной инфекции у детей. http://www.bsmu.by.
12. Кудин АП, Романовская ТР, Белевцев МВ. Состояние специфического иммунитета при инфекционном мононуклеозе у детей. http://www bsmu.by.
13. Минцер ОП, Угаров БН, Власов ВВ. 1991. Методы обработки медицинской информации. Учеб пособ. К, Вища школа: 271.
14. Иванова ВВ, Родионова ОВ, Александрова НВ, Железникова ГФ. 2002. Принципы иммуномодулирующей терапии у детей после перенесенного инфекционного мононуклеоза. Интернац журн иммунореабилитации. 4;1: 126.
15. Проведення додаткових доклінічних досліджень нових форм препарату «Протефлазід». Звіт. Інститут епідеміології і інфекційних хвороб ім. ЛВ Громашевського АМН України. К. 2003.
16. Харченко ЮП, Шаповалова ГА. 2007. Застосування препарату флавозід при інфекційному мононуклеозі у дітей. Совр педиатрия. 4: 115—118.
17. Юлиш ЕИ, Волосовец АП. 2005. Врожденные и приобретенные TORCH-инфекции у детей. Донецк, Регина: 216.
18. Roy M, Bailey B, Amre DK et al. 2004. Dexamethasone for the treatment of sore throat in children with suspected infectious mononucleosis: a randomized, double-blind, placebo-controlled, clinical trial. Archiv Pediatric Adolescent Med. 158: 250—254. http://dx.doi.org/10.1001/archpedi.158.3.250; PMid:14993084
19. Cohen JI, Kimura H, Nakamura S et al. 2009. Epstein-Barr virus-associated lymphoproliferative disease in non-immunocompromised hosts: a status report and summary of an international meeting, 8—9 September 2008. Ann Oncol. 20(9): 1472—1482. http://dx.doi.org/10.1093/annonc/mdp064; PMid:19515747 PMCid:PMC2731018
20. Foerster J. 1999. Infectious mononucleosis. Lee. Wintrobe’s Clinical Hematology. 10th ed. 1926—1955.
21. Gershburg E, Pagano JS. 2005. Epstein—Barr infections: prospects for treatment. J of Antimicrobial Chemotherapy. 56;2: 277—281. http://dx.doi.org/10.1093/jac/dki240; PMid:16006448
22. Kawa K. 2000. Epstein—Barr virus_associated diseases in humans. Inf J Hematol. 71: 108—117. PMid:10745621
71: 108—117. PMid:10745621
23. Craig MV, Clare N, Skar JL, Banks PM. 1992. T-cell lymphoma and virus_associated hemophagocytic syndrome. Am J Clin Pathol. 97: 189—94.
24. Faulkner GC, Krajewski AS, Crawford DH. 2000. The infectious mononucleosis and outs of EBV infеction. Trends in Microiology. 8: 185—189.
Детский мононуклеоз и вирусная инфекция Эпштейна-Барра: основы практики, предпосылки, патофизиология
Dunmire SK, Hogquist KA, Balfour HH. Инфекционный мононуклеоз. Curr Top Microbiol Immunol . 2015. 390 (Pt 1): 211-40. [Медлайн]. [Полный текст].
Али А.С., Аль-Шраим М., Аль-Хаками А.М., Джонс И.М. Вирус Эпштейна-Барра: клинические и эпидемиологические обзоры и генетические основы онкогенеза. Откройте Virol J . 2015 г. 3. 9: 7-28.[Медлайн]. [Полный текст].
EPSTEIN MA, ACHONG BG, BARR YM. ЧАСТИЦЫ ВИРУСА В КУЛЬТУРНЫХ ЛИМФОБЛАСТАХ ЛИМФОМЫ БЕРКИТТА. Ланцет . 1964, 28 марта, 1 (7335): 702-3. [Медлайн]. [Полный текст].
Эпштейн MA. Частицы вируса в культивируемых лимфобластах лимфомы Беркитта. Ланцет . 1964. 1: 702.
Хенле Г., Хенле В., Диль В. Связь вируса герпеса, связанного с опухолью Беркитта, с инфекционным мононуклеозом. Proc Natl Acad Sci U S A . 1968, январь, 59 (1): 94-101. [Медлайн].
Сойер Р.Н., Эванс А.С., Нидерман Дж.С., Макколлум Р.В. Перспективные исследования группы первокурсников Йельского университета. I. Возникновение инфекционного мононуклеоза. J Заразить Dis . 1971, март, 123 (3): 263-70. [Медлайн].
Данмир, СК, Хогквист, КА, Бальфур, HH. Инфекционный мононуклеоз. Curr Top Microbiol Immunol . 2015. 390 (Pt 1): 211-40. [Медлайн].
Инфекционный мононуклеоз. Curr Top Microbiol Immunol . 2015. 390 (Pt 1): 211-40. [Медлайн].
Lung ML, Cheung AK, Ko JM, Lung HL, Cheng Y, Dai W. Взаимодействие генетических факторов хозяина и вируса Эпштейна-Барра в развитии карциномы носоглотки. Рак подбородка J . 2014 ноябрь 33 (11): 556-68. [Медлайн].
Мишра Б., Мохан Б., Ратхо, РК. Инфекционный мононуклеоз, положительный по гетерофильным антителам. Индиан Дж. Педиатр . 2004, январь 71 (1): 15-8. [Медлайн].
Джозеф С. Пагано.Передается ли вирус Эпштейна-Барра половым путем ?. Журнал инфекционных болезней, . 15 февраля 2007 г. Том 195. вып. 4, стр. 469–470. [Полный текст].
Гербер П., Уолш Дж. Х., Розенблюм EN, Перселл Р. Ассоциация EB-вирусной инфекции с постперфузионным синдромом. Ланцет . 1969 22 марта. 1 (7595): 593-5. [Медлайн].
Hanto DW, Frizzera G, Purtilo DT, Sakamoto K, Sullivan JL, Saemundsen AK и др. Клинический спектр лимфопролиферативных нарушений у реципиентов почечного трансплантата и доказательства роли вируса Эпштейна-Барра. Cancer Res . 1981, ноябрь 41 (11, часть 1): 4253-61. [Медлайн]. [Полный текст].
Lockey TD, Zhan X, Surman S, Sample CE, Hurwitz JL. Разработка вакцины против вируса Эпштейна-Барра: коктейль литического и латентного белка. Передний Biosci . 2008 г. 1 мая. 13: 5916-27. [Медлайн]. [Полный текст].
Cohen JI. Разработка вакцины против вируса Эпштейна-Барра. Adv Exp Med Biol . 2018. 1045: 477-493. [Медлайн].
Balfour HH Jr, Данмир, СК, Хогквист, К.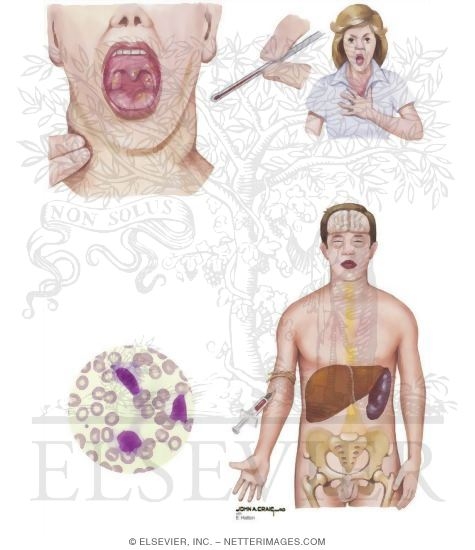 А.Инфекционный мононуклеоз. Clin Transl Immunology . 2015 Февраль 4 (2): e33. [Медлайн].
А.Инфекционный мононуклеоз. Clin Transl Immunology . 2015 Февраль 4 (2): e33. [Медлайн].
Лимфома Эпштейна А. Беркитта и открытие вируса Эпштейна-Барра. Br J Haematol . 2012 Март 156 (6): 777-9. [Медлайн].
Zhang X, Dawson CW, He Z, Huang P. Стратегии иммунного уклонения человеческих гамма-герпесвирусов: последствия для вирусного туморогенеза. J Med Virol . 2012 Февраль 84 (2): 272-81. [Медлайн].
Hjalgrim H, Askling J, Sorensen P, Madsen M, Rosdahl N, Storm HH и др.Риск болезни Ходжкина и других видов рака после инфекционного мононуклеоза. Национальный институт рака . 2000. 92: 1522.
Лангер-Гулд А., Ву Дж., Лукас Р., Смит Дж., Гонсалес Е., Амезкуа Л. и др. Восприимчивость к вирусу Эпштейна-Барра, цитомегаловирусу и рассеянному склерозу: многоэтническое исследование. Неврология . 2017 26 сентября. 89 (13): 1330-1337. [Медлайн].
Crawford DH, Macsween KF, Higgins CD, Thomas R, McAulay K, Williams H, et al.Когортное исследование среди студентов университетов: определение факторов риска сероконверсии и инфекции вируса Эпштейна-Барра. Clin Infect Dis . 2006. 43: 276–282. [Полный текст].
Лоуренс С. Янг и Кристофер У. Доусон. Вирус Эпштейна-Барра и рак носоглотки. Рак подбородка J . 2014 декабрь 33 (12): 581–590. [Медлайн].
Luzuriaga K, Sullivan JL. Инфекционный мононуклеоз. N Engl J Med . 2010 май.27; 362 (21): 1993-2000. [Полный текст].
Dowd JB, Palermo T, Brite J, McDade TW, Aiello A. Распространенность вирусной инфекции Эпштейна-Барра у детей в возрасте 6-19 лет в США, 2003-2010 гг.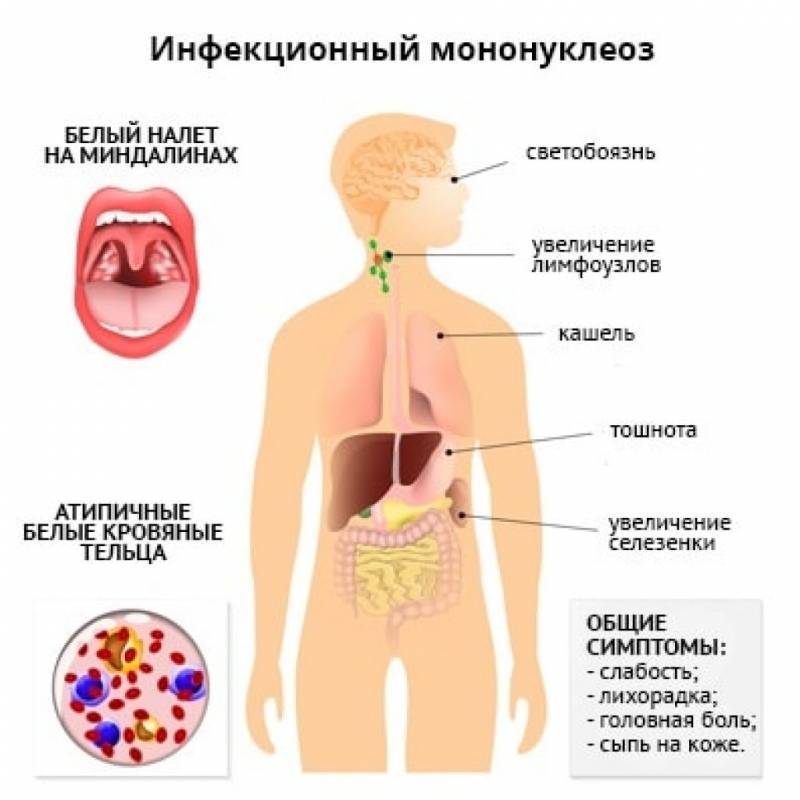 PLoS One . 2013. 8 (5): e64921. [Медлайн].
PLoS One . 2013. 8 (5): e64921. [Медлайн].
Госе Л., Винтер-младший, Тейлор Г.С., Льюис Дж. Э., Стэг Х. Моделирование динамики передачи EBV для информирования профиля целевого продукта вакцины и будущей стратегии вакцинации. Научный сотрудник . 2019 июн 26.9 (1): 9290. [Медлайн].
Lung ML, Chang GC, Miller TR, Wara WM, Phillips TL. Генотипический анализ изолятов вируса Эпштейна-Барр, ассоциированных с карциномой носоглотки у китайских иммигрантов в США. Инт Дж. Рак . 1994 15 декабря. 59 (6): 743-6. [Медлайн].
Кац Б.З., Сираиси Ю., Мирс К.Дж., Биннс Х.Дж., Тейлор Р. Синдром хронической усталости после инфекционного мононуклеоза у подростков. Педиатрия . 2009 июл.124 (1): 189-93. [Медлайн]. [Полный текст].
Candy B, Chalder T, Cleare AJ и др. Предикторы утомляемости после начала инфекционного мононуклеоза. Психол Мед . 2003 июл.33 (5): 847-55. [Медлайн].
Флавелл Дж. Р., Баумфорт К. Р., Вуд В. Х. и др. Подавление целевого гена TGF-бета, PTPRK, вирусом Эпштейна-Барра, кодируемым EBNA1, способствует росту и выживанию клеток лимфомы Ходжкина. Кровь .2008 г., 1. 111 (1): 292-301. [Медлайн]. [Полный текст].
Баумфорт К.Р., Биргерсдоттер А., Рейнольдс Г.М. и др. Экспрессия ядерного антигена 1 вируса Эпштейна-Барра, кодируемого вирусом Эпштейна-Барра, в клетках лимфомы Ходжкина опосредует повышающую регуляцию CCL20 и миграцию регуляторных Т-клеток. Ам Дж. Патол . 2008 июль 173 (1): 195-204. [Медлайн]. [Полный текст].
Чаганти С., Ма С.С., Белл А.И. и др. Персистенция вируса Эпштейна-Барра в отсутствие обычных В-клеток памяти: IgM + IgD + CD27 + В-клетки несут вирус у пациентов с Х-сцепленным лимфопролиферативным заболеванием. Кровь . 2008, 1 августа. 112 (3): 672-9. [Медлайн].
Domachowske JB. Инфекционные триггеры гемофагоцитарного синдрома у детей. Pediatr Infect Dis J . 2006 25 ноября (11): 1067-8. [Медлайн].
Томпсон Д.Ф., Рамос КЛ. Сыпь, вызванная антибиотиками, у пациентов с инфекционным мононуклеозом. Энн Фармакотер . 2017 Февраль 51 (2): 154-162. [Медлайн].
Фарли Д.Р., Цитлоу С.П., Бэннон М.П., Фарнелл МБ.Самопроизвольный разрыв селезенки из-за инфекционного мононуклеоза. Mayo Clin Proc . 1992 сентябрь 67 (9): 846-53. [Медлайн].
Бартлетт А., Уильямс Р., Хилтон М. Разрыв селезенки при инфекционном мононуклеозе: систематический обзор опубликованных отчетов о случаях. Травма . 2016 Март 47 (3): 531-8. [Медлайн].
Стивенсон Дж. Т., Дюбуа Дж. Дж. Неоперативное лечение спонтанного разрыва селезенки при инфекционном мононуклеозе: описание случая и обзор литературы. Педиатрия . 2007 августа 120 (2): e432-5. [Медлайн].
Heo DH, Baek DY, Oh SM, Hwang JH, Lee CS, Hwang JH. Инфаркт селезенки, связанный с острым инфекционным мононуклеозом, вызванным инфекцией вируса Эпштейна-Барра. J Med Virol . 2017 Февраль 89 (2): 332-336. [Медлайн].
Thacker EL, Mirzaei F, Ascherio A. Инфекционный мононуклеоз и риск рассеянного склероза: метаанализ. Энн Нейрол . 2006 Март 59 (3): 499-503.[Медлайн].
Грин М, Майклс МГ. Инфекция, вызванная вирусом Эпштейна-Барра, и посттрансплантационное лимфопролиферативное заболевание. Трансплантат Am J . 2013 фев. 13 Дополнение 3: 41-54; викторина 54. [Medline].
2013 фев. 13 Дополнение 3: 41-54; викторина 54. [Medline].
Вассерман Д.Х., Гир Р.Дж., Вильямс П.Е., Беккер Т., Лейси Д.Б., Абумрад Н.Н. Взаимодействие кишечника и печени в метаболизме азота во время упражнений. Метаболизм . 1991 Март 40 (3): 307-14. [Медлайн].
Лернер А.М., Бекадж С.Х., Дитер Р.Г., Фицджеральд Дж. Т..Лечение валацикловиром при синдроме хронической усталости подгруппы вируса Эпштейна-Барра: наблюдение через тридцать шесть месяцев. In Vivo . 2007 сентябрь-октябрь. 21 (5): 707-13. [Медлайн].
Когельник А.М., Лумис К., Хуг-Петерсен М., Россо Ф., Хишьер С., Монтойя Дж. Применение валганцикловира у пациентов с повышенными титрами антител против вируса герпеса человека-6 (HHV-6) и вируса Эпштейна-Барра (EBV), которые страдали дисфункцией центральной нервной системы, включая длительную усталость. Дж. Клин Вирол .2006 декабрь 37 Приложение 1: S33-8. [Медлайн].
Moretti M, Lava SAG, Zgraggen L, Simonetti GD, Kottanattu L, Bianchetti MG, et al. Острое повреждение почек при симптоматическом первичном инфекционном мононуклеозе вируса Эпштейна-Барра: систематический обзор. Дж. Клин Вирол . 2017 июн. 91: 12-17. [Медлайн].
Ким А., Ян Х. Р., Мун Дж. С., Чанг Дж. Й., Ко Дж. С. Инфекция вируса Эпштейна-Барра при остром бескаменном холецистите. Гастроэнтерол педиатр Hepatol Nutr .2014 17 марта (1): 57-60. [Медлайн].
Кимура Х, Хосино Й, Канеган Х, Цуге И, Окамура Т, Кава К. и др. Клинико-вирусологическая характеристика хронической активной инфекции вирусом Эпштейна-Барра. Кровь . 2001 г. 15 июля. 98 (2): 280-6. [Медлайн].
webmd.com”> Севье, TL. Инфекционное заболевание у спортсменов. Med Clin North Am . 1994 г., 78 (2): 389-412. [Медлайн].
МАРК Х. ЭБЕЛЛ. Инфекционный мононуклеоз вируса Эпштейна-Барра. Американский семейный врач . 2004 Октябрь. 70 (7): 1279-86.
Dunmire SK1, Verghese PS2, Balfour HH Jr. Первичная инфекция вирусом Эпштейна-Барра. Дж. Клин Вирол . 2018. 102: 84-92. [Полный текст].
HOAGLAND RJ. КРИТЕРИИ ДИАГНОСТИКИ ИНФЕКЦИОННОГО МОНОНУКЛЕОЗА. Среднее время . 1965 июн. 93: 663-5. [Медлайн].
Фьельде А. Природа инфекционного мононуклеоза и роль клеток Дауни. Программа Clin Biol Res . 1983. 133: 215-20. [Медлайн].
Seitanidis B. Сравнение теста Monospot с тестом Пола-Баннелла при инфекционном мононуклеозе и других заболеваниях. Дж. Клин Патол . 1969 Май. 22 (3): 321-3. [Медлайн].
Маршалл-Андон Т., Хайнц П. Как использовать… тесты на моноспот и другие гетерофильные антитела. Arch Dis. Детское обучение, изд. . 2017 Август 102 (4): 188-193. [Медлайн].
Майкельсон П., Уоткинс Б., Уэббер С.А., Вадовски Р., Майклс М.Г.Скрининг на наличие PTLD у реципиентов легких и трансплантатов сердце-легкие путем измерения нагрузки ДНК ВЭБ в жидкости бронхоальвеолярного лаважа с использованием ПЦР в реальном времени. Педиатр-трансплант . 2008 июн. 12 (4): 464-8. [Медлайн].
Де Паор М., О’Брайен К., Фэхи Т. и др. Противовирусные средства при инфекционном мононуклеозе (железистой лихорадке). Кокрановская база данных Syst Rev . 2016 8 декабря; 12: [Полный текст].
Тайнелл Э., Аврелий Э., Бранделл А., Джуландер I, Вуд М., Яо QY и др.Лечение острого инфекционного мононуклеоза ацикловиром и преднизолоном: многоцентровое двойное слепое плацебо-контролируемое исследование. J Заразить Dis . 1996 Август 174 (2): 324-31. [Медлайн].
Candy B, Chalder T, Cleare AJ, Wessely S, Hotopf M. Рандомизированное контролируемое испытание психолого-педагогического вмешательства для выздоровления при инфекционном мононуклеозе. J Psychosom Res . 2004 Июль 57 (1): 89-94. [Медлайн].
Коэн Дж. И., Яффе Э. С., Дейл Дж. К., Питталуга С., Хеслоп Х. Э., Руни С. М. и др.Характеристика и лечение хронической активной болезни, вызванной вирусом Эпштейна-Барра: 28-летний опыт работы в США. Кровь . 2 июня 2011 г. 117 (22): 5835-49. [Медлайн].
[Рекомендации] Стычински Дж., Ван дер Вельден В., Фокс С. П. и др. Ведение инфекций, вызванных вирусом Эпштейна-Барра, и посттрансплантационных лимфопролиферативных заболеваний у пациентов после трансплантации аллогенных гемопоэтических стволовых клеток: рекомендации Шестой Европейской конференции по инфекциям при лейкемии (ECIL-6). Haematologica . 2016 июл.101 (7): 803-11. [Медлайн]. [Полный текст].
Ма Ц., Вонг С.К., Вонг Б.К., Чан К.С., Лун С.В., Ли Н. и др. Цитокиновые ответы в тяжелом случае железистой лихорадки успешно лечили фоскарнетом в сочетании с преднизолоном и внутривенным иммуноглобулином. J Med Virol . 2009 Январь 81 (1): 99-105. [Медлайн].
Oertel SH, Riess H. Противовирусное лечение лимфопролифераций, связанных с вирусом Эпштейна-Барра. Последние результаты Cancer Res . 2002. 159: 89-95. [Медлайн].
2002. 159: 89-95. [Медлайн].
Schneider U, Ruhnke M, Delecluse HJ, Stein H, Huhn D. Регрессия лимфопролиферативных нарушений, связанных с вирусом Эпштейна-Барра, у пациентов с синдромом приобретенного иммунодефицита во время терапии фоскарнетом. Энн Гематол . 2000 апр. 79 (4): 214-6. [Медлайн].
Knorr B, Kessler U, Pöschl J, Fickenscher H, Linderkamp O. Гемофагоцитарный лимфогистиоцитоз (HLH) -подобная картина после цитомегаловирусной инфекции, передаваемой через грудное молоко, у недоношенного ребенка. Scand J Infect Dis . 2007. 39 (2): 173-6. [Медлайн].
Cheeseman SH, Henle W., Rubin RH, et al. Инфекция вируса Эпштейна-Барра у реципиентов почечного трансплантата. Эффекты антитимоцитарного глобулина и интерферона. Энн Интерн Мед. . Июль 1980 г. 93 (1): 39-42. [Медлайн].
Резник Л., Хербст Дж. С., Аблаши Д. В. и др. Регрессия волосистой лейкоплакии полости рта после перорального приема ацикловира. JAMA . 15 января 1988 г.259 (3): 384-8. [Медлайн].
Schooley RT, Carey RW, Miller G и др. Хроническая инфекция вируса Эпштейна-Барра, связанная с лихорадкой и интерстициальным пневмонитом. Клинические и серологические особенности и ответ на противовирусную химиотерапию. Энн Интерн Мед. . 1986 Май. 104 (5): 636-43. [Медлайн].
Сайран Э.М., Роу Дж. М., Блум RE. Внутривенное лечение гаммаглобулином при иммунной тромбоцитопении, связанной с инфекционным мононуклеозом. Ам Дж. Гематол .1991 Октябрь 38 (2): 124-9. [Медлайн].
Коэн Дж. И., Мокарски Е. С., Рааб-Трауб Н., Кори Л., Набель Г. Дж. Необходимость и проблемы разработки вакцины против вируса Эпштейна-Барра.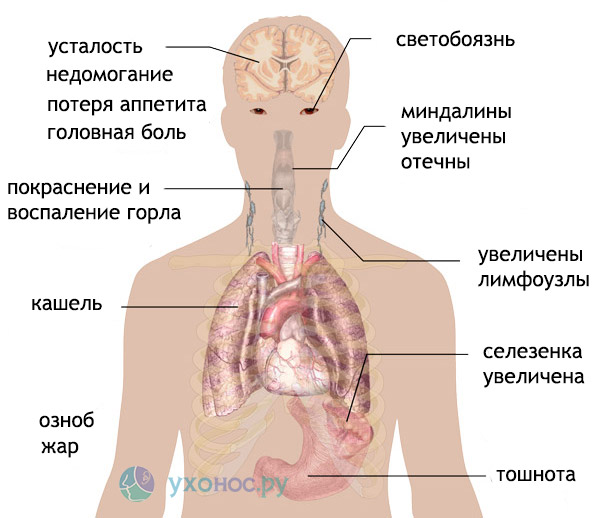 Вакцина . 2013 г., 18 апреля. 31 Прил. 2: B194-6. [Медлайн].
Вакцина . 2013 г., 18 апреля. 31 Прил. 2: B194-6. [Медлайн].
Сокал Е.М., Хоппенбрауэрс К., Вандермёлен С., Маутшен М., Леонар П., Морелс А. и др. Рекомбинантная вакцина gp350 от инфекционного мононуклеоза: рандомизированное двойное слепое плацебо-контролируемое исследование фазы 2 для оценки безопасности, иммуногенности и эффективности вакцины против вируса Эпштейна-Барра у здоровых молодых людей. J Заразить Dis . 2007 15 декабря. 196 (12): 1749-53. [Медлайн].
Balfour HH Jr. Прогресс, перспективы и проблемы в разработке вакцины против вируса Эпштейна-Барра. Curr Opin Virol . 2014 июн. 6: 1-5. [Медлайн].
Бартлетт А., Уильямс Р., Хилтон М. Разрыв селезенки при инфекционном мононуклеозе: систематический обзор опубликованных отчетов о случаях. Травма . 2016 Март 47 (3): 531-8. [Медлайн].
Hsieh WC, Chang Y, Hsu MC, et al.Появление антител к эритроцитам запускает фагоцитоз эритроцитов активированными макрофагами на кроличьей модели гемофагоцитарного синдрома, связанного с вирусом Эпштейна-Барра. Am Jour Path . May 2007. 170 (5): 1629-39. [Медлайн].
Окано М, Брутто ТГ. Гемофагоцитарный синдром, связанный с вирусом Эпштейна-Барра, и фатальный инфекционный мононуклеоз. Ам Дж. Гематол . Октябрь 1996. 53 (2): 111-5. [Медлайн].
Maakaroun NR, Moanna A, Jacob JT, Albrecht H.Вирусные инфекции, связанные с гемофагоцитарным синдромом. Rev Med Virol . 1 февраля 2010 г. [Medline].
Rea TD, Russo JE, Katon W, Ashley RL, Buchwald DS. Проспективное изучение естественного течения инфекционного мононуклеоза, вызванного вирусом Эпштейна-Барра. J Am Board Fam Pract . 2001 июль-август. 14 (4): 234-42. [Медлайн].
J Am Board Fam Pract . 2001 июль-август. 14 (4): 234-42. [Медлайн].
Гу SY, Хуанг TM, Руань Л., Мяо Й.Х., Лу Х., Чу С.М. и др. Первое испытание вакцины против ВЭБ на людях с использованием рекомбинантного вируса осповакцины, экспрессирующего основной мембранный антиген. Дев Биол Стенд . 1995. 84: 171-7. [Медлайн].
Rostgaard K, Wohlfahrt J, Hjalgrim H. Генетическая основа инфекционного мононуклеоза: данные семейного исследования госпитализированных случаев в Дании. Clin Infect Dis . 2014 июн 58 (12): 1684-9. [Медлайн].
Харли Дж. Б., Чен Х, Пуджато М., Миллер Д., Мэддокс А., Форни С. и др. Факторы транскрипции действуют во всех локусах болезни, при этом EBNA2 участвует в аутоиммунитете. Нат Генет .2018 май. 50 (5): 699-707. [Медлайн].
Халворсен Дж. А., Бревиг Т., Аас Т., Скар А. Г., Слеволден Е. М., Мой Х. Генитальные язвы как начальное проявление инфекции, вызванной вирусом Эпштейна-Барра: два новых случая и обзор литературы. Acta Derm Venereol . 2006. 86 (5): 439-42. [Медлайн].
Wingate PJ, McAulay KA, Anthony IC, Crawford DH. Регуляторная активность Т-клеток при первичной и персистирующей инфекции вируса Эпштейна-Барра. J Med Virol .2009 Май. 81 (5): 870-7. [Медлайн].
Cohen JI. Первичные иммунодефициты, связанные с заболеванием EBV. Curr Top Microbiol Immunol . 2015. 390 (Pt 1): 241-65. [Медлайн].
Вецика Е.К., Каллан М. Инфекционный мононуклеоз и вирус Эпштейна-Барра. Эксперт Рев Мол Мед . 2004 г. 5. 6 (23): 1-16. [Медлайн].
Чеджановский Н., Закай Н., Амселем С., Баренхольц Ю., Лойтер А. Мембранные везикулы, содержащие гликопротеин, связывающий вирус Сендай, но не вирусный гибридный белок, сливаются с липосомами фосфатидилсерина при низком pH. Биохимия . 1986 26 августа, 25 (17): 4810-7. [Медлайн].
Хан Г, Хашим МДж. Глобальное бремя смертей от злокачественных новообразований, связанных с вирусом Эпштейна-Барра, 1990-2010 гг. Заражение возбудителем рака . 2014. 9 (1): 38. [Медлайн].
Де Паор М., О’Брайен К., Фэхи Т., Смит С.М. Противовирусные средства при инфекционном мононуклеозе (железистой лихорадке). Кокрановская база данных Syst Rev . 2016 8 декабря. 12: CD011487. [Медлайн].
Hsu JL, Glaser SL.Злокачественные новообразования, связанные с вирусом Эпштейна-Барра: эпидемиологические закономерности и этиологические последствия. Crit Rev Oncol Hematol . 2000 апр. 34 (1): 27-53. [Медлайн].
Мононуклеоз
Мононуклеоз, также известный как «мононуклеоз», обычно вызывается микробом, который называется вирусом Эпштейна-Барра. Другие вирусы, такие как ЦМВ и ВИЧ, и другие инфекции, такие как токсоплазмоз, также могут вызывать мононуклеоз. Хотя мононуклеоз наиболее известен тем, что вызывает опухание желез и усталость, он может принимать разные формы.Большинство детей с моно выздоравливают без каких-либо проблем. Но болезнь может пройти долго. В некоторых случаях моно может вызвать проблемы с печенью, селезенкой или сердцем. Поэтому важно, чтобы моно был диагностирован и за ребенком внимательно наблюдали.
Причины мононуклеозаMono может легко передаваться через слюну инфицированного человека через:
- Пить и есть после них
- Совместное использование соломинки, чашки, зубных щеток и столовых приборов
- Поцелуи и близкий контакт
- Обращение с игрушками с детьми слюни
Общие симптомы у детей включают:
- Усталость, слабость
- Лихорадка
- Боль в горле
- Болезненные или опухшие лимфатические узлы на шее или подмышках
- Опухшие миндалины ,00
- Сыпь
- Боль в мышцах или скованность
- Головная боль
- Потеря аппетита, тошнота
- Тупая боль в области живота
- Увеличенные печень и селезенка
- Головные боли
- Пухлые глаза
- Светочувствительность
Мононуклеоз может быть диагностирован с помощью простого анализа крови, выполненного вашим врачом.
Лечение мононуклеозаПоскольку это вирусная инфекция, антибиотики не излечивают моно. Лечащий врач вашего ребенка может прописать лекарства, которые помогут облегчить боль или дискомфорт вашего ребенка. Лучшее лечение моно – отдых. Ребенку с моно также следует пить много жидкости. Чтобы помочь вашему ребенку почувствовать себя лучше и быстрее выздороветь:
- Убедитесь, что ребенок много отдыхает.
- Держите ребенка в тепле.
- Давайте ребенку много жидкости, например воды или яблочного сока.
- Не позволяйте никому курить рядом с ребенком.
- Убедитесь, что ваш ребенок в течение месяца избегает контактных видов спорта и подъема тяжестей, чтобы не повредить селезенку. Во время этой болезни может увеличиваться селезенка. Обсудите с лечащим врачом вашего ребенка, когда он или она сможет вернуться к нормальной деятельности.
- Лечите у ребенка жар, боль в горле или мышечные боли с помощью детского ацетаминофена или ибупрофена. Никогда. не давайте ребенку аспирин.
Симптомы обычно длятся несколько недель, но иногда могут длиться от 1 до 2 месяцев или дольше.Даже после того, как симптомы исчезнут, ваш ребенок может некоторое время чувствовать усталость или слабость.
Предотвращение распространения мононуклеозаПока вы ухаживаете за ребенком с моно:
- Часто мойте руки теплой водой с мылом, особенно до и после ухода за больным ребенком.
- Следите за своим здоровьем и здоровьем других членов семьи
- Ограничьте контакт больного ребенка с другими детьми.
- Посуду и столовые приборы, используемые больным ребенком, следует мыть отдельно в очень горячей мыльной воде.Или пропустите их в посудомоечной машине.
Немедленно позвоните поставщику медицинских услуг, если ваш ребенок в остальном здоров:
- Младенец младше 3 месяцев с ректальной температурой 100,4 ° F (38 ° C) или выше
- Является ли ребенок любого возраста, у которого повторяется температура 104 ° F (40 ° C) или выше
- Имеет лихорадку, которая держится более 24 часов у ребенка в возрасте до 2 лет или в течение 3 дней у ребенка в возрасте 2 лет и старше
- Был припадок, вызванный лихорадкой
- Испытывает затрудненное или учащенное дыхание.
- Не успокаивается, проявляет признаки раздражительности или беспокойства.
- Кажется необычно сонным, вялым или безразличным.
- Имеет проблемы с едой, питьем или глотанием.
- Прекращает дыхание даже на мгновение.
- Показывает признаки сильной боли в груди, шее или животе.
Инфекционный мононуклеоз | DermNet NZ
Автор: д-р Сара Хилл, регистратор дерматологии, больница Вайкато, Гамильтон, Новая Зеландия, 2007 г.Обновлено доктором Кэтрин Тиан, сотрудником городской больницы Окленда. Главный редактор DermNet в Новой Зеландии: доцент А / профессор Аманда Окли, дерматолог, Гамильтон, Новая Зеландия. Медицинский редактор: д-р Хелен Гордон, Окленд, Новая Зеландия. Копия отредактирована Гасом Митчеллом. Август 2020.
Добавьте фото инфекционного мононуклеоза
Что такое инфекционный мононуклеоз?
Инфекционный мононуклеоз – распространенное инфекционное заболевание, вызываемое вирусом Эпштейна-Барра (ВЭБ). Это более широко известно как железистая лихорадка.
Кто заболевает инфекционным мононуклеозом?
Инфекционный мононуклеоз обычно поражает молодых людей в возрасте 15–25 лет. Он одинаково распространен у представителей обоих полов и поражает все расы. Почти 95% людей переболели ВЭБ к тому времени, когда они стали взрослыми. Заболевание встречается во всем мире без сезонной предрасположенности.
Что вызывает инфекционный мононуклеоз?
Инфекционный мононуклеоз – это заразная вирусная инфекция, обычно вызываемая ВЭБ (человеческий герпесвирус-4, HHV4), ДНК-вирусом гамма-герпеса.ВЭБ вовлечен в широкий спектр заболеваний человека, многие из которых имеют кожно-слизистые проявления, которые могут быть острыми или хроническими.
Как передается инфекционный мононуклеоз?
ВЭБ передается от человека к человеку через слюну при интимных контактах, таких как поцелуи, или через такие предметы, как зубная щетка или стакан для питья. Вирус выживает на объекте, пока он остается влажным. ВЭБ также может передаваться через кровь и сперму во время полового контакта, переливания крови, трансплантации органов и других процедур.Предполагается, что дети передаются от родителей или братьев и сестер, которые переносят ВЭБ и периодически передают вирус.
Каковы клинические признаки инфекционного мононуклеоза?
Клинические проявления инфекции зависят от взаимодействия вируса и иммунной системы хозяина. Инкубационный период от контакта до появления симптомов обычно составляет 6-7 недель.
Первичная инфекция EBV
Инфекционный мононуклеоз обычно встречается у 75% молодых людей; 15% имеют атипичное проявление, а у 10% инфекция протекает бессимптомно.У детей часто протекает бессимптомно или предполагается, что у них неспецифическая вирусная инфекция.
Есть два типичных проявления:
- внезапное начало тяжелой ангины с шейной лимфаденопатией
- постепенное начало субфебрильной лихорадки, недомогания, артралгии и миалгии.
Селезенка и печень
- Спленомегалия (увеличение селезенки), обычно на второй и третьей неделях
- Связанная боль или дискомфорт в животе
- Гепатомегалия редко пальпируется клинически, хотя часто обнаруживается на УЗИ
- Повышение уровня печеночных трансаминаз обычно до 50%
- Явный гепатит с желтухой и болезненной гепатомегалией встречается у 5-10%
- Пожилые люди более склонны к развитию гепатомегалии и желтухи, чем подростки.
Суставы
- Артрит одного или нескольких суставов
Почки
Нервная система
- Асептический менингит
- Паралич лицевого нерва
- Поперечный миелит
- Периферический неврит, неврит зрительного нерва
- Церебеллит
- Синдром Гийена-Барре
- Менингоэнцефалит
Легкие
- Обструкция дыхательных путей
- Интерстициальная пневмония
Сердце
Глаза
- Периорбитальный отек и век (признак Хогланда)
- Конъюнктивит
- Кератит
- Увеит
- Ретинит
Система крови
Каковы кожно-слизистые особенности инфекционного мононуклеоза?
Типичная экзантема инфекционного мононуклеоза – острая генерализованная макулопапулезная сыпь.Экзантема:
- Поражает от 4,2 до 13% пациентов, не принимающих антибиотики
- Обычно слабый и без зуда, сначала появляется на туловище и плечах, распространяется на лицо и предплечья.
- Может быть болезненной, папулезной, скарлатинообразной, везикулярной или пурпурной
- Разрешается примерно через неделю.
Более интенсивная и обширная кожная сыпь появляется почти у 90% пациентов с инфекционным мононуклеозом через 2–10 дней после начала приема антибиотиков.К ним относятся ампициллин, азитромицин, амоксициллин, цефалоспорины, тетрациклины и макролиды, такие как эритромицин. Недавние исследования показывают, что фактическая частота появления этой сыпи, вызванной антибиотиками, намного ниже, чем сообщалось ранее.
- Лекарственная сыпь представляет собой зудящую пятнисто-папулезную или болезненную сыпь.
- Поражает разгибательные поверхности и точки давления, лицо, шею, туловище, ладони и подошвы.
- Может поражать слизистые оболочки.
- Сыпь обычно проходит в течение недели после отмены антибиотика.
Лекарственная аллергия обычно преходящая. Однако повторное воздействие антибиотика может иногда приводить к рецидиву сыпи спустя годы.
Небные петехии обнаруживаются на твердом и мягком небе у 50% молодых людей в первые дни болезни.
Холестатическая желтуха, вызванная поражением печени, проявляется зудом, приводящим к ссадинам и синякам.
К другим, менее часто встречающимся кожным признакам инфекционного мононуклеоза относятся иммунная тромбоцитопеническая пурпура, холодовая крапивница и узловатая эритема.
Кожные признаки инфекционного мононуклеоза
Скрытый EBV
После острой симптоматической фазы EBV сохраняется в В-клетках памяти в миндалинах и периферическом кровообращении инфицированного хозяина в латентном нелетальном состоянии носителя на протяжении всей жизни. Вирус может распространяться с перерывами, а инфекция может снова активироваться.
Как диагностируется инфекционный мононуклеоз?
Клинических особенностей и положительного гетерофильного теста обычно достаточно для диагностики инфекционного мононуклеоза.
Гетерофильные антитела (Monospot)
- Гетерофильные антитела становятся положительными через 2–9 недель после заражения; чувствительность составляет 70–92% в первые две недели.
- Они могут сохраняться год и более.
- Примерно у 40% детей младше 4 лет не вырабатываются гетерофильные антитела после первичной инфекции EBV.
- Гетерофильные антитела неспецифичны и могут присутствовать при других инфекциях, злокачественных новообразованиях и аутоиммунных заболеваниях.
Другие анализы крови
- Уровни лимфоцитов повышены, при этом не менее 10% являются атипичными. При других вирусных инфекциях наблюдается снижение лимфоцитов.
- Иммуноглобулин (Ig) M к антигену вирусного капсида (VCA) во время активной фазы инфекционного мононуклеоза обнаруживается у 75% пациентов и обычно исчезает в течение 4–6 недель.
- VCA IgG-антитела достигают максимума примерно через 2–4 недели после появления симптомов, а затем слегка снижаются. Они могут сохраняться всю жизнь.
- Другие тесты оценивают ранний антиген (EA) EBV и ядерный антиген (EBNA).
- Высокие нагрузки EBV обнаруживаются с помощью полимеразной цепной реакции (ПЦР) в полости рта и крови во время острой клеточной литической фазы.
- Функциональные пробы печени часто показывают повышенный уровень трансаминаз.
- Другие тесты будут зависеть от того, какие органы поражены инфекцией.
Визуализация
УЗИ брюшной полости может оценить гепатоспленомегалию.
Что такое дифференциальный диагноз инфекционного мононуклеоза?
Основными дифференциальными диагнозами острого инфекционного мононуклеоза являются:
Другие дифференциальные диагнозы включают стрептококковый фарингит (который может сосуществовать), лейкоз, тонзиллит, дифтерию, простуду, грипп и COVID-19.
Как лечить инфекционный мононуклеоз?
Варианты лечения инфекционного мононуклеоза обычно носят поддерживающий характер, например:
Менее распространенные варианты лечения включают:
- Противовирусные препараты, такие как ацикловир или валацикловир, не используются или полезны при неосложненных случаях инфекционного мононуклеоза. Иногда их назначают при менингите ВЭБ, периферическом неврите, гепатите или при гематологических осложнениях.
- Антибиотики могут быть назначены для лечения подтвержденной вторичной бактериальной инфекции.
Можно ли предотвратить инфекционный мононуклеоз?
В настоящее время вакцины для защиты от EBV-инфекции не существует. Профилактика предполагает соблюдение социальной гигиены и недопущение совместного использования напитков, еды или личных вещей.
Каковы осложнения инфекционного мононуклеоза?
Осложнения инфекционного мононуклеоза включают:
- Бета-гемолитический стрептококковый фарингит группы А
- Перитонзиллярный абсцесс
- Разрыв селезенки – спортсменам рекомендуется избегать занятий спортом в первые три недели болезни
- Хроническая активная инфекция ВЭБ – повторяющиеся или постоянные симптомы, напоминающие инфекционный мононуклеоз, наблюдаемые преимущественно у азиатских детей.Могут возникнуть опасные для жизни осложнения.
Каков прогноз инфекционного мононуклеоза?
Выздоровление после острой фазы начальной EBV-инфекции у здоровых и иммунокомпетентных людей обычно занимает несколько недель, но может потребоваться несколько месяцев, чтобы снова почувствовать себя полностью здоровым. Продолжительная вялость, усталость и боль в суставах – обычное явление, часто продолжающееся 6 месяцев и более.
EBV вызывает пожизненную инфекцию, поскольку вирус остается в спящем состоянии в B-лимфоцитах.Неповрежденный иммунный ответ предотвращает прогрессирование заболевания, вызванного ВЭБ. Однако подавление иммунитета или другое заболевание может реактивировать вирус, вызывая расплывчатые и субклинические симптомы и, в редких случаях, агрессивное заболевание. На этом этапе вирус может передаваться другим людям.
Какие еще болезни может вызывать вирус Эпштейна-Барра?
Другие кожные проявления EBV-инфекции включают:
Другие болезни, связанные с EBV, включают:
Эпидемиология инфекционного мононуклеоза в Северной Шотландии: снижение заболеваемости и зимний пик | BMC Infectious Diseases
Лузуриага К., Салливан Дж. Л.: Инфекционный мононуклеоз. N Engl J Med. 2010, 362: 1993-2000. 10.1056 / NEJMcp1001116.
CAS Статья PubMed Google Scholar
Хак Т., Илиаду П., Хоссейн А., Кроуфорд Д.Х.: Сероэпидемиологическое исследование инфекции вируса Эпштейна-Барра в Бангладеш. J Med Virol. 1996, 48: 17-21. 10.1002 / (SICI) 1096-9071 (199601) 48: 1 <17 :: AID-JMV3> 3.0.CO; 2-O.
CAS Статья PubMed Google Scholar
Crowcroft NS, Vyse A, Brown DW, Strachan DP: Эпидемиология вирусной инфекции Эпштейна-Барра у детей до подросткового возраста: применение нового метода исследования слюны в Эдинбурге, Шотландия. J Epidemiol Community Health. 1998, 52: 101-104. 10.1136 / jech.52.2.101.
CAS Статья PubMed PubMed Central Google Scholar
Хиггинс CD, Swerdlow AJ, Macsween KF, Harrison N, Williams H, McAulay R, Thomas R, Reid S, Conacher M, Britton K, Crawford DH: исследование факторов риска для приобретения Эпштейна-Барра вирус и его подтипы.J Infect Dis. 2007, 195: 474-482. 10.1086 / 510854.
Артикул PubMed Google Scholar
Crawford DH, Macsween KF, Higgins CD, Thomas R, McAulay K, Harrison N, Reid S, Conacher M, Douglas J, Swerdlow AJ: когортное исследование среди студентов университета: Определение факторов риска для Эпштейна- Сероконверсия вируса Барра и инфекционный мононуклеоз. Clin Infect Dis. 2006, 43: 276-282. 10.1086 / 505400.
Артикул PubMed Google Scholar
Hislop AD, Taylor GS, Sauce D, Rickinson AB: Клеточные реакции на вирусную инфекцию у людей: уроки вируса Эпштейна-Барра. Энн Рев Иммунол. 2007, 25: 587-617. 10.1146 / annurev.immunol.25.022106.141553.
CAS Статья Google Scholar
Hadinoto V, Shapiro M, Greenough TC, Sullivan JL, Luzuriaga K, Thorley-Lawson DA: О динамике острой EBV-инфекции и патогенезе инфекционного мононуклеоза. Кровь.2008, 111: 1420-1427.
CAS Статья PubMed PubMed Central Google Scholar
Резк С.А., Вайс Л.М.: Лимфопролиферативные нарушения, связанные с вирусом Эпштейна-Барра. Hum Pathol. 2007, 38: 1293-1304. 10.1016 / j.humpath.2007.05.020.
CAS Статья PubMed Google Scholar
Natelson BH, Ye N, Moul DE, Jenkins FJ, Oren DA, Tapp WN, Cheng Y: Высокие титры ДНК-полимеразы вируса Эпштейна-Барра обнаружены у пациентов с тяжелым утомительным заболеванием.J Med Virol. 1994, 42: 42-46. 10.1002 / jmv.18
109.CAS Статья PubMed Google Scholar
Ascherio A, Munger KL: Факторы экологического риска рассеянного склероза. Часть I: роль инфекции. Энн Нейрол. 2007, 61: 288-299. 10.1002 / ana.21117.
Артикул PubMed Google Scholar
Альмохмид Ю.Х., Авенелл А., Окотт Л., Викерс М.А.: Систематический обзор и метаанализ сероэпидемиологической связи между вирусом Эпштейна-Барра и рассеянным склерозом.PLoS One. 2013, 8 (4): e61110-10.1371 / journal.pone.0061110. DOI: 10.1371 / journal.pone.0061110
CAS Статья PubMed PubMed Central Google Scholar
Хэнлон П., Авенелл А., Окотт Л., Викерс М.А.: Систематический обзор и метаанализ сероэпидемиологической связи между вирусом Эпштейна-Барра и системной красной волчанкой. Arthritis Res Ther. 2014, 16: R3-10.1186 / ar4429.
Артикул PubMed PubMed Central Google Scholar
McAulay KA, Higgins CD, Macsween KF, Lake A, Jarrett RF, Robertson FL, Crawford DH: Полиморфизмы HLA класса I связаны с развитием инфекционного мононуклеоза при первичной инфекции EBV. J Clin Invest. 2007, 117: 3042-3048. 10.1172 / JCI32377.
CAS Статья PubMed PubMed Central Google Scholar
Валлийский Р.М., Че Дж. У., Брем М.А., Селин Л.К .: Гетерологический иммунитет между вирусами. Immunol Rev.2010, 235: 244-266.
CAS Статья PubMed PubMed Central Google Scholar
Huynh GT, Adler FR: Математическое моделирование возрастной зависимости инфекционного мононуклеоза, связанного с вирусом Эпштейна-Барра. Math Med Biol. 2012, 29: 245-261. 10.1093 / imammb / dqr007.
Артикул PubMed Google Scholar
Asher M, Montefort S, Bjorksten B, Lai CKW, Strachan DP, Weiland SK, Williams H, The ISAAC Phase Three Study Group: Мировые временные тенденции в распространенности симптомов астмы, аллергического риноконъюнктивита, и экзема в детстве: повторные кросс-секционные исследования ISAAC, фазы 1 и 3, в нескольких странах.Ланцет. 2006, 368: 733-743. 10.1016 / S0140-6736 (06) 69283-0.
Артикул PubMed Google Scholar
Jacobson LD, Gange SJ, Rose NR, Graham NMH: Эпидемиология и расчетное бремя отдельных аутоиммунных заболеваний среди населения в Соединенных Штатах. Clin Immunol Immunopathol. 1997, 84: 223-243. 10.1006 / Clin.1997.4412.
CAS Статья PubMed Google Scholar
Фисман Д.Н.: Сезонность инфекционных болезней. Annu Rev Public Health. 2007, 28: 127-143. 10.1146 / annurev.publhealth.28.021406.144128.
Артикул PubMed Google Scholar
Staples J, Ponsonby A, Lim L: Низкое воздействие ультрафиолета на мать во время беременности, месяца рождения и риска рассеянного склероза у потомства: продольный анализ. BMJ. 2010, 340: c1640-
PubMed PubMed Central Google Scholar
Disanto G, Chaplin G, Morahan JM, Giovannoni G, Hypponen E, Ebers GC, Ramagopalan SV: месяц рождения, витамин D и риск аутоиммунного опосредованного заболевания: исследование случай-контроль. BMC Med. 2012, 10: 69-10.1186 / 1741-7015-10-69.
CAS Статья PubMed PubMed Central Google Scholar
Альберт П.Л., Проал А.Д., Маршалл Т.Г.: Витамин D: альтернативная гипотеза. Autoimmun Rev.2009, 8: 639-644. 10.1016 / j.autrev.2009.02.011.
CAS Статья PubMed Google Scholar
Ureta G, Osorio F, Morales J, Rosemblatt M, Bono MR, Fierro JA: Создание дендритных клеток с регулирующими свойствами. Transplant Proc. 2007, 39: 633-637. 10.1016 / j.transproceed.2006.12.032.
CAS Статья PubMed Google Scholar
Каннелл Дж. Дж., Вьет Р., Умхау Дж. К., Холик М. Ф., Грант У. Б., Мадронич С., Гарланд С. Ф., Джованнуччи Е: Эпидемический грипп и витамин D.Epidemiol Infect. 2006, 134: 1129-1140. 10.1017 / S0950268806007175.
CAS Статья PubMed PubMed Central Google Scholar
Холмой Т: статус витамина D модулирует иммунный ответ на вирус Эпштейна-Барра: синергетический эффект факторов риска при рассеянном склерозе. Мед-гипотезы. 2008, 70: 66-69. 10.1016 / j.mehy.2007.04.030.
Артикул PubMed Google Scholar
Дэвидсон Р.Дж.: Исследование инфекционного мононуклеоза в Северо-Восточном региональном районе Совета больниц Шотландии, 1960–1999 гг. J Hyg. 1970, 68: 393-400. 10.1017 / S0022172400042297.
CAS Статья PubMed PubMed Central Google Scholar
Tilton RC, Dias F, Ryan RW: Сравнительная оценка трех коммерческих тестов для обнаружения гетерофильных антител у пациентов с инфекционным мононуклеозом. J Clin Microbiol.1988, 26: 275-278.
CAS PubMed PubMed Central Google Scholar
Отдел информационных услуг Шотландии. http://www.isdscotlandarchive.scot.nhs.uk/isd/3793.html,
Результаты переписи населения Шотландии в Интернете. http://www.scotlandscensus.gov.uk/documents/censusresults/release2a/StatsBulletin2A.pdf,
Главное управление регистрации в Шотландии. http: //www.gro-scotland.gov.uk/statistics/theme/population/estimates/mid-year/,
Роджер Дж. Х .: Тест значимости циклических тенденций в данных о заболеваемости. Биометрика. 1977, 64: 152-155. 10.1093 / биомет / 64.1.152.
Артикул Google Scholar
Эдвардс Дж. Х .: Признание циклических тенденций. Энн Хам Жене. 1961, 25: 83-85. 10.1111 / j.1469-1809.1961.tb01501.x.
CAS Статья PubMed Google Scholar
Моррис MC, Эдмундс WJ: Изменяющаяся эпидемиология инфекционного мононуклеоза ?. J Infect. 2002, 45: 107-109. 10.1053 / jinf.2002.1022.
CAS Статья PubMed Google Scholar
Таттевин П., Ле Тулсо И., Минжоль С., Человек А, Чапплен Дж. М., Арвье С., Томас Р., Мишле С. Рост заболеваемости тяжелым инфекционным мононуклеозом, связанным с вирусом Эпштейна-Барра: надзорное исследование. J Clin Microbiol. 2006, 44: 1873-1874.10.1128 / JCM.44.5.1873-1874.2006.
Артикул PubMed PubMed Central Google Scholar
Cheng C, Chang L, Shao P, Lee P, Chen J, Lu C, Lee C, Huang L: Клинические проявления и количественный анализ вирусной нагрузки у тайваньских детей с инфекционным мононуклеозом, связанным с вирусом Эпштейна-Барра . J Microbiol Immunol Infect. 2007, 40: 216-221.
PubMed Google Scholar
Wan K, Yu Y, Wu W: Первичная инфекция вирусом Эпштейна-Барра у 2-летних детей: отчет о 3 случаях. Turk J Pediatr. 2010, 52: 655-658.
PubMed Google Scholar
Хоуп-Симпсон RE: Передача эпидемического гриппа. J Hygiene. 1981, 86: 35-47. 10.1017 / S0022172400068728.
CAS Статья Google Scholar
Newell KW: Зарегистрированная заболеваемость железистой лихорадкой.Анализ отчета службы Лаборатории общественного здравоохранения. J Clin Pathol. 1957, 10: 20-22. 10.1136 / jcp.10.1.20.
CAS Статья PubMed PubMed Central Google Scholar
Henke CE, Kurland LT, Elveback LR: Инфекционный мононуклеоз в Рочестере, Миннесота, с 1950 по 1969 год. Am J Epidemiol. 1973, 98: 483-490.
CAS PubMed Google Scholar
Бродский А.Л., Хит К.В.: Инфекционный мононуклеоз: эпидемиологические закономерности в колледжах и университетах США. Am J Epidemiol. 1972, 96: 87-93.
CAS PubMed Google Scholar
Heath CW, Бродский А.Л., Потольский А.И.: Инфекционный мононуклеоз в общей популяции. Am J Epidemiol. 1972, 95: 46-52.
PubMed Google Scholar
Leard SE: Сезонная заболеваемость инфекционным мононуклеозом.J AM Coll Health Assoc. 1972, 21: 169-
CAS PubMed Google Scholar
Чанг Р.С., Розен Л., Капикян А.З.: Инфекции вируса Эпштейна-Барра в питомнике. Am J Epidemiol. 1981, 113: 22-29.
CAS PubMed Google Scholar
Грот I, Мимуни Д., Уэрта М., Мимуни М., Коэн Д., Робин Дж., Питлик С., Грин М.С.: Клинические и лабораторные проявления инфекционного мононуклеоза с положительным результатом ВЭБ у молодых людей.Epidemiol Infect. 2003, 131: 683-689. 10.1017 / S0950268803008550.
CAS Статья PubMed PubMed Central Google Scholar
Crawford DH, Swerdlow AJ, Higgins CD, McAulay R, Harrison N, Williams H, Britton K, Macsween KF: Сексуальный анамнез и инфекция вируса Эпштейна-Барра. J Infect Dis. 2002, 186: 731-736. 10.1086 / 342596.
Артикул PubMed Google Scholar
Общее обследование домашних хозяйств. http://www.ons.gov.uk/ons/rel/ghs/general-household-survey/2002-edition/index.html,
Andiman WA, Miller G: Ответ антител на Эпштейн-Барр Вирус. Man Clin Imm. Под редакцией: Роуз Н.Р., Фридман Х. 1980, Вашингтон, округ Колумбия: Американское общество микробиологии, 628-633. 2
Google Scholar
Синдром Джанотти Крости – NORD (Национальная организация по редким заболеваниям)
УЧЕБНИКИ
Учебник Нельсона по педиатрии, 15-е изд.: Ричард Э. Берман, редактор; W.B. Saunders Company, 1996. P. 1868.
СТАТЬИ В ЖУРНАЛЕ
Синдром Джанотти-Крости. D. Rubenstein et al .; Педиатрия (март 1978 г .; 61 (3)). Стр. 433-37.
Синдром Джанотти-Крости. Обзор десяти случаев, не связанных с гепатитом B. К.Л. Spear et al .; Arch Dermatol (июль 1984; 120 (7)). Стр. 891-96.
Синдром Джанотти-Крости: исследование 26 случаев. A. Taieb et al .; Br J Dermatol (июль 1986; 115, (1)). Стр. 49-59.
Эпидемия детского папулезного акродерматита (синдром Джанотти-Крости), вызванная вирусом Эпштейна-Барра.У. Балдари и др .; Дерматология (1994; 188 (3)). Стр. 203-04.
Синдром Джанотти-Крости при вирусной инфекции Эпштейна-Барра. R.E. Шопф; Hautarzt (октябрь 1995 г .; 46 (10)). Стр. 714-16.
Отчет о клиническом случае: синдром Джанотти-Крости, связанный с инфекцией вируса герпеса-6 человека. С. Ясумото и др .; J. Dermatol (июль 1996 г .; 23 (7)). Стр. 499-501.
Синдром Джанотти-Крости, вызванный смешанной инфекцией, продуцируемой вирусом эпидемического паротита и вирусом парагриппа типа 2. R. Hergueta Lendinez et al.; An Esp Pediatr (январь 1996; 44 (1)). Стр. 65-66.
Синдром Джанотти-Крости, связанный с инфекцией вируса Эпштейна-Барра. B. Hofmann et al .; Pediatr Dermatol (июль-август 1997 г .; 14 (4)). Стр. 273-77.
Папулезный акродерматит детского возраста, связанный с инфекцией поксвируса и парвовируса B19. J.M. Carrascosa et al .; Кутис (май 1998 г .; 61 (5)). Стр. 265-67.
Синдром Джанотти-Крости: клинические, серологические и терапевтические данные от девяти детей. K. Boeck et al .; Кутис (декабрь 1998 г .; 62 (6)).Стр. 271-74. Тест: стр. 286.
Синдром Джанотти-Крости, связанный с ротавирусной инфекцией (письмо). В. Ди Лерния; Pediatr Dermatol (ноябрь-декабрь 1998 г .; 15 (6)). Стр. 485-86.
ИЗ ИНТЕРНЕТА
Синдром eMedicine-Gianotti-Crosti: статья Кара Н Шах, доктор медицинских наук
hhtp: //www.emedicine.com/derm/topic165.htm
Frontiers | Т-клеточное лимфопролиферативное заболевание, связанное с вирусом Эпштейна-Барра, проявляющееся в виде хронической диареи и кишечного кровотечения: отчет о болезни
Введение
Вирус Эпштейна-Барра (EBV), повсеместно распространенный ДНК-вирус, принадлежит к подсемейству γ герпесвирусов.Подсчитано, что почти 95% взрослых инфицированы ВЭБ. Большинство случаев инфицирования ВЭБ происходит в раннем детстве и в большинстве случаев протекает бессимптомно. Однако сообщается, что инфекции у подростков или молодых людей приводят к инфекционному мононуклеозу (ИМ), у пациентов часто наблюдается лихорадка, фарингит, лимфаденопатия и спленомегалия (1, 2). Начало IM включает временную пролиферацию EBV-инфицированных B-клеток в дополнение к чрезмерному ответу цитотоксических T-клеток (CTL), которые являются EBV-специфичными (3).У большинства пациентов эти IM-симптомы проходят без последствий. Однако у редких пациентов, даже без явного иммунодефицита, заболевание проявляется в хронической EBV-инфекции, которая характеризуется стойкими IM-подобными симптомами, называемыми «хронической активной EBV-болезнью (CAEBV)». Это состояние включено в классификацию лимфом Всемирной организации здравоохранения (ВОЗ) 2008 года как системный ВЭБ + Т-клеточный LPD у детей. Пациенты имеют характерно высокую нагрузку EBV-ДНК в периферической крови и системную клональную экспансию EBV-инфицированных Т-клеток или естественных киллеров (NK) клеток (3, 4).
Сообщения о ASEBV + T-LPD являются спорадическими и редкими (5), а желудочно-кишечные симптомы ASEBV (+) T-LPD еще реже. Эти симптомы часто ошибочно принимают за туберкулез и воспалительные заболевания кишечника. Здесь мы сообщаем о случае иммунокомпетентного взрослого пациента, который предъявил первичную жалобу на хроническую диарею, боль в животе и небольшую гематохезию, но в конечном итоге у него был диагностирован ВЭБ-ассоциированный Т-клеточный LPD (II: пограничный). Цель этого отчета и нашего анализа – способствовать распознаванию поражений кишечника при ASEBV + T-LPD.
Согласие
Пациент дал согласие на участие в исследовании и предоставил письменное согласие на публикацию этого описания случая.
Презентация кейса
Ранее здоровая 43-летняя женщина, проживающая на пастбищах, без личного или семейного анамнеза иммунодефицита, поступила с перемежающейся лихорадкой в течение 2 месяцев, которая иногда сопровождалась ознобом, болями в животе, диареей и гематохезией.
Начальная презентация
Женщина сначала обратилась в местную больницу, где у нее диагностировали воспалительное заболевание кишечника и лечили клиндамицином, что привело к некоторому клиническому улучшению.Когда ее предыдущие симптомы ухудшились в течение 10 дней, ее осмотрели в гастроэнтерологическом отделении нашей больницы. На рентгенограмме брюшной полости пациентки в амбулаторном отделении выявлены признаки «неполной кишечной непроходимости», и она была госпитализирована для дальнейшего обследования. Ее физическое обследование не отличалось от других, за исключением низкого кровяного давления (97/71 мм рт. Ст.) И бледности. При первоначальном обращении не было зарегистрированной потери веса / аппетита или других значимых клинических проявлений. Лабораторные тесты на этой первоначальной презентации сведены в Таблицу 1.
Таблица 1 . Лабораторные результаты пациента при первичном обращении.
Лечение
Пациент изначально лечился противоинфекционной и симптоматической терапией. Усовершенствованная компьютерная томография, проведенная на 2-й день в больнице, показала диффузные изменения восходящей, поперечной и нисходящей ободочной кишки, имитирующие язвенный колит. Были видны множественные лимфатические узлы брыжеечной и задней брюшины (рис. 1). Было предложено экстренное обследование с помощью колоноскопии, которое выявило множественные дискретные язвы с неровными границами и чистым основанием, разбросанные по толстой кишке.Диаметр язв варьировал от 6 до 30 мм, вокруг эрозии виднелись эрозии. Нормальная слизистая оболочка также была отчетливо видна среди язв (рис. 2).
Рисунок 1 . Расширенная КТ брюшной полости: диффузное утолщение слизистой оболочки восходящей, поперечной и нисходящей ободочной кишки с грубыми краями, неравномерное усиление в фазе артерии (красная стрелка) (A) . Изображение венозной фазы (красная стрелка) (B) . Множественные лимфатические узлы можно было увидеть в мезентериальной и задней областях брюшины.
Рисунок 2 . Проявление предоперационной колоноскопии: изъязвление с четким краем и основанием на конце подвздошной кишки (A) . Предоперационная колоноскопия выявила множественные дискретные язвы, видимые в разных сегментах толстой кишки (B – E) и прямой кишки (F) .
Специфическая клоноскопическая картина убедительно свидетельствует о воспалительном заболевании, включая язвенный колит (ЯК) и болезнь Крона (БК). Специфическое инфекционное заболевание кишечника, особенно туберкулез кишечника, также подозревалось из-за стойкой лихорадки, и диагноз лимфомы кишечника также не мог быть исключен.Были проведены дополнительные лабораторные исследования, включая комбинацию хронической воспалительной энтеропатии, антиядерных антител (ANA), цитоплазматических антител против нейтрофилов (ANCA), факторов, связанных с ревматизмом (ASO + RF + CRP), онкомаркеров пищеварительного тракта, прокальцитонина (PCT). , посев крови, посев кала, обнаружение амебного трофозоита, цитомегаловирус (CMV), антитела против EBV, пятнистый эксперимент с Т-клетками и тест PPD на Mycobacterium tuberculosis , реакция Видаля, антитела против Brucella, индикаторы вируса гепатита, D-глюкан Fungi обнаружение и др.Результаты всех этих тестов были либо отрицательными, либо ничем не примечательными, за исключением высоких титров антител, связанных с EBV: вирусный капсидный антиген против EBV (VCA) -IgG: (4,157 с / со), анти-EBV VCA-IgM (0,391 с. / co), IgG к ядерному антигену Барра Эпштейна (EBNA) (0,865 s / co), EBEA IgG (1,933 s / co) и IgM к раннему антигену Эпштейна-Барра (EBEA) (0,187 s / co).
Во время госпитализации у пациента не было признаков ремиссии. На 10-й день цветная допплерография брюшной полости показала спленомегалию. Через 14 дней после поступления у пациента развилось сильное кишечное кровотечение, ему была выполнена экстренная тотальная колэктомия, терминальная эктомия подвздошной кишки, анастомоз тонкой и прямой кишки и профилактическая илеостомия.Она была выписана после стабильного состояния и лечилась месалазином от язвенного колита (ЯК) на основании патологического диагноза, поставленного нашей больницей после операции. Месалазин был отменен после нескольких курсов.
Госпиталь Дружбы Пекина, входящий в состав больницыСтоличного медицинского университета, после гистологического исследования резецированной ткани поставил гистологический диагноз Т-клеточного LPD ВЭБ (II: пограничный). Микроскопическое исследование слайдов резецированной толстой кишки выявило изъязвление слизистой оболочки кишечника и интерстициальный отек кишечника, который сопровождался диффузной инфильтрацией плеоморфных мягких атипичных лимфоидных клеток малого и среднего размера в слизистой и подслизистой оболочке смесью плазматических клеток и эозинофильных гранулоцитов и тканей. клетки.Некоторые лимфоидные клетки имели большое ядро и более явные ядрышки. Лимфоидные клетки были распределены в мышечном слое и серозной оболочке (рис. 3). Мы подтвердили диагноз EBV-ассоциированного Т-клеточного LPD на основании результатов иммуногистохимии (IHC) и in situ гибридизации кодируемой EBV миРНК (EBER). ИГХ выявил, что легкие атипичные лимфоидные клетки были положительными по экспрессии (фиг. 4B) CD3, (фиг. 4A) CD2, (фиг. 4E) CD7 и (фиг. 4C) экспрессии CD4. Кроме того, несколько атипичных клеток также оказались положительными по CD8 (фиг. 4F), (фиг. 4H) GranzymeB (фиг. 4J) TIAI, TCRGβ и TCRγδ.Лимфоидные клетки были отрицательными по CD56. (Рисунок 4I) Положительность Ki-67 составляла 40-50%. Гибридизация in situ для EBER (фигура 4K) продемонстрировала EBV-положительные атипичные лимфоидные клетки 50 / HPF.
Рисунок 3 . Слайды резецированной толстой кишки показали изъязвление слизистой оболочки кишечника и интерстициальный отек кишечника (A – D) наряду с диффузной инфильтрацией плеоморфных легких атипичных лимфоидных клеток малого и среднего размера в слизистой и подслизистой оболочке смесью плазматических клеток и эозинофильных гранулоцитов. и клетки ткани (C, D) .Некоторые лимфоидные клетки имели большое ядро и явные ядрышки (D) . Лимфоидные клетки были распределены в мышечном слое и серозной оболочке (A, B) .
Рисунок 4. (A) Иммуногистохимия выявила большое количество атипичных лимфоидных клеток, экспрессирующих CD2 ( A : 20X10), CD3 ( B : 20X10), CD4 ( C : 20X10) и CD7 ( E : 20X10). CD5 ( D : 20X10) -положительных клеток было меньше, чем CD3-положительных клеток; CD8 ( F : 20X10) -положительные клетки были меньше, чем CD4-положительные клетки, а CD20 ( G : 20X10) -положительные клетки имели очаговое распределение.Гранзим B ( H : 20 × 10) -положительные клетки были разбросаны. Отмечена частичная положительная реакция на TIAI ( J : 20X10), TCRGβ и TCRγδ. Клетки были отрицательными по CD56 и Ki-67 ( I : 20X10) – положительность составляла 40-50%. (B) EBV in situ гибридизация с кодируемой EBV ми-РНК (EBER) продемонстрировала EBV-положительные (50 / HPF) атипичные лимфоидные клетки ( K : 20X10).
Последующие посещения
Больному рекомендовано ежемесячно возвращаться в больницу на повторное обследование.Во время этих посещений у нее каждый раз были признаки рецидива, включая новые язвы стомы и кровавый стул. Тест на вирусную нагрузку EB был проведен во время ее первого контрольного визита, и было обнаружено, что ДНК EBV составляет 2,55 × 10 6 копий / мл для. Послеоперационная колоноскопия, выполненная при первом рецидиве, выявила множественные афтозные кровоточащие язвы, разбросанные от стомы до примерно 40 см от тонкой кишки, в дополнение к послеоперационному анастомозиту толстой кишки (рис. 5). Гистологическое исследование образцов биопсии подтвердило патологический диагноз EBV-T-клеточной LPD.Лечение преднизолоном 10 мг ежедневно было начато внутривенно в течение нескольких дней в больнице. После этого был назначен пероральный преднизолон в дозе 40 мг / день, после чего дозу постепенно снижали. Пациент показал значительное клиническое улучшение. Гематохезия временно контролировалась до тех пор, пока дозировка преднизолона не была снижена до 25 мг, а EBV-ДНК не снизилась до 1,31 × 10 6 копий / мл. Более того, на этот раз при колоноскопии ничего примечательного не наблюдалось (рис. 6). Настоятельно рекомендовалось провести аспирацию костного мозга, но она не была проведена из-за отказа семьи.
Рисунок 5 . Множественные афтозные кровоточащие язвы, рассыпанные от стомы на расстоянии 40 см от тонкой кишки (черная стрелка) (A) ; Послеоперационный анастомозит толстой кишки (B) .
Рисунок 6 . Язвы или новообразования при эндоскопии не обнаружены. Послеоперационные изменения тонкой кишки (А, Б) .
Последний раз пациентка возвращалась в наше отделение для повторного обследования через 4 месяца после первого обращения.Во время этого последнего визита была выполнена аспирация костного мозга, которая оказалась нормальной. Однако функциональные пробы печени оказались ненормальными (АЛТ 100 МЕ / л и AST 43 МЕ / л). ДНК EBV составляла 1 × 10 6 копий / мл. Пациент был направлен в онкологическое отделение нашей больницы для обследования. Ее попросили продолжить прием преднизолона и противовирусных препаратов до тех пор, пока у нее не появится стойкая лихорадка и гематохезия, и она умерла через 3 месяца.
Обсуждение
EBV, как известно, инфицирует В-клетки.Он также может инфицировать Т-клетки и NK-клетки. ДПЛ, ассоциированная с EBV, составляет большую группу заболеваний, которые характеризуются чрезмерной лимфоидной пролиферацией (2, 3, 6, 7). В последние годы увеличилось количество взрослых пациентов, у которых развивается системный ВЭБ + Т-клеточный ДПД без иммунодефицита. Случаи заболевания у взрослых редки, но болезнь быстро прогрессирует. По этой теме доступно лишь небольшое количество отчетов (3), что подчеркивает проблемы, с которыми сталкиваются врачи, оказывающие помощь таким пациентам.Без сомнения, необходимы дальнейшие исследования T-LPD ВЭБ во взрослом возрасте, чтобы проиллюстрировать дифференциальный диагноз, особенно уникальные клинические проявления, которые необходимы для лучшего понимания прогрессирования заболевания и лучшего клинического ведения.
Хотя T-LPD ВЭБ у взрослых носит системный характер, в основном он поражает печень, селезенку и сердце (7, 8). Наиболее частыми клиническими симптомами являются лихорадка, нарушение функции печени, гепатомегалия, спленомегалия, системная лимфаденопатия и тромбоцитопения (2, 3, 9, 10).Согласно обзору литературы, во всем мире зарегистрировано лишь несколько случаев T-LPD ВЭБ у взрослых, проявляющихся преимущественно кишечными симптомами (7, 8, 11). Na et al. (7) сообщили о двух случаях иммунокомпетентных пациентов с EBV-ассоциированной Т-клеточной ДПД тонкой и толстой кишки. Этим двум пациентам изначально был поставлен неверный диагноз: туберкулез кишечника и болезнь Крона (БК). Одним из пациентов был ранее здоровый мужчина 50 лет с общей слабостью, потерей веса, жидким стулом и лихорадкой.Другой пациенткой была 49-летняя женщина с рецидивирующей гематохезией. Оба пациента были подвергнуты экстренной резекции тонкой кишки из-за перфорации кишечника, и после гистологического исследования образцов биопсии им был поставлен точный диагноз EBV-ассоциированного Т-клеточного LPD. Абдул-Гафар и др. (8) сообщили об одном случае фульминантного EBV-ассоциированного Т-клеточного LPD у иммунокомпетентного мужчины среднего возраста, у которого была хроническая диарея и желудочно-кишечное кровотечение. Колоноскопия этого пациента выявила множественные неглубокие язвы различного размера и неправильной формы от прямой кишки до илеоцекального клапана.Первоначально ему поставили неправильный диагноз: инфекционный колит и язвенный колит. Однако повторное обследование с помощью колоноскопии, наряду с гистологическим исследованием образцов биопсии, помогло поставить точный диагноз EBV-ассоциированного Т-клеточного LPD. Пациент был подвергнут тотальной колэктомии из-за неконтролируемой гематохезии и умер от диссеминированного внутрисосудистого свертывания крови (ДВС). Другой случай, описанный Sazuka et al. (11), это была женщина 71 года, поступившая с 3-месячным анамнезом тяжелой диареи, похудания и гипоальбуминемии.Капсульная эндоскопия, проведенная этой пациентке, выявила сплющенные ворсинки по всему тонкому кишечнику. Кроме того, двухбаллонная энтероскопия подтвердила диффузно атрофированные ворсинки тонкого кишечника и четко видимые пейеровы пятна. Окрашивание слизистой оболочки тонкого кишечника гематоксилином и эозином свидетельствует о глютеновой болезни из-за наличия атрофических ворсинчатых структур. Пациент был переведен на безглютеновую диету на 1 месяц, но симптомы не уменьшились. Дальнейшие тесты, такие как серологический тест на EBV, EBV-ДНК, Саузерн-блот-анализ EBV-инфицированных клеток, сортировка клеток с активацией флуоресценции (FACS) и гибридизация кодируемой EBV РНК in situ , помогли поставить окончательный диагноз EBV-ассоциированного T -ячейка LPD.Несмотря на последовательное лечение циклоспорином и CHOP, пациент умер через 5 месяцев. Наконец, Zheng et al. (12) сообщили об одном случае иммунокомпетентного пациента с EBV-ассоциированным Т-клеточным LPD толстой кишки. У этого 26-летнего пациента мужского пола изначально был ошибочный диагноз язвенного колита (ЯК). Пациент обратился с жалобами на диарею и гематохезию и сообщил о перемежающейся высокой температуре в течение более 3 месяцев. Пациенту был поставлен диагноз ВЭБ + Т-клеточный LPD (степень II: пограничные поражения) на основании результатов морфологических определений, IHC, ISH для перестройки генов EBER и TCR.Этому пациенту была выполнена правая гемиколэктомия из-за активного кровотечения из язв толстой кишки, но пациент умер через 2 месяца после постановки диагноза ВЭБ + Т-клеточный LPD.
Имеются ограниченные знания о поражениях кишечника при системном T-LPD ВЭБ у взрослых. Сообщалось, что у некоторых пациентов наблюдались легкие симптомы, такие как хроническая диарея, в то время как у других было быстрое клиническое течение с такими осложнениями, как перфорация кишечника и тяжелое желудочно-кишечное кровотечение, приводившее к смерти пациента в течение периода времени от нескольких дней до нескольких месяцев после болезни. диагноз.Очевидно, что ранняя диагностика и соответствующее лечение имеют решающее значение. Во время колоноскопии часто можно увидеть множественные язвы с окружающей отечной и эритематозной слизистой оболочкой. Могут быть вовлечены как тонкая, так и толстая кишка, и сообщается об изменении формы, глубины и размера язвы. Гистологический анализ изъязвленной слизистой может выявить степень пролиферации различных лимфоцитов в дополнение к идентификации клеток как нормальных или атипичных. Как обсуждалось выше, это заболевание может быть легко ошибочно диагностировано как туберкулез кишечника (ITB) и воспалительные заболевания кишечника (IBD) из-за атипичных проявлений колоноскопии и клинических особенностей, особенно когда биопсия ткани недостаточна и в образцы.У пациентов с ТБ и ВЗК часто наблюдаются такие симптомы, как лихорадка, лимфаденопатия, диарея и анемия, что затрудняет дифференциальный диагноз.
Несмотря на сходные очаги при колоноскопии, имеются некоторые специфические клинические проявления, эндоскопические и патологические данные ТБ или ВЗК, соответственно. Колоноскопия туберкулеза обычно выявляет поперечные язвы, мелкие и неровные, с поражением илеоцекальной области. Кроме того, типичными патологическими признаками являются казеозные гранулемы и кислотостойкость.Надежный диагноз ITB может быть основан на сочетании симптомов и тестов, таких как ночная потливость, сопутствующий туберкулез легких, положительный туберкулиновый кожный тест, положительный результат на антитела к туберкулезу и абдоминальная лимфаденопатия и асцит. Хотя отдельные язвы в представленном здесь случае имитировали поражения, обнаруженные при БК, ее эндоскопические особенности отличались от таковых у язв БК, в первую очередь потому, что продольные язвы, имеющие вид булыжника или продольно расположенные афтозные язвы, не были видны.Некаеозные гранулемы специфичны для CD. Гематохезия, кишечная непроходимость, свищ и т. Д. – частые осложнения у пациентов с БК (13). Положительный диагноз ЯК ставится на основании симптомов и эндоскопических доказательств непрерывного воспаления слизистой оболочки толстой кишки со свежей кровью и нагноением на ней, которое почти всегда начинается в прямой кишке и распространяется проксимально. Образцы биопсии оцениваются как средство для дальнейшего подтверждения диагноза и не должны заменять сам диагноз.Эти образцы помогают установить хронический активный колит. Говоря гистологически, заболевание ограничивается слоями слизистой оболочки с различной степенью инфильтратов из лимфоцитов, плазматических клеток и гранулоцитов. Другие гистологические находки включают искажение архитектуры крипт с укорочением и беспорядком крипт, атрофию крипт, абсцессы крипт и ветвление крипт (14). Иногда диагноз ВЗК может быть легко поставлен, но классификационный диагноз ВЗК трудно подтвердить, потому что два основных типа, язвенный колит (ЯК) и болезнь Крона (БК), имеют схожие симптомы и неотличимы друг от друга.Неопределенный колит (IC) и неклассифицированное воспалительное заболевание кишечника (IBDU) – это болезненные состояния, часто диагностируемые у таких трудно диагностируемых пациентов (15).
Кишечный EBV-T-LPD, ограниченный тонкой кишкой, встречается крайне редко, и в литературе описан только один случай (11). Изменения в кишечнике – это не язвенная слизистая оболочка, а диффузно атрофированные ворсинки тонкой кишки и четко видимые пейеровы бляшки, как было выявлено двойной эндоскопией, что предположительно указывает на глютеновую болезнь.Целиакия – одна из наиболее частых причин хронической мальабсорбции. Нарушение усвоения адекватных калорий приводит к потере веса, а такое нарушение всасывания приводит к боли в животе и вздутию живота (16). Таким образом, лечение безглютеновой диетой может помочь дифференцировать глютеновую болезнь от EBV-T-LPD тонкого кишечника, поскольку только пациенты с глютеновой болезнью демонстрируют значительное облегчение симптомов.
Гистопатологические тесты играют решающую роль в постановке точного диагноза EBV-T + LPD.Они помогают определить различные степени пролиферации Т-лимфоцитов в дополнение к обнаружению атипичных клеток. Это важно, потому что у пациентов с ВЗК нет атипичных лимфоцитов (17). Ohshima et al. (9) сообщили об исследовании, в котором оценивали 108 случаев EBV-T / NK-LPD. Сообщалось, что все случаи были положительными на цитотоксические молекулы, что указывало на их происхождение из цитотоксических Т-клеток. Анализ IHC нашего пациента показал, что несколько атипичных клеток были положительными по CD8, GranzymeB, TIAI, TCRGβ и TCRγδ, что аналогично результатам, описанным в Ohshima et al.изучение. В настоящее время широко распространено мнение, что правильный диагноз EBV-T + LPD достигается путем интеграции гистопатологии, IHC и EBER и анализа клональности в контексте истории болезни и лабораторных данных инфекции EBV (включая профиль антител и нагрузку ДНК EBV в сыворотка) (6).
В настоящее время отсутствует стандартный протокол лечения пациентов с системным EBV-T-LPD. Были протестированы различные методы лечения, включая противовирусные препараты, кортикостероиды, химиотерапию и иммуномодулирующие препараты.Однако успех был очень ограниченным с минимальной ремиссией. Такие терапевтические подходы приводили к полной ремиссии только в редких случаях, и в настоящее время ТГСК является единственной лечебной терапией (2, 3, 6, 18), хотя известно, что ТГСК связана со значительным риском осложнений, связанных с трансплантацией. Пациентам часто бывает трудно дать согласие на ТГСК, особенно если симптомы не очень тяжелые (3). Доклинические испытания двух лекарственных препаратов-кандидатов от этой болезни недавно были опубликованы с некоторыми обнадеживающими результатами.Одним из таких новых препаратов является бортезомиб, известный ингибитор протеасомы 26S. Он может индуцировать апоптоз и экспрессию генов литического цикла EBV BZLF1 и gp350 / 220 в различных линиях клеток Т-клеточной лимфомы человека (19). Другой новый препарат – вальпроевая кислота, широко используемый противоэпилептический препарат и известный ингибитор гистондеацетилаз (HDAC). Iwata et al. (20) сообщили об индукции апоптоза вальпроевой кислотой в Т-клетках человека, инфицированных EBV. Подводя итог, можно сказать, что систематический EBV-T-LPD у взрослых с началом кишечных проявлений в основном имеет скоротечное клиническое течение и быстро прогрессирует.Из-за серьезных осложнений пациенты не имеют большого выбора, и им необходимо перенести операцию. Раннее обнаружение этого заболевания, наряду с правильным диагнозом, может позволить себе столь необходимое время для консервативного и эффективного лечения. Хотя недавно был достигнут некоторый прогресс, срочно необходимы дальнейшие исследования для выявления новых лекарств и стратегий лечения.
Авторские взносы
ЮЛ был лечащим врачом этого пациента и руководил всем процессом написания.MW и WC участвовали во всех сборах и обработке данных. XD отвечал за чтение и интерпретацию патологических изображений. ТТ выполнила колоноскопическое обследование. YW, YaL и XM были основными участниками в организации записей и составлении рукописи. Все авторы вычитали и одобрили рукопись.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Это исследование было поддержано финансированием доклинических исследований новых препаратов, относящихся к целевому рекомбинантному молекулярному слитому белку R9-GRIM-19 для лечения рака желудочно-кишечного тракта (XM).
Список литературы
1. Амели Ф., Гафуриан Ф., Масир Н. Систематическое Т-клеточное лимфопролиферативное заболевание с положительным результатом на вирус Эпштейна-Барра, проявляющееся в виде стойкой лихорадки и кашля: отчет о клиническом случае. J Med Case Rep. (2014) 8: 288. DOI: 10.1186 / 1752-1947-8-288
PubMed Аннотация | CrossRef Полный текст | Google Scholar
2.Коэн Дж. И., Джаффе Е. С., Дейл Дж. К., Питталуга С., Хеслоп Х. Э., Руни С. М. и др. Характеристика и лечение хронической активной болезни, вызванной вирусом Эпштейна-Барра: 28-летний опыт работы в США. Clin Trials Observ. (2011) 117: 5835–49. DOI: 10.1182 / кровь-2010-11-316745
PubMed Аннотация | CrossRef Полный текст | Google Scholar
3. Фудзивара С., Кимура Х., Имадоме К., Араи А., Кодама Е., Морио Т. и др. Текущее исследование хронической активной инфекции вируса Эпштейна-Барра в Японии. Pediatr Int. (2014) 56: 159–66. DOI: 10.1111 / ped.12314
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Пак С., Ким К., Ким В.С., Ю К. Х., Ку Х Х, Ко Й Х и др. Системная ВЭБ + Т-клеточная лимфома у пожилых пациентов: сравнение с детьми и молодыми взрослыми пациентами. Арка Вирхова. (2008) 453: 155–63. DOI: 10.1007 / s00428-008-0640-7
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5. Zheng XD, Zhou XG, Jin Y, Xie JL, Zhong FL, Feng J, Meng QX и др.Клинические особенности и лабораторные данные для взрослых лимфопролиферативных T / NK вирусов Эпштейна-Барра. Чжунго Ши Ян Сюэ Е Сюэ За Чжи (2013) 21: 953–7. DOI: 10.7534 / j.issn.1009-2137.2013.04.027
CrossRef Полный текст | Google Scholar
6. Ван Р-К, Чанг С.-Т, Се Й-К, Хуанг В. Т., Хсу Дж. Д., Ценг С. Е. и др. Спектр лимфопролиферативного Т-клеточного заболевания, связанного с вирусом Эпштейна-Барра, у подростков и молодых людей на Тайване. Int J Clin Exp Pathol. (2014) 7: 2430–7.
PubMed Аннотация | Google Scholar
7. Na HK, Ye BD, Yang SK, Yang DH, Jung KW, Kim KJ, et al. EBV-ассоциированные лимфопролиферативные заболевания, ошибочно диагностированные как болезнь Крона. J Crohns Colitis (2012) 7: 649–52. DOI: 10.1016 / j.crohns.2012.09.018
PubMed Аннотация | CrossRef Полный текст | Google Scholar
8. Абдул-Гафар Дж., Ким Дж. У., Пак К. Х., Чо Мая. Фульминантное Т-клеточное лимфопролиферативное заболевание, связанное с вирусом Эпштейна-Барра, у иммунокомпетентного мужчины среднего возраста с хронической диареей и желудочно-кишечным кровотечением. J Korean Med Sci. (2011) 26: 1103–7. DOI: 10.3346 / jkms.2011.26.8.1103
PubMed Аннотация | CrossRef Полный текст | Google Scholar
9. Охшима К., Кимура Х., Йошино Т., Ким К.В., Ко Й.Х., Ли С.С. и др. Предлагаемая категоризация патологических состояний EBV-ассоциированного T / лимфопролиферативного расстройства (LPD) естественных киллерных клеток у детей и молодых людей: перекрывается с хронической активной EBV-инфекцией и младенческой молниеносной EBV T-LPD. Pathol Int. (2008) 58: 209–217.DOI: 10.1111 / j.1440-1827.2008.02213.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10. Кимура Х., Ито Й., Кавабе С., Гото К., Такахаши Й., Кодзима С. и др. EBV-ассоциированные лимфопролиферативные заболевания T / NK-клеток у хозяев без иммунодефицита: проспективный анализ 108 случаев. Кровь (2012) 119: 673–86. DOI: 10.1182 / кровь-2011-10-381921
PubMed Аннотация | CrossRef Полный текст | Google Scholar
11. Sazuka S, Takahashi Y, Kawaguchi T., Sato T., Nakagawa T., Furuya Y, et al.Эндоскопические данные о лимфопролиферативном заболевании Т-клеток, ассоциированном с вирусом Эпштейна – Барра в тонком кишечнике. Эндоскопия (2012) 44: E30–1. DOI: 10.1055 / с-0030-1257081
PubMed Аннотация | CrossRef Полный текст | Google Scholar
12. Чжэн X, Xie J, Zhou X. Т-клеточное лимфопролиферативное заболевание, связанное с вирусом Эпштейна-Барра, ошибочно диагностированное как язвенный колит: отчет о клиническом случае. Int J Clin Exp Pathol. (2015) 8: 8598–602.
PubMed Аннотация | Google Scholar
13.Yu H, Liu Y, Wang Y, Peng L, Li A, Zhang Y. Клинические, эндоскопические и гистологические различия между болезнью Крона и туберкулезом кишечника. Пищеварение (2012) 85: 202–9. DOI: 10.1159 / 000335431
PubMed Аннотация | CrossRef Полный текст | Google Scholar
15. Нин З., Вэй XC, Шао Х.С., Сюй С-Ф, Ли И-М. Воспалительные заболевания кишечника без классификации. Zhejiang Univ Sci B (2011) 12: 280–6. DOI: 10.1631 / jzus.B1000172
CrossRef Полный текст | Google Scholar
16.Альберто Р.Т., Айвор Д.Х., Сиаран П.К., Колдервуд А.Х., Мюррей Дж. Клинические рекомендации Американского колледжа гастроэнтерологии: диагностика и лечение целиакии. Am J Gastroenterol. (2013) 108: 656–77. DOI: 10.1038 / ajg.2013.79
CrossRef Полный текст | Google Scholar
17. Ли Й.Дж., Ян С.К., Бён Дж.С., Мён С.Дж., Чанг Х.С., Хонг С.С. Анализ результатов колоноскопии при дифференциальной диагностике туберкулеза кишечника и болезни Крона. Эндоскопия (2006) 38: 592–7.DOI: 10,1055 / с-2006-924996
PubMed Аннотация | CrossRef Полный текст | Google Scholar
18. Араи А., Имадоме К., Ватанабэ Ю., Йошимори М., Кояма Т., Кавагути Т. и др. Клинические особенности хронической активной инфекции вируса Эпштейна-Барра у взрослых: ретроспективный анализ. Int J Hematol. (2011) 93: 602–9. DOI: 10.1007 / s12185-011-0831-x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19. Fu DX, Tanhehco YC, Chen J, Foss CA, Fox JJ, Lemas V, et al.Визуализация ассоциированной с вирусом опухоли путем индукции экспрессии вирусного гена. Clin Cancer Res. (2007) 13: 1453–8. DOI: 10.1158 / 1078-0432.CCR-06-2295
PubMed Аннотация | CrossRef Полный текст | Google Scholar
20. Ивата С., Сайто Т., Ито Й, Камакура М., Гото К., Кавада Дж. И др. Противоопухолевое действие вальпроевой кислоты на Т-клетки, ассоциированные с вирусом Эпштейна-Барра, и клетки естественной киллерной лимфомы. Cancer Sci. (2012) 103: 375–81. DOI: 10.1111 / j.1349-7006.2011.02127.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Реактивация вируса Эпштейна – Барра, проявляющаяся в виде массивной спленомегалии после начала лечения голимумабом
Инфекция вирусом Эпштейна – Барра обычно протекает бессимптомно в острых случаях, когда конечным результатом инфекции является принятие фенотипа вирусной латентности.Вирус может реактивироваться в более позднем возрасте, что приводит к аномальной пролиферации инфицированных B-, T- или NK-клеток. Настоящим мы сообщаем о 71-летней женщине с серонегативным ревматоидным артритом, у которой наблюдалась массивная спленомегалия, панцитопения и позитивизация антител против двухцепочечной дезоксирибонуклеиновой кислоты (дцДНК) после инициации голимумаба против фактора некроза опухоли (TNF). Диагноз EBV-ассоциированного лимфопролиферативного расстройства (LPD) был продемонстрирован увеличением плазматической вирусной нагрузки EBV.Отмена анти-TNF и лечение ритуксимабом антителом к CD20 позволили обратить клинические отклонения. Связанные с EBV LPD описаны после начала применения других анти-TNF агентов, таких как инфликсимаб, но в литературе не найдено сообщений о связанном с голимумабом LPD EBV. Механизмы этого явления не ясны, но известно, что они включают экспрессию группы вирусных белков, специфичных для фенотипов вирусной латентности.
1. Введение
Вирус Эпштейна – Барра (EBV) – это гамма-герпесвирус, который преобладает у более чем 90% населения.Первичная инфекция чаще всего протекает бессимптомно и может проявиться позже в зрелом возрасте [1]. Хотя В-клетки являются основной мишенью ВЭБ из-за его тропизма к клеткам CD21 + , вирус также может инфицировать Т-клетки, NK-клетки и, реже, эпителиальные клетки. Вирус может оставаться в этих клетках в спящем состоянии и может реактивироваться позже во взрослом возрасте с помощью механизмов, которые плохо изучены. В этой статье сообщается о возникновении реактивации EBV, проявляющейся в виде биклонального лимфопролиферативного расстройства (LPD), у пациента с ревматоидным артритом, вызванной началом терапии с помощью противоопухолевого фактора некроза (TNF) голимумаба.
2. Описание клинического случая
71-летняя женщина обратилась в наше отделение неотложной помощи из-за боли в животе слева, усталости, анорексии, раннего насыщения и субфебрильной температуры в течение двух недель. Ей поставили диагноз серонегативный ревматоидный артрит (РА) на основании наличия воспалительного артрита с отрицательными антителами к антицитруллинированным пептидам (АСРА) и отрицательными ревматоидными факторами (РФ). Первоначально ее воспалительные симптомы контролировались с помощью этанерцепта, но за год до обращения ее заменили на тофацитиниб по причине хронического кашля.Однако тофацитиниб вызывал эпизоды повышенного артериального давления, головокружения и головных болей, поэтому голимумаб был назначен за три месяца до этого. Пока она принимала голимумаб, ее симптомы, связанные с артритом, контролировались. Другие ее лекарства включали метопролола тартрат, амлодипин, ирбесартан, левотироксин и парацетамол от артралгии. Недавно она вернулась из Южной Африки, где побывала только в городах. В семейном анамнезе сестры было замечательно наличие воспалительного заболевания кишечника и эссенциальной тромбоцитемии.В отличие от своей сестры, у пациентки никогда не было симптомов, связанных с воспалительным заболеванием кишечника или псориазом.
При осмотре показатели жизненно важных функций были в пределах нормы, обследование выявило отек нижних конечностей и пальпируемую селезенку. Лабораторные тесты показали наличие гемоглобина 8,0 г / дл с нормальным средним корпускулярным объемом и повышенным процентом ретикулоцитов до 5,27% с отрицательным прямым тестом на антиглобулин. Количество тромбоцитов составляло 4,4 × 10 10 / л, а количество лейкоцитов – 6.49 × 10 9 / л с 27% атипичных лимфоцитов. Эти параметры были нормальными до начала приема голимумаба. Химический состав сыворотки был нормальным, за исключением небольшого повышения щелочной фосфатазы на 178 МЕ / л (диапазон значений 45–117 МЕ / л) и лактатдегидрогеназы 641 МЕ / л (диапазон значений: 84–246 МЕ / л). Исследования железа показали, что в норме железо, трансферрин и ферритин, а гаптоглобин не обнаруживается. Ее С-реактивный белок был повышен до 99,1 мг / л. Антитело против двухцепочечной дезоксирибонуклеиновой кислоты (ДНК), определенное с помощью непрямого иммунофлуоресцентного анализа Crithidia luciliae , было положительным при 1:20.Другие антинуклеарные антитела были отрицательными. Больной госпитализирован. Компьютерная томография (КТ) брюшной полости продемонстрировала наличие массивной спленомегалии (рис. 1) с очаговой гипоаттенуацией и нормальным поглощением на позитронно-эмиссионной томографии (ПЭТ). Уровни C3 составляли 70 мг / л, а уровни C4 были в пределах нормы. Мазок периферической крови показал присутствие клеток Дауни типа II (рис. 2), а анализ высвобождения интерферона-γ дал отрицательный результат. Биопсия костного мозга выявила гиперклеточный костный мозг для возраста с трехлинейным гемопоэзом, гиперплазией эритроидов и легким ретикулиновым фиброзом.Проточная цитометрия крови показала, что лимфоцитоз состоит в основном из CD4 + Т-лимфоцитов без отклонений и 10% В-клеток. Наличие реактивных лимфоцитов побудило провести тестирование на вирусные инфекции. Вирусный капсидный антиген EBV (VCA), иммуноглобулин (Ig) G составлял 207 МЕ / мл, а определяемый EBV ядерный антиген (EBNA) IgG составлял 71,1 МЕ / мл, с отрицательным EBV VCA IgM и положительным CMV IgG с отрицательным CMV IgM. . Количественная ПЦР ДНК EBV на мононуклеарных клетках периферической крови дала положительный результат 1703 копий / мл.Перед началом исследования вирусная нагрузка ВЭБ не определялась. Пациентке перелили одну единицу эритроцитов, отменили голимумаб и выписали домой.
Шесть недель спустя она обратилась в офис с частичным улучшением ее начальных симптомов и уменьшением размера селезенки. Повторная проточная цитометрия показала, что B-клетки удвоились до 20-25% (рис. 3 (a)), биклональные для гена IGK (рис. 3 (b)) в исследованиях реаранжировки гена B-клеточного рецептора (BCR).Диагноз показал ятрогенное ВЭБ-ассоциированное B-клеточное лимфопролиферативное заболевание (LPD), и был назначен ритуксимаб. После двух месяцев лечения количество клеток крови нормализовалось, и селезенка стала непальпируемой. При последующих наблюдениях проточная цитометрия периферической крови не показала клональной популяции В-клеток, а вирусная нагрузка ВЭБ оставалась отрицательной. Анти-дцДНК оставалась положительной при разведении 1:80.
3. Обсуждение
У пациента развился LPD, связанный с иммунодефицитом (IDA), вызванный реактивацией EBV после введения голимумаба против фактора некроза опухоли (TNF).LPD – это общий термин, который варьируется от реактивной до моноклональной лимфоидной пролиферации со злокачественным поведением [2], и это отражает стадию цикла репликации EBV [3]. Несмотря на то, что точные события, которые приводят к экспрессии вирусных латентных фенотипов, четко не определены, они идентифицируются на основе экспрессии множественных ядерных антигенов (EBNA) и латентных мембранных белков (LMP), белков, которые помогают вирусу уклоняться от иммунитета. наблюдение. Комбинация различных изоформ каждого из этих белков и транскриптов позволяет различать по крайней мере три четко определенных паттерна латентности со специфическими клиническими проявлениями [3, 4].Представление LPD у пациента соответствовало экспрессии фенотипа с латентным периодом III, который связан с IDA-LPD, и является наиболее иммуногенным результатом экспрессии всех латентных транскриптов и белков EBV [3]. Ограниченная экспрессия кодируемых EBV малых РНК (EBER) или EBNA1 соответствует латентности паттерна I и происходит в B-клетках памяти. Выбранная экспрессия EBNA1, LMP1, LMP2A и LMP2B, EBER и правых транскриптов BamHI A (BART) определяет латентность паттерна II. Этот паттерн наблюдается в В-клетках зародышевого центра.Паттерн латентности III встречается в наивных В-клетках [3].
Фенотип с эксклюзивной латентностью I встречается при субклинической реактивной лимфоидной гиперплазии, лимфоме Беркитта, плазмобластной лимфоме и первичной лимфоме с выпотом. Коинфекция EBV в латентном паттерне I с вирусом герпеса человека 8 типа и вирусом иммунодефицита человека (ВИЧ) может привести к развитию моноклонального LPD. Паттерн латентности II встречается у иммунокомпетентных людей, у которых развивается EBV-ассоциированная лимфома Ходжкина, T / NK-клеточная лимфома и фолликулярная T-клеточная лимфома [3].Этот тип латентного периода также имеет место во время Hydroa Vaciniforme и тяжелой аллергии на укус комара, причем оба поликлональных LPD локализуются на коже и могут распространяться как ограниченный клонами LPD [5]. Латентный период III возникает в случае ВЭБ-ассоциированной диффузной крупноклеточной В-клеточной лимфомы, посттрансплантационных лимфопролиферативных расстройств, ДПЗ, связанных с иммунодефицитом, и ятрогенных ДПЗ. Выражение фенотипа с латентным периодом III связано с одновременным подавлением апоптоза и прогрессированием клеточного цикла до M фазы, что приводит к остановке роста и последующей иммортализации инфицированных лимфоцитов [5].
Реактивация EBV может быть связана с использованием блокаторов TNF [6], причем инфликсимаб является наиболее распространенным возбудителем в этом классе [7, 8]. Однако доказательства, связывающие использование агентов TNF в качестве независимого фактора риска развития ДПН, неубедительны: некоторые когорты демонстрируют повышенный риск развития лимфом [9], а другие демонстрируют несущественную связь [10, 11]. Это несоответствие может быть объяснено степенью активности РА, включая ранее неконтролируемое заболевание в анамнезе до начала применения блокатора ФНО, поскольку РА независимо связан с развитием ДПЗ, включая лимфомы, и риск, по-видимому, не полностью устранен. после применения любого из противоревматических препаратов, модифицирующих заболевание (БПВП) [12].Фактически, эти пациенты имеют более высокий риск развития лимфомы даже во время лечения [13]. Заболевание нашей пациентки имело низкую активность на основании ее симптомов, связанных с РА, в момент начала приема голимумаба, и решение о начале приема биологического агента было вызвано тем фактом, что она плохо реагировала на другие DAMRD в прошлом. включая метотрексат (MTX). Что касается тех случаев, которые возникают в связи с реактивацией ВЭБ, это кажется редким событием, и поэтому связь определить труднее.Это первое сообщение о случае ВЭБ-ассоциированного ДПЗ после начала приема голимумаба у пациента, который ранее подвергался воздействию в два отдельных момента ингибитора Янус-киназы и этанерцепта, и у которого после отмены произошла клиническая реверсия. Регресс LPD после отмены терапии также был описан для случаев RA-ассоциированных EBV-лимфом у пациентов, принимающих метотрексат [14], при этом наличие EBV в опухоли является предиктором возникновения этого феномена. Маловероятно, что тофацитиниб сыграл роль в этом случае, поскольку не было доказано, что этот агент влияет на вирусную нагрузку EBV или CMV [15].Следует отметить, что до настоящего времени не проводилось исследований, оценивающих влияние тофацитиниба на вирусную нагрузку ВЭБ у пациентов с РА, и имеющиеся данные получены от пациентов с псориазом, заболеванием, которое не имеет внутренней связи с развитием лимфом. Одним из потенциальных факторов, способствующих этой клинической картине, была история длительного использования этанерцепта пациентом, которое прекратилось за несколько месяцев до начала приема голимумаба, поскольку долгосрочные побочные эффекты от использования этих препаратов непредсказуемы [16].
Для диагностики нагрузка EBV в мононуклеарных клетках периферической крови (PBMC) может помочь определить, когда LPD управляется реактивацией EBV. В то время как вирусная нагрузка EBV выше 500 копий на 500 нг определяет связь реактивации EBV с LPD [17], пациенты с RA, как правило, имеют вирусную нагрузку, которая примерно в 10 раз выше, чем у пациентов без заболевания [18]. Использование анти-TNF терапии само по себе не связано с увеличением нагрузки EBV [19, 20]. Следовательно, кинетика вирусной нагрузки EBV имеет лучшую прогностическую ценность для диагностики EBV-ассоциированных LPD при мониторинге вирусной нагрузки EBV PBMC, а именно у пациентов, которые являются реципиентами аллотрансплантата или трансплантата гемопоэтических стволовых клеток (HSCT) [21].В этих случаях полезны исследования реаранжировки B-клеточного рецептора (BCR), так как они позволяют идентифицировать клональную природу LPD, поскольку большинство LPD, связанных с EBV, являются B-клетками по происхождению [2]. За исключением реактивных лимфоидных пролифераций, ДПЗ, ассоциированные с EBV, чаще всего являются моноклональными. Реже встречаются олигоклональные или поликлональные LPD.
Экспрессия вирусных белков во время реактивации ВЭБ может привести к перекрестной активации самореактивных Т- или В-клеток, явление, называемое антигенной мимикрией.Например, вирусный латентный белок EBNA-1 может приводить к образованию антител, способных связывать дцДНК [22]. Антинуклеарные антитела с высоким титром (ANA) также связаны с присутствием IgM или IgG против VCA EBV [23], хотя у нашего пациента ANA не определялась. Неизвестно, имеют ли эти антитела такое же иммунологическое и клиническое значение, что и при системной красной волчанке (СКВ), и это подтверждает теорию о том, что антитела дцДНК относятся к континууму, в котором антитела дцДНК с низкой авидностью могут развиваться спонтанно и могут быть обнаружены у некоторых здоровых людей, в то время как Антитела с более высокой авидностью более специфичны для пациентов с клиническим проявлением СКВ [24].Было показано появление анти-дцДНК во время терапии анти-TNF [25].
Лечение ВЭБ-ассоциированных ДПЗ зависит от иммунного статуса пациента и опухолевой патологии. В целом, у пациентов с ослабленным иммунитетом и, как показано в этом случае, отмена иммуносупрессивного инсульта является основой лечения; если это не удается, ритуксимаб является потенциальным дополнением к лечению B-клеточного LPD в этой ситуации [5]. Решение о добавлении химиотерапии зависит от первоначального гистологического диагноза, при этом для большинства В-клеточных лимфом высокой степени злокачественности требуются комбинированные схемы с добавлением ритуксимаба [5].Кроме того, пациентам, которым не удалось пройти начальное терапевтическое испытание из-за отмены препарата и использования ритуксимаба, может потребоваться противовирусная терапия в дополнение к химиотерапии, но этот подход все еще исследуется [5]. Рекомендации для случаев ятрогенных ВЭБ-ассоциированных ДПЗ после начала приема лекарств менее четко определены, но отмена одного лишь триггерного лекарства может изменить их. Трансплантация гемопоэтических стволовых клеток в дополнение к иммунохимиотерапии является эффективным подходом для лечения CAEBV или HLH со злокачественными характеристиками [26].Пациентам с сопутствующей ВИЧ-инфекцией требуется высокоактивное антиретровирусное лечение [5]. Более специфические методы лечения, нацеленные на клетки, инфицированные EBV, находятся в стадии разработки, и эти стратегии включают использование генной терапии для повышения чувствительности EBV в латентной фазе к противовирусным агентам или для индукции апоптоза клеток, инфицированных EBV, а также вливание аутологичных цитотоксических Т-лимфоцитов, специфичных против Белки латентного периода ВЭБ (CMD-003, baltaleucel-T) [27]. Другой многообещающий подход – индукция литического цикла EBV, который увеличивает чувствительность к противовирусным препаратам, достигается с помощью химиотерапии [27].
4. Заключение
Этот случай демонстрирует, что реактивация EBV происходит у пациентов с хроническими иммунологическими нарушениями после начала иммуномодулирующей терапии. Несмотря на то, что части молекулярных событий, связанных с латентным периодом EBV, известны, конкретные механизмы, с помощью которых анти-TNF агенты могут запускать развитие LPD, до конца не изучены. Основываясь на текущих данных, использование вирусной нагрузки EBV в сочетании с анализом проточной цитометрии являются полезными инструментами для выявления пациентов с потенциально излечимыми заболеваниями.